
- •1. Термодинамічні характеристики ідеальних газових сумішей
- •2. Термодинамічні характеристики ідеальних газових сумішей
- •4.1. Теплопровідність багатошарової плоскої стінки
- •5.Інфрачервоне випромінення поверхонь
- •6. Конвективний теплообмін
- •7. Розрахунок теплообмінних апаратів
- •8. Розрахунок масообмінних апаратів
- •Розрахунково-графічна робота з дисципліни «Основи термодинаміки, тепломасообміну і теплопередачі»
- •Література
- •1. Термодинамічні характеристики ідеальних газових сумішей……..…....4
- •2. Термодинамічні характеристики ідеальних газових сумішей .………... 6
1. Термодинамічні характеристики ідеальних газових сумішей
Завдання 1. Газова суміш задана складом
Відсоткове задання суміші (ri) |
РСМ, МПа |
VСМ, м3 |
tСМ, ОС |
ΔtСМ, ОС |
|||||||||
СО2 |
Н2 |
СО |
N2 |
Н2О |
О2 |
||||||||
|
|
|
20 |
40 |
40 |
1 |
0.5 |
1900 |
200 |
||||
Визначити: 1. Масові частки компонентів суміші; 2. Газові сталі компонентів та газову сталу суміші; 3. Середню молярну масу суміші; 4. Масу суміші та її окремих компонентів; 5. Парціальний тиск компонентів газової суміші.
Розв’язок.
1. Молекулярна маса складових газової суміші
μN2 = 0.028
μH2O= 0.018
μО2= 0.032
2. Газові сталі компонентів газової суміші

RN2
=
 =
297
=
297
RH2O=
 =
462
=
462
RО2
=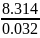 = 260
= 260
3. Газова стала суміші
RCM
=
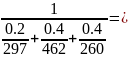 325
325
4
4. Середня молярна маса суміші, кг/моль
μсм
=
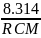 =
=

5. Парціальний тиск компонентів газової суміші
рN2=
rN2 PCM=
0.2
PCM=
0.2 = 2
= 2
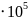 Па
Па
рH2O
= rH2O
PCM=
0.4
 =
=
 Па
Па
рО2 = rО2 PCM = 0.4 = 4 Па
6. Масові долі компонентів суміші

gN2
=

gH2O=

gО2
=

7. Загальна маса суміші, кг
MCM
=

8. Маса окремих компонентів суміші, кг
mN2 = gN2 MCM= 0.215 0.718 = 0.154
mH2O= gH2O MCM= 0.277 0.718 = 0.199
mО2 = gО2 MCM= 0.492 0.718 = 0.353
5
2. Термодинамічні характеристики ідеальних газових сумішей
Завдання 2.За умовою завдання 1 знайти: 1. Густину суміші та її окремих компонентів при заданих РСМ та VСМ; 2. Молярну, об’ємну та масову теплоємності суміші при Р=const та V=const; 3. Кількість теплоти на нагрівання суміші при заданій різниці температур.
Розв’язок.
1. Об’єм компонентів газової суміші, м3
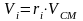
VN2 = 0.1
VH2O = 0.2
VО2 = 0.2
2. Густина суміші та її компонентів, кг/м3

ρCM=
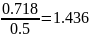
ρN2
=

ρH2O
=
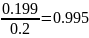
ρО2
=

3.Знаходимо
табличні
значення
середніх
мольних
теплоємностей
компонентів
газової
суміші при
t=1900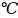 і
P=const, кДж/кмольОС
(додатокГ):
і
P=const, кДж/кмольОС
(додатокГ):
6
μcN2= 33.0846
μcH2O = 43.5447
μcО2 = 35.0108
4. Середня мольна теплоємність суміші при P=const, кДж/кмольОС
μcсм
=
Σri i
= 38.0391
i
= 38.0391
5. Середня мольна теплоємність при постійному об’ємі, кДж/кмольОС
μСv = μСр– 8.314 = 38.0391 – 8.314 = 29.7251
6. Середня масова теплоємність при P=const, Дж/кг ОС

СN2=

Сн2o
=
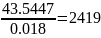
Со2
=

Середня теплоємність суміші:
Ccp
=

7. Середня масова теплоємність при V=const, Дж/кг ОС

Сv(N2) = 1182 – 297 = 885
Сv(Н2О) = 2419 – 462 = 1957
Сv(О2) = 1089– 260 = 829
суміші Сv(см) = 1224 7
8. Об’ємна теплоємність при P=const, Дж/м3 ОС

Ср(N2)
= 1182 1.540
= 1820
1.540
= 1820
Ср(Н2О) = 2419 0.995 = 2407
Ср(О2) = 1094 1.765 = 1931
середня теплоємність Ср(ср) = 2053
9. Об’ємна теплоємність при V=const, Дж/м3 ОС

Сv(N2) = 885 1.540 = 1363
Сv(Н2О) = 1957 0.995 = 1947
Сv(О2) = 829 1.765 = 1463
середня теплоємність Сv(ср) = 1591
10. Знаходимо кількість молей газу
N
=

N
=

11. Визначаємо кількість теплоти на нагрівання суміші при P=const, Дж
Q = Cp MCM Δt = 1565 0.718 (1900 - 200) = 1910239
12. Визначаємокількістьтеплоти на нагріваннясуміші при V=const, Дж
Q
= Сv
Mcм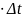 = 1224
0.718
1700
= 1494014.4
= 1224
0.718
1700
= 1494014.4
8
Рішення.
1. На I-d діаграмі вологого повітря визначаємо положення початкової (1) та кінцевої (2) точок процесу.
Для
цього, по ізотермі мокрого термометра
(tМ
) знаходимо точку на лінії
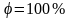 .
Через неї проводимо лінію i=const
до перетину
з ізотермою сухого термометра (tC
). Отримана на перетині точка (1, 2)
відображає стан цього вологого повітря.
.
Через неї проводимо лінію i=const
до перетину
з ізотермою сухого термометра (tC
). Отримана на перетині точка (1, 2)
відображає стан цього вологого повітря.
2. За допомогою I-d діаграми знаходимо термодинамічні характеристики кожної точки: вологовміст, відносну вологість, ентальпію, парціальний тиск водяної пари, температуру точки роси.
Для визначення вологовмісту повітря в точці 1 опускаємо вертикальну лінію з цієї точки до перетину шкалою вологовмісту.
d1 = 2.4 г/кг
d2 = 5.1 г/кг.
Відносну вологість повітря (%)визначаємо інтерполяцією між двома сусідніми лініями постійної вологості:
φ = 40%
Ентальпію (кДж/кг) визначаємо інтерполяцією між двома сусідніми лініями I=const.
І = 25.3 кДж/кг
Парціальний тиск водяної пари (кПа) знаходимо на шкалі, розташованій в нижній частині діаграми.
Р1 = 0.38 кПа
Р2 = 0.83 кПа.
Температуру точки роси визначаємо за ізотермою проведеною з точки перетину вертикальної лінії опущеної з точки 1 і лінії .
tp1 = -5 ОС
tp2 = 4.9 ОС.
10
3. З’єднуємо точки 1 і 2 прямою лінією та визначаємо напрямок променя процесу.
Методом паралельного перенесення суміщаємо лінію паралельну 1-2 з точкою яка має температуру 0 ОС і вологість 0 %. Продовжуємо цю лінію до границі діаграми і визначаємо ε.
ε
 -0.8 кДж/кг
-0.8 кДж/кг
В даному випадку спостерігається процес політропного охолодження зі зволоженням.
