
- •1 Исходные данные
- •2 Расчет газового цикла при постоянной теплоемкости
- •2.1 Определение параметров для основных точек цикла
- •2.2 Определение для каждого процесса
- •2.3 Определение q, l, lI, , в каждом процессе
- •2.4 Определение lЦ, t, Pi
- •3 Расчет газового цикла с учетом переменной теплоемкости
- •3.1 Определение параметров для основных точек цикла
- •3.2 Определение для каждого процесса
- •3.3 Определение q, l, l, , в каждом процессе
- •3.4 Определение lц, t, pi
- •4 Графики цикла
- •Список использованных источников
2.4 Определение lЦ, t, Pi
Полезная работа газа за цикл определяется:
- как разность работ расширения и сжатия,
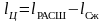 ,
(25)
,
(25)
где lЦ – полезная работа газа за цикл,
- как разность теплоты, подведенной и отведенной:
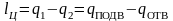 .
(26)
.
(26)
С учетом знаков плюс и минус полезная работа за цикл определяется как алгебраическая сумма:
 ,
(27)
,
(27)
или
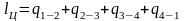 ,
(28)
,
(28)
или
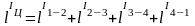 ,
(29)
,
(29)
Определяем по формуле (27):
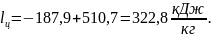
Знак плюс соответствует положительному направлению процесса, то есть подводу тепла и расширению. Знак минус – отводу тепла и сжатию.
Термический к.п.д.:
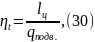
где t – термический к. п. д.,
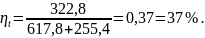
Термический к.п.д. цикла, по формуле (31):

Среднецикловое давление (индикаторное):

где Pi – среднецикловое давление,
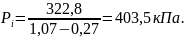
3 Расчет газового цикла с учетом переменной теплоемкости
с = f(t),
Расчет производится с помощью таблиц термодинамических свойств газов.
3.1 Определение параметров для основных точек цикла
Параметры P, V, t определяют также по уравнению состояния (4) и соотношении параметров в процессах, приведенных ранее. Исключение составляет адиабатный процесс. Поскольку с = f(t), то показатель адиабаты зависит от температуры.
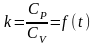 (33)
(33)
Поэтому соотношения формулы (34)
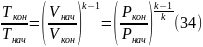
заменяют выражениями (35) и (36)
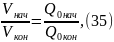

Безразмерные величины относительный объем 0 и относительное давление 0 взять из таблицы в зависимости от температуры.
Параметры U, i, S находят по таблицам, в которых отсчет внутренних удельных энергий, энтальпий и энтропий начинается с 0 К.
Для точки 1:
T1=273+800C=353 К,
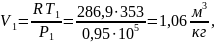
Рассмотрим адиабатный процесс 1-2:
При t1=800C (T1=353 K) относительный объем 01=4210, тогда из формулы (35):

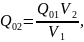
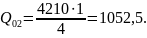
По таблице находим t2332,40C (T2 605,4 K).
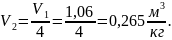
По таблице находим
01 = 2,4553,
02 16,8497, тогда из формулы (36):
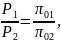
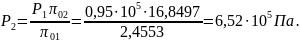
Из графика видно:


Рассмотрим изохору 2-3:
P3=P22,4=6,521052,4=15,65105 Па,

Рассмотрим политропный процесс 3-4:
P3V3n=P4V4n , (37)
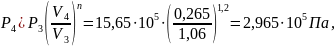
В формулу (7) предыдущего раздела подставляем соотношение параметров для политропы, получаем формулу (12) и выражаем T4:
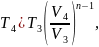
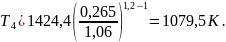
Параметры U, i, S найдем из таблицы (приблизительно). Все результаты параметров в таблице 4.
Таблица 4 – Результаты определения параметров в точках
№ точки |
P, 105 Па |
V, м3/кг |
t, 0C |
Т, К |
U, кДж/кг |
i, кДж/кг |
S, кДж/(кг·К) |
1 |
0,95 |
1,06 |
80 |
353 |
252,80 |
353,60 |
6,8662 |
2 |
6,52 |
0,26 |
332 |
605 |
438,64 |
612,20 |
7,4182 |
3 |
15,6 |
0,26 |
1151 |
1424 |
1135,5 |
1544,2 |
8,3825 |
4 |
2,96 |
1,06 |
806 |
1079 |
827,06 |
1136,8 |
8,0552 |
