
- •1 Исходные данные
- •2 Расчет газового цикла при постоянной теплоемкости
- •2.1 Определение параметров для основных точек цикла
- •2.2 Определение для каждого процесса
- •2.3 Определение q, l, lI, , в каждом процессе
- •2.4 Определение lЦ, t, Pi
- •3 Расчет газового цикла с учетом переменной теплоемкости
- •3.1 Определение параметров для основных точек цикла
- •3.2 Определение для каждого процесса
- •3.3 Определение q, l, l, , в каждом процессе
- •3.4 Определение lц, t, pi
- •4 Графики цикла
- •Список использованных источников
Министерство образования и науки Российской Федерации
федеральное государственное автономное образовательное учреждение
высшего профессионального образования
|
«Северный (Арктический) федеральный университет имени М.В.Ломоносова»
Кафедра теплотехники |
|
||||||||||||||
|
(наименование кафедры) |
|
||||||||||||||
|
|
|
||||||||||||||
|
Павловская Полина Юрьевна |
|
||||||||||||||
|
(фамилия, имя, отчество студента) |
|
||||||||||||||
|
|
|
||||||||||||||
|
Институт |
ЭиТ |
курс |
II |
группа |
617 |
|
|
||||||||
|
|
|
||||||||||||||
|
|
|
||||||||||||||
|
|
|
||||||||||||||
|
РАСЧЁТНО-ГРАФИЧЕСКАЯ РАБОТА |
|
||||||||||||||
|
|
|
||||||||||||||
|
По дисциплине |
|
Техническая термодинамика |
|
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
На тему |
|
«Расчет газового цикла» |
|
||||||||||||
|
|
(наименование темы) |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||||||
|
Отметка о зачёте |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
(дата) |
|
||||||||
|
|
|
|
|
||||||||||||
|
Руководитель |
|
|
|
|
|
|
|||||||||
|
|
|
(должность) |
|
(подпись) |
|
(и.,о., фамилия) |
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
(дата) |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
Архангельск |
|
||||||||||||||
|
2012 |
|
||||||||||||||
ЛИСТ ДЛЯ ЗАМЕЧАНИЙ
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОГЛАВЛЕНИ
РАСЧЁТНО-ГРАФИЧЕСКАЯ РАБОТА 1
1 Исходные данные 3
2 Расчет газового цикла при постоянной теплоемкости 5
2.1 Определение параметров для основных точек цикла 6
2.2 Определение для каждого процесса 11
2.3 Определение q, l, lI, , в каждом процессе 13
2.4 Определение lЦ, t, Pi 16
3 РАСЧЕТ ГАЗОВОГО ЦИКЛА С УЧЕТОМ ПЕРЕМЕННОЙ ТЕПЛОЕМКОСТИ 19
3.1 Определение параметров для основных точек цикла 19
3.2 Определение для каждого процесса 22
3.3 Определение q, l, l, , в каждом процессе 24
3.4 Определение lц, t, pi 27
4 Графики цикла 29
Вывод 31
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 32
1 Исходные данные 3
2 Расчет газового цикла при постоянной теплоемкости 5
2.1 Определение параметров для основных точек цикла 5
2.2
Определение
 для каждого процесса 9
для каждого процесса 9
2.3 Определение q, l, lI, , в каждом процессе 10
2.4 Определение lЦ, t, Pi 12
3 РАСЧЕТ ГАЗОВОГО ЦИКЛА С УЧЕТОМ ПЕРЕМЕННОЙ ТЕПЛОЕМКОСТИ 14
3.1 Определение параметров для основных точек цикла 14
3.2 Определение для каждого процесса 16
3.3 Определение q, l, l, , в каждом процессе 18
3.4 Определение lц, t, pi 19
4 Графики цикла 21
Вывод 23
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 24
1 Исходные данные
8 вариант
Рабочее тело обладает свойствами воздуха, масса равна 1 кг.
Газовый цикл состоит из четырёх процессов, определяемых по показателю политропы. Известны начальные параметры в точке 1 (давление и температура), а также безразмерные отношения параметров в некоторых процессах.
Данные для расчётов:
Показатель политропы n
1 – 2: К
2 – 3: ∞
3 – 4: 1,2
4 – 1: ∞
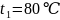
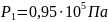
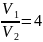
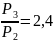

Требуется
1) Определить параметры P, , t, U, I, S для основных точек цикла.
2) Определить для каждого
процесса
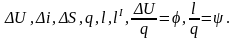
3) Определить работу газа за цикл lц, термический к.п.д. и среднецикловое давление рi.
4) Построить в масштабе цикл в координатах P, v; T, S.
5) Расчет произвести в двух вариантах:
а) при постоянной теплоемкости с f(t);
б) при переменной теплоемкости с = f(t).
2 Расчет газового цикла при постоянной теплоемкости
Теплоемкость в этом варианте расчета не зависит от температуры, с f(t), и определяется по молекулярно-кинетической теории. Так как рабочим телом согласно заданию является воздух, то теплоемкости определяются для двухатомного газа.
Изохорная теплоемкость:

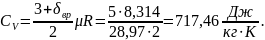
Изобарная теплоемкость:
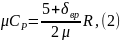

Удельная газовая постоянная определяется из соотношения
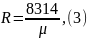
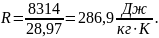
2.1 Определение параметров для основных точек цикла
Параметры p, V, T определяются c использованием уравнения состояния (4) и соотношений параметров в процессах

T1 = 273,15+800C = 353 К,
где T1 – температура точки цикла,

где
 – объем точки цикла,
– объем точки цикла,

Рассмотрим процесс 1 – 2: Адиабата
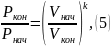
Преобразуем формулу (5)

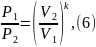
где k – показатель адиабаты.
Выразим
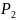 из формулы (6), где k =
1,4 ,
из формулы (6), где k =
1,4 ,
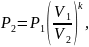
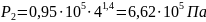 .
.
В формулу (7) подставляем соотношение параметров для адиабаты, получаем формулу (8) и выражаем V2:


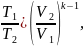

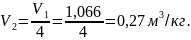
Из графика видно:
 ,
,
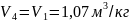 .
.
Рассмотрим процесс 2 – 3: Изохора

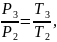
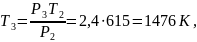
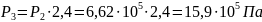 .
.
Рассмотри процесс 3 – 4: Политропа
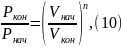
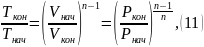


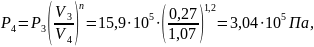
В формулу (7) подставляем соотношение параметров для политропы, получаем формулу (12) и выражаем T4:


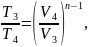
где n – показатель политропы,
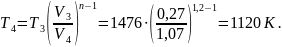
Параметры U, i, S определяют, выбрав начало отсчета. Условно считая при t0=0 0C, Р0 = 760 мм рт. ст. = 101325 Па удельную внутреннюю энергию, удельную энтальпию и удельную энтропию идеального газа равными нулю, получаем:
U = CV T, (13)
i = CP T, (14)
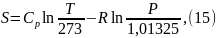
где P – давление [бар],
i – удельная энтальпия,
U – удельная внутренняя энергия,
S – удельная энтропия.
Находим параметр U по формуле (13),
где CV
= 717,46 Дж/(кг
 К):
К):
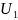 =
CV
T1=
717,46
353
= 253265,498 Дж/кг =253,3 кДж/кг;
=
CV
T1=
717,46
353
= 253265,498 Дж/кг =253,3 кДж/кг;
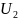 = CV
T2 =
717,46
615
= 441,2 кДж/кг;
= CV
T2 =
717,46
615
= 441,2 кДж/кг;
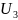 = CV
T3
= 717,46
1476
= 1059 кДж/кг;
= CV
T3
= 717,46
1476
= 1059 кДж/кг;
 = CV
T4
= 717,46
1120
= 803,5кДж/кг.
= CV
T4
= 717,46
1120
= 803,5кДж/кг.
Находим параметр i по формуле (14),
где Ср=1004,45 Дж/(кг К):
i1 = CP T1= 1004,45 353 = 354570,85 Дж/кг = 354,57 кДж/кг;
i2 = CP T2 = 1004,45 615 = 617,74 кДж/кг;
i3 = CP T3 = 1004,45 1476 = 1482,6кДж/кг;
i4 = CP T4 = 1004,45 1120 = 1124,9кДж/кг.
Находим параметр S по формуле (15):
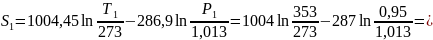
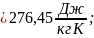

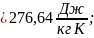
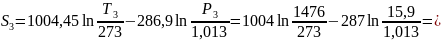

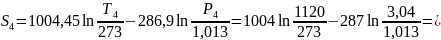
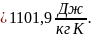
Результаты определения параметров в точках сводятся в таблицу 1.
Таблица 1 – Результаты определения параметров в точках
№ точки |
P, 105 Па |
V, м3/кг |
t, 0C |
Т, К |
U, кДж/кг |
i, кДж/кг |
S, кДж/(кг·К) |
1 |
0,95 |
1,07 |
80 |
353 |
253,3 |
354,57 |
0,276 |
2 |
6,62 |
0,27 |
342 |
615 |
441,2 |
617,74 |
0,277 |
3 |
15,9 |
0,27 |
1203 |
1476 |
1059 |
1482,6 |
0,904 |
4 |
3,04 |
1,07 |
847 |
1120 |
803,5 |
1124,9 |
1,102 |
