
- •В.Ф. Шульгин, н.С. Певзнер
- •Симферополь - 2004
- •Лекция № 1. Предмет химии. Современное атомно-молекулярное учение. Основные понятия химии, законы стехиометрии
- •Лекция № 2. Основные положения квантово-механической теории строения атома
- •Литература: [1] с. 55 - 81; [2] с. 43 - 59; [3] с. 20 - 30 Лекция № 3. Принципы описания электронной оболочки многоэлектронного атома. Периодическая система химических элементов д.И. Менделеева
- •Литература: [1] с. 81 - 98; [2] с. 60 - 103; [3] с. 30 - 46 Лекция № 4. Основы теории химической связи. Метод валентных связей
- •Основные положения метода валентных связей
- •Литература: [1] с. 109 - 135; [2] с. 104 - 118; [3] с. 70 - 90 Лекция № 5. Метод молекулярных орбиталей
- •Литература: [1] с. 135 - 143; [2] с. 118 - 126; [3] с. 52 - 63
- •Литература: [1] с. 143 - 158, 513 - 519; [2] с. 133 - 161; [3] с. 90 - 96
- •Литература: [1] с. 158 - 157, 182 - 196; [2] с. 162 - 195; [3] с. 155 - 174
- •Химическое равновесие, принцип Ле Шателье
- •Литература: [1] c. 163 - 182; [2] с. 184 - 228; [3] с. 172 - 199
- •Физико-химические свойства растворов неэлектролитов
- •Литература: [1] с. 205 - 222; [2] с. 229 - 253 Лекция № 10. Растворы электролитов. Теория электролитической диссоциации
- •Лекция № 11. Теории кислот и оснований
- •Литература: [1] с. 234 - 237; [2] с. 309 - 313; [3] с. 131 - 132 Лекция № 12. Электролитическая диссоциация воды. Расчет значений рН водных растворов кислот, оснований и солей
- •Литература: [1] с. 243 - 255; [2] с. 296 - 302 Лекция № 13. Буферные растворы. Равновесия в растворах малорастворимых электролитов. Произведение растворимости
- •Литература: [1] с. 241 - 242; [2] с. 298 - 299, 302 - 304 Лекция № 14. Окислительно-восстановительные реакции
- •Литература: [1] c. 255 - 263; [2] с. 317 - 326; [3] с. 206 - 210
- •Литература: [1] с. 263 - 293; [2] с. 326 - 360; [3] с. 214 - 216 Лекция № 16. Дисперсные системы, коллоидные растворы
- •Литература: [1] с. 295 - 330; [2] с. 254 - 262 Лекция № 17. Координационные соединения
- •Литература: [1] с. 563 - 587; [2] с. 367 - 396 Лекция № 18. Водород
- •Соединения водорода
- •Литература: [1] с. 330 - 338, [2] с. 411 - 415, [3] с. 262 - 270 Лекция № 19. Элементы VII-a-подгрупы (галогены)
- •Cоединения галогенов
- •Лекция № 20. Элементы via-подгруппы
- •20.1. Кислород и его соединения
- •20.2. Сера и ее соединения
- •Соединения серы
- •20.3. Селен, теллур и их соединения
- •Литература: [1] с. 359 - 383, [2] с. 425 - 435, [3] с. 297 - 328 Лекция № 21. Элементы va-подгруппы
- •21.1. Азот и его соединения
- •Соединения азота
- •21.2. Фосфор и его соединения
- •Соединения фосфора
- •21.3. Элементы подгруппы мышьяка
- •Литература: [1] с. 383 - 417, [2] с. 435 - 453, [3] с. 328 - 371 Лекция № 22. Элементы iva-подгруппы
- •22.1. Углерод и его соединения
- •Соединения углерода
- •22.2. Кремний и его соединения
- •Соединения кремния
- •22.3. Германий, олово, свинец
- •Литература: [1] с. 417 - 435, 491 - 513, [2] с. 453 - 472, [3] с. 371 - 409 Лекция № 23. Элементы iiia-подгруппы
- •23.1. Бор и его соединения
- •Соединения бора
- •23.2. Алюминий и его соединения
- •Соединения алюминия
- •23.3. Подгруппа галлия
- •Литература: [1] с. 608 - 619, [2] с. 472 - 481, [3] с. 412 - 446 Лекция № 24. Элементы iia-подгруппы
- •24.1. Бериллий и его соединения
- •24.2. Магний и его соединения
- •22.3. Щелочноземельные металлы
- •Литература: [1] с. 587 - 599, [2] с. 481 - 486, [3] с. 447 - 460 Лекция № 25. Элементы ia-подгруппы (щелочные металлы)
- •Литература: [1] с. 543 - 551, [2] с. 486 - 489, [3] с. 461 - 470 Лекция № 26. Общая характеристика d-элементов. Элементы iiiв - vb подгрупп (подгруппы скандия,титана и ванадия)
- •26.1. Общая характеристика d-элементов
- •26.2. Элементы iiiв подгруппы (подгруппы скандия)
- •26.3. Элементы ivв подгруппы (подгруппы титана)
- •26.4. Элементы vв подгруппы (подгруппы ванадия)
- •Литература: [1] с. 619 - 633, [2] с. 489 - 523, [3] с. 478 - 481, 499 - 520 Лекция № 27. Элементы viв и viiв-подгрупп (подгруппы хрома и марганца)
- •27.1 Элементы viв-подгруппы (подгруппа хрома)
- •27.2. Элементы viiв-подгруппы (подгруппа марганца)
- •Литература: [1] с. 633 - 645, [2] с. 523 - 539, [3] с. 521 - 548 Лекция № 28. Элементы viiib-подгруппы
- •28.1. Элементы подгруппы железа
- •Соединения железа
- •28.2. Элементы подгруппы кобальта
- •28.3. Элементы подгруппы никеля
- •Литература: [1] с. 650 - 679, [2] с. 540 - 550, [3] с. 548 - 584 Лекция № 29. Элементы ib- и iib-подгрупп (подгруппы меди и цинка)
- •29.1 Элементы ib-подгруппы (подгруппы меди)
- •29.2 Элементы iib-подгруппы (подгруппы цинка)
- •Литература: [1] с. 551 - 563, 599 - 608, [2] с. 550 - 554, [3] с. 585 - 602 Лекция 30. Основы геохимии.
- •30.1. Теория строения атомных ядер. Радиоактивность.
- •30.2. Распространенность химических элементов
- •30.3. Миграция химических элементов. Факторы миграции
- •Список рекомендуемой литературы
- •Оглавление
Соединения водорода
Если учесть органические вещества, то следует признать, что водород - элемент, образующий наибольшее число соединений. Важнейшими неорганическими соединениями водорода являются гидриды и бинарные соединения водорода в степени окисления +1. Последние также часто называют гидридами, что не совсем корректно, ибо гидриды - это бинарные соединения водорода в степени окисления -1. "Классические гидриды" могут образовывать только те элементы, электроотрицательность у которых значительно меньше, чем у водорода. Это щелочные и щелочноземельные металлы, а также магний и бериллий. Они образуют типичные солеподобные гидриды, при электролизе расплавов которых водород выделяется на аноде:
2H- - 2e- H20
При взаимодействии гидридов данного типа с водой также выделяется водород:
NaH-1 + H2+1O = NaOH + H20
Элементы, электроотрицательность которых незначительно отличается от водорода, образуют ковалентные гидриды (B2H6, SiH4). Известно небольшое число комплексных гидридов, например, Li[AlH4], Na[BH4], которые широко применяются в органическом синтезе в качестве восстановителей.
Из бинарных соединений водорода в степени окисления +1 в данном разделе будет рассмотрен оксид водорода (вода) и его пероксид (перекись водорода).
Химически чистая вода представляет собой бесцветную жидкость без вкуса и запаха. Молекула воды - Н2О - имеет угловое строение. Образование молекулы воды происходит с участием sp3-гибридных орбиталей атома кислорода, две из которых заняты неподеленными электронными парами и поэтому вклада в геометрию молекулы не вносят. Перекрывание одноэлектронных облаков двух гибридных орбиталей кислорода и 1s-орбиталей двух атомов водорода приводит к образованию уголковой молекулы. Отталкивающие действие двух неподеленных пар электронов уменьшает валентный угол HOH до 104,5 (см. стр. 19).
В кристаллическом состоянии молекула воды, окруженная четырьмя соседями, образует с ними очень прочные водородные связи, вследствие чего вода обладает аномально высокой температурой кристаллизации (0 ) и кипения (100 С). Согласно клатратной теории в жидкой воде существуют микроскопические фрагменты кристаллической структуры льда - клатраты, находящиеся в равновесии с жидкой фазой.
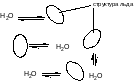
За счет образования прочных водородных связей, а также координационных соединений, вода является хорошим растворителем для многих типов органических и неорганических соединений, частицы которых существуют в растворах в виде аддуктов с молекулами воды - гидратов. При выделении из водных растворов многие вещества кристаллизуются в виде гидратов, образуя кристаллогидраты. Можно выделить три типа кристаллогидратов, отличающихся характером связывания воды:
1. Клатраты - имеющие кристаллическую структуру льда, полости которой заняты частицами вещества. Такое строение имеют кристаллогидраты солей щелочных металлов, содержащие большое количество воды, например, Na2SO410H2O, а также кристаллогидраты, образуемые галогенами и инертными газами - Cl28H2O, или Ar 6H2O.
2. Аквакомплексы, содержащие воду, координированную катионом металла, чаще всего переходного, например, CoCl26H2O, точнее [Co(OH2)6]Cl2.
3. Кристаллогидраты, содержащие воду, связанную с частицами вещества водородными связями. Часто этот тип связывания воды реализуется в кристаллогидратах органических веществ.
С химической точки зрения вода довольно реакционноспособное соединение, вступающее во взаимодействие с различными простыми и сложными веществами, в том числе с органическими соединениями.
Кроме оксида водорода хорошо изучен его аналог - оксид дейтерия - D2O, более известный под названием "тяжелая вода". Тяжелая вода широко применяется в атомной энергетике как замедлитель нейтронов. Реакции с участием тяжелой воды идут медленней, а температура ее кипения (101,4 С) несколько выше по сравнению с H2O, поэтому при проведении электролиза или дистилляции большого количества воды тяжелая вода накапливается в остатке.
Пероксид водорода (перекись) - Н2О2 - бесцветная сиропообразная жидкость (d = 1,45 г/см3), неустойчивая в чистом виде, но устойчивая в водных растворах до 30% концентрации. Распад пероксида водорода катализируется соединениями тяжелых металлов, например, MnO2.
2Н2О2 = 2Н2О + О2
Получают пероксид водорода электролизом водных растворов серной кислоты или гидросульфата аммония. При этом на аноде образуется пероксосерная кислота, гидролиз которой приводит к образованию пероксида водорода:
2HSO4- - 2e- H2S2O8
H2S2O8 + 2H2O = 2H2SO4 + H2O2
Вследствие промежуточной степени окисления кислорода (-1), пероксид водорода, в зависимости от условий проведения реакции, может быть как окислителем, так и восстановителем. В кислой среде H2O2 довольно сильный окислитель:
H2O2 + 2H+ + 2e- 2H2O; E0 = 1,78 В
В то же время пероксид водорода окисляется более сильными окислителями, например, перманганатом калия:
2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + 5O2 + K2SO4 + 8H2O
Водные растворы пероксида водорода (в основном 3%) применяются для отбелки тканей и меха, дезинфекции, консервации, протравливания семян. Важную роль пероксид водорода играет в процессах самоочищения природных водоемов, в которых он содержится в ничтожной концентрации (порядка 310-5 моль/л), но тем не менее, эффективно окисляет биологические загрязнения.
