
Лабораторная работа №4
Определение поверхностного натяжения жидкости методом измерения максимального избыточного давления в пузырьках воздуха.
Цель: Изучение понятия поверхностных явлений, их проявлений в различных областях.
Задача: Определение коэффициента поверхностного натяжения
Принадлежности: аспиратор, манометр, сосуд в форме пробирки с боковым отростком и пробкой, трубка с оттянутым концом, два стакана, термометр, электроплитка, мешалка, штатив, исследуемая жидкость.
Краткая теория:
Поверхность и поверхностные явления
Поверхность – это граница раздела между двумя контактирующими средами. В каждой из сред вблизи от поверхности простирается слой, в котором элементный состав и химическое состояние, атомная и электронная структура, и следовательно весь комплекс свойств: механические, электрические, магнитные, химические и др. существенно отличаются от свойств в объеме. Толщина этого слоя в зависимости от характерной для данного физического явления длины может быть различной , так для 10-10…10-5м.
Поверхностный слой анизотропен. Плотность, вязкость, поляризуемость и т.п. его отличаются от объемных фаз. В поверхностных слоях наблюдаются специфические химические эффекты: смещение химического равновесия, изменение констант скоростей реакций и т.д., а у Sm и Cr даже меняется валентность.
Особыми свойствами обладают и родственные поверхностным слоям малые (хотя бы в толщину) объекты – тонкие пленки и нити, узкие щели и поры микроскопических размеров.
Явления, связанные с существованием межфазных границ и их особыми свойствами, называются поверхностными явлениями. Это адсорбция (преимущественная концентрация молекул газа или растворенного в жидкости вещества на поверхности жидкости или твердого тела), адгезия (взаимодействие между молекулами различных фаз, прилипание), поверхностный электрический потенциал, капиллярные явления и многое другое.
Любая поверхность обладает некоторой избыточной поверхностной энергией, так как образование новой поверхности требует разрыва или перестройки связей между атомами или молекулами в конденсированной среде. Работа образования единицы площади поверхности равна удельной поверхностной свободной энергии или иначе поверхностному натяжению.
Когда в однородной среде начинает выделяться новая фаза необходимость затраты энергии на образование межфазной поверхности приводит к явлениям перегрева или переохлаждения
Работа образования единицы поверхности σ путем разрезания описывается обобщенным уравнением Гиббса. Это уравнение устанавливает связь между важнейшими поверхностными явлениями – адсорбцией и поверхностной активностью.
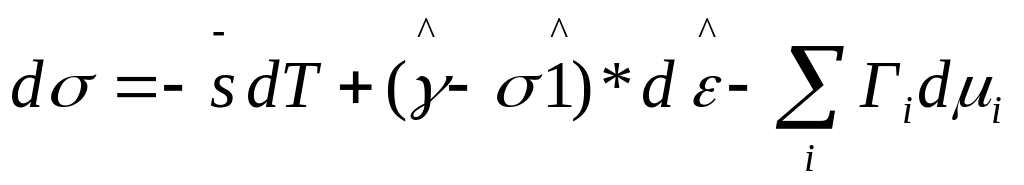 (1)
(1)
где
![]() −
удельная поверхностная
энтропия;
−
удельная поверхностная
энтропия;
![]() −
тензор поверхностных
натяжений;
−
тензор поверхностных
натяжений;
![]() −
тензор деформации;
−
тензор деформации;
![]() −
химические потенциалы
молекул разных компонентов;
−
химические потенциалы
молекул разных компонентов;
![]() −
их адсорбции,
суммирование производится по всем
компонентам, для которых возможно
равновесие между объемной фазой и
поверхностным слоем.
−
их адсорбции,
суммирование производится по всем
компонентам, для которых возможно
равновесие между объемной фазой и
поверхностным слоем.
Таким образом, поверхностная энергия σ имеет три составляющие: энтропийную, деформационную и химико-адсорбционную. Для жидкостей поверхностная энергия σ сводится к энергии поверхностного натяжения γ, причем деформационная составляющая отсутствует.
Поверхностное натяжение
Поверхностное натяжение γ − это механическая и термодинамическая характеристика межфазной поверхности, определяемая межмолекулярными взаимодействиями и структурой поверхностного слоя. Термодинамически γ определяется как работа обратимого образования новой поверхности путем растяжения старой.
П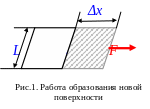 усть
полоску поверхности жидкости шириной
L
растягивают
силой F
на дополнительную длину Δх.
Работа
ΔА,
затраченная на создание
дополнительной площади ΔS
= LΔх,
равна
ΔА=F
Δх.
усть
полоску поверхности жидкости шириной
L
растягивают
силой F
на дополнительную длину Δх.
Работа
ΔА,
затраченная на создание
дополнительной площади ΔS
= LΔх,
равна
ΔА=F
Δх.
Вводя в общем случае σ − удельную энергию единицы площади поверхности, имеем:
![]() (2)
(2)
Для жидкости поверхностная энергия равна поверхностному натяжению, поэтому можно использовать коэффициент γ, называемый коэффициентом поверхностного натяжения.
Коэффициент поверхностного натяжения γ, как видно из (2), имеет как энергетический, так и силовой смысл: он также может быть определен как сила поверхностного натяжения, действующая на единицу длины поверхности пленки жидкости.
Единицей измерения поверхностного натяжения будет [γ ] =1 Н/м для силового выражения или 1 Дж/м2 для энергетического. Для большинства жидкостей при нормальных температурах значение γ лежит в пределах 0,01…0,1 Н/м.
Следствием адгезии жидкости к определенной поверхности является смачивание, проявляющееся в растекании жидкости по этой поверхности и формировании так называемого адгезионного контакта.
Смачивание
В зависимости от соотношения энергий адгезии и когезии (межмолекулярного взаимодействия внутри объема самого вещества), на поверхности раздела фаз действуют силы поверхностного натяжения. Поэтому капля жидкости, лежащей на твердой поверхности, получает определенную форму (рис.2)
У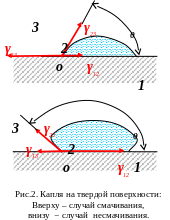 словие
равновесия в точке О между силами
поверхностного натяжения γ12−на
поверхности раздела «1 (твердое тело)
−2 (жидкость)», γ13−на
«1−3 (воздух); γ23−
на поверхности раздела «2-3»:
словие
равновесия в точке О между силами
поверхностного натяжения γ12−на
поверхности раздела «1 (твердое тело)
−2 (жидкость)», γ13−на
«1−3 (воздух); γ23−
на поверхности раздела «2-3»:
cos θ = (γ13 − γ12)/ γ23 (3)
здесь θ − краевой угол (угол смачивания). θ острый в случае смачивания и тупой при несмачивании.
При контакте жидкости с твердым телом поверхность жидкости искривляется и становится либо выпуклой либо вогнутой. Силы поверхностного натяжения дают равнодействующую, направленную всегда в сторону центра кривизны. Таким образом, внутри всякой искривленной поверхности создается добавочное, вызванное именно кривизной поверхности, давление.
Капиллярные явления
Следствием этого являются капиллярные явления. Если поместить узкую трубку (капилляр) одним концом в жидкость, налитую в широкий сосуд, то вследствие смачивания или несмачивания жидкостью стенок капилляра кривизна мениска − поверхности жидкости в капилляре становится значительной. В случае смачивания мениск вогнутый, при несмачивании − выпуклый. Над вогнутой поверхностью воды создается дефицит давления ΔР. Вследствие этого жидкость поднимается по капилляру на такую высоту h, чтобы вес столбика жидкости на уровнем воды в сосуде уравнял бы силу давления этого дефицита:
Vρg = πr2hρg = πr2ΔР =2 πrγ
где V – объем жидкости; ρ −плотность жидкостиg; r − радиус капилляра; πr2 -- площадь сечения и 2πr − окружность сечения капилляра, h – высота столбика жидкости.
Имеем тогда высоту
столбика воды в капилляре
![]() .
.
Вода может подниматься по узким капиллярам на значительную высоту (до 3 м), что имеет важное значение в природе. Ступенчатой капиллярной подачей растения обеспечивают живительной влагой листья на кроне на высоту десятки метров. В технике и быту капиллярные явления используются в фитилях, системах смазки, химическом производстве и т.д.
Как следует из уравнения (1) поверхностное натяжение в жидкостях помимо энтропийной составляющей имеет адгезионную. Поверхностно-активные вещества (ПАВ) значительно снижают адгезию, тем самым и поверхностное натяжение (например мыло снижает γ с 0,075 до 0,045 Н/м). Сахар и соль, наоборот, увеличивают γ воды.
Поверхностные явления играют важную роль в процессах в живой и неживой природы, во всех областях человеческой жизнедеятельности.
В последние годы быстро развиваются нанотехнологии, в которых для получения новых материалов и конструкций реализуются специфические свойства поверхностных слоев.
