
3.5. Политропный процесс
Политропный процесс
можно определить как термодинамический
процесс изменения параметров идеального
газа при постоянной теплоемкости
![]() .
.
Все термодинамические процессы являются частными случаями политропного процесса.
Для политропного процесса первое начало термодинамики имеет вид
![]() (45)
(45)
или
![]() (46)
(46)
где
![]()
массовая теплоемкость газа в политропном
процессе.
массовая теплоемкость газа в политропном
процессе.
Также первое начало термодинамики для политропного процесса можно представить в виде
![]() (47)
(47)
или
![]() (48)
(48)
Из выражения первого начала термодинамики в форме (46) найдем уравнение политропного процесса
![]()
![]() (49)
(49)
Воспользуемся выражением (35)
![]() ,
,
тогда
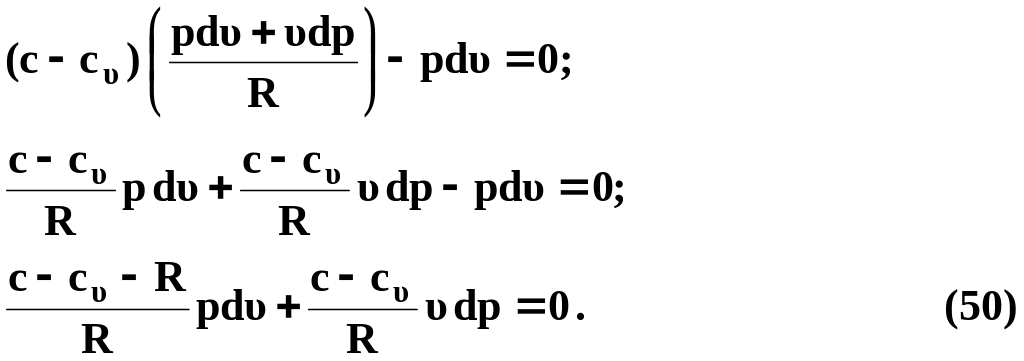
Согласно формуле Майера
![]() ,
,
тогда выражение (50) примет вид
![]()
![]() (51)
(51)
Обозначим отношение
![]()
где
![]()
показатель политропы.
показатель политропы.
Тогда
![]() (52)
(52)
Проинтегрируем выражение (52)
![]() (53)
(53)
или
![]() .
(54)
.
(54)
Таким образом, если логарифм некоторой функции величина постоянная, то и сама функция является постоянной величиной
![]() .
(55)
.
(55)
Выражение (55) представляет собой уравнение политропного процесса.
Выразим теплоемкость идеального газа в политропном процессе через известную изохорную теплоемкость.
Из выражения для показателя политропы
![]() и показателя
адиабаты
и показателя
адиабаты
![]() имеем
имеем
![]() (56)
(56)
С учетом выражения
(46) и уравнения состояния
![]() можно записать
можно записать
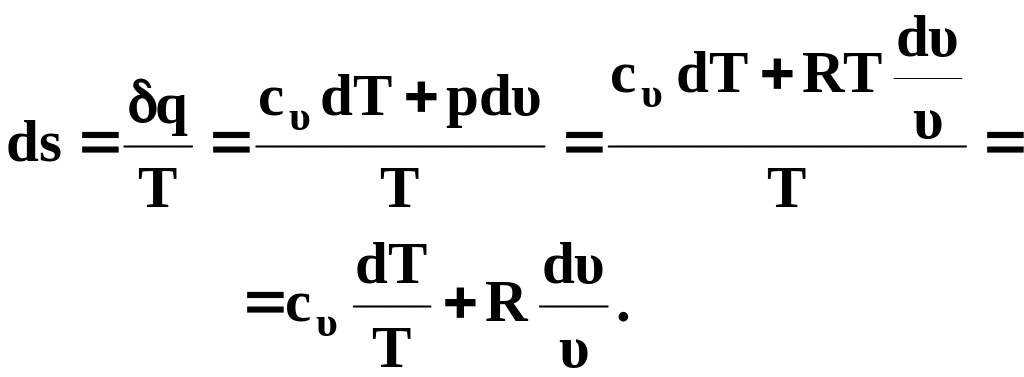 (57)
(57)
В интегральной форме первое начало термодинамики для политропного процесса будет иметь вид
(58)
или
![]() (59)
(59)
Из выражений (45) ─
(59) следует, что для политропного процесса
идеального газа
![]() :
:
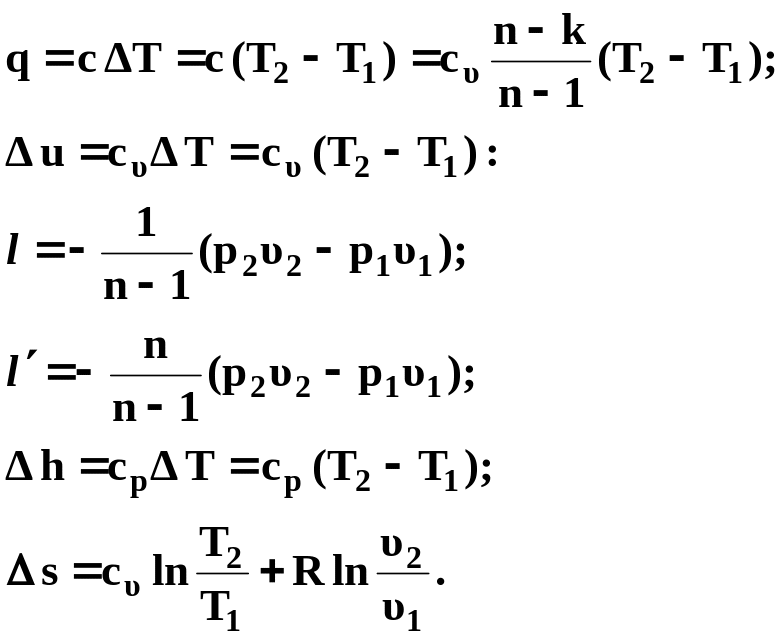 (60)
(60)
Показать политропы может меняться от 0 до .
Рассмотрим частные случаи:
1. при
![]() уравнение
политропного процесса
переходит в уравнение изобарного
процесса
уравнение
политропного процесса
переходит в уравнение изобарного
процесса
![]() ;
;
2. при
![]() уравнение политропного процесса
переходит в уравнение изотермического
процесса
уравнение политропного процесса
переходит в уравнение изотермического
процесса
![]() ;
;
3. при
![]() уравнение политропного процесса
переходит в уравнение адиабатного
процесса
уравнение политропного процесса
переходит в уравнение адиабатного
процесса
![]() .
.
4. при
![]() уравнение политропного процесса
переходит в уравнение изохорного
процесса
уравнение политропного процесса
переходит в уравнение изохорного
процесса
![]() .
.
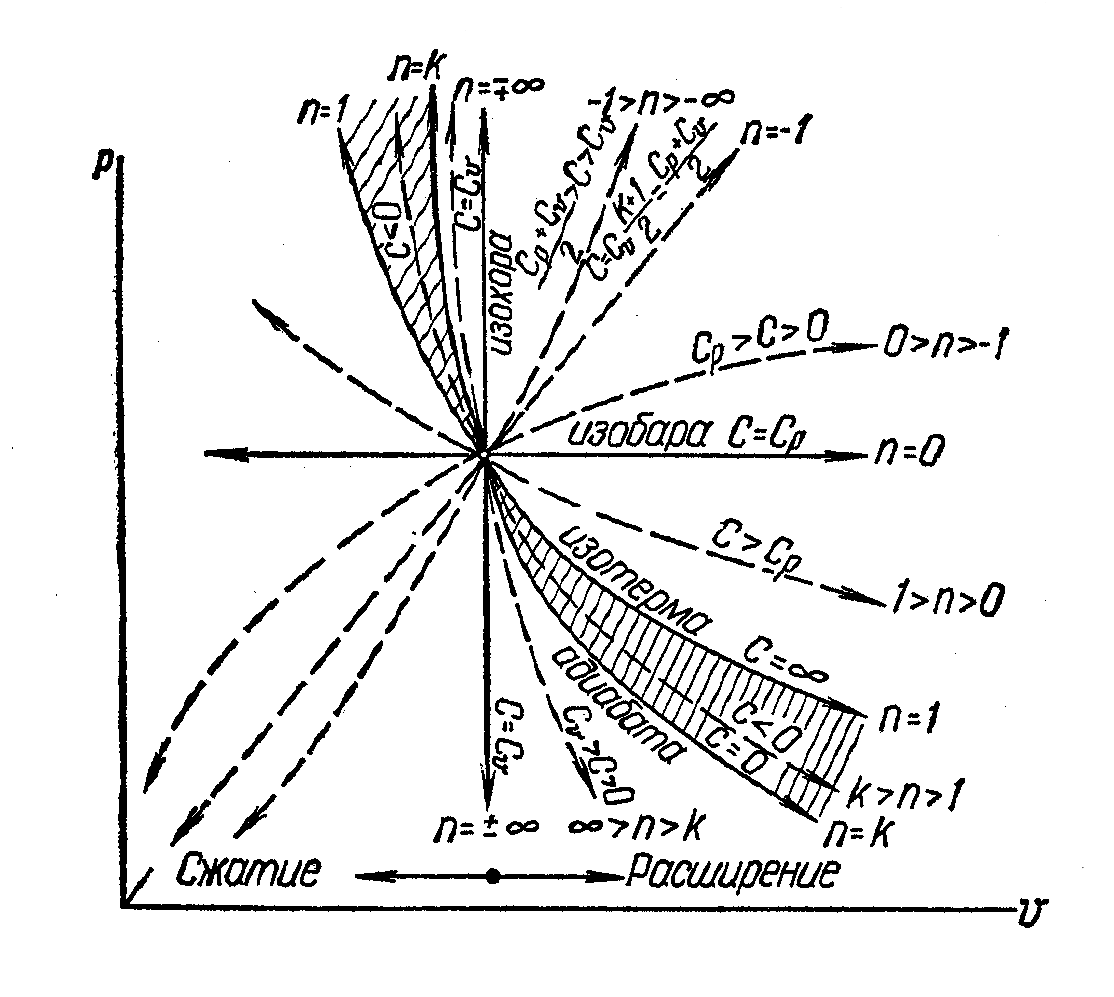
На рисунках 5 и 6 изображены все представленные термодинамические процессы в и ─ диаграммах.
Р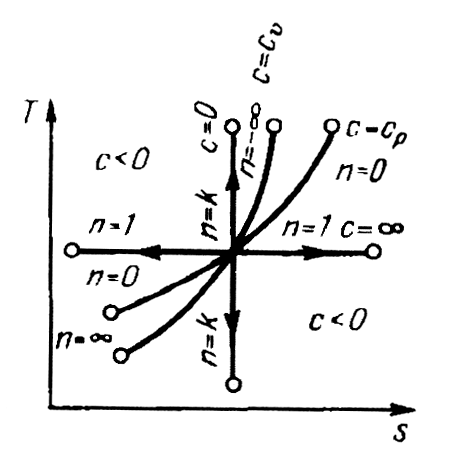 ис.
5 Изображение основных процессов в
-
диаграмме
ис.
5 Изображение основных процессов в
-
диаграмме
Рис. 6. Изображение основных термодинамических процессов
в - диаграмме
Все процессы начинаются в одной точке (в центре).
Изохора
![]() делит поле диаграммы на две области:
процессы, находящиеся правее изохоры,
характеризуются положительной работой,
так как сопровождаются расширением
рабочего тела; для процессов, расположенных
левее изохоры, характерна отрицательная
работа.
делит поле диаграммы на две области:
процессы, находящиеся правее изохоры,
характеризуются положительной работой,
так как сопровождаются расширением
рабочего тела; для процессов, расположенных
левее изохоры, характерна отрицательная
работа.
Процессы, расположенные правее и выше адиабаты, идут с подводом теплоты к рабочему телу; процессы, лежащие левее и ниже адиабаты, протекают с отводом теплоты.
Для процессов,
расположенных над изотермой
![]() ,
характерно увеличение внутренней
энергии газа; процессы, расположенные
под изотермой, сопровождаются уменьшением
внутренней энергии.
,
характерно увеличение внутренней
энергии газа; процессы, расположенные
под изотермой, сопровождаются уменьшением
внутренней энергии.
Процессы,
расположенные между адиабатой и
изотермой, имеют отрицательную
теплоемкость, так как
![]() и
и
![]() (а, следовательно, и
(а, следовательно, и
![]() ),
имеют в этой области противоположные
знаки. В таких процессах
),
имеют в этой области противоположные
знаки. В таких процессах
![]() ,
поэтому на производство работы при
расширении тратится не только подводимая
теплота, но и часть внутренней энергии
рабочего тела.
,
поэтому на производство работы при
расширении тратится не только подводимая
теплота, но и часть внутренней энергии
рабочего тела.
Рис. 5 Изображение основных процессов в - диаграмме
Рис. 6. Изображение основных термодинамических процессов в - диаграмме
