
- •Химические аспекты экологии
- •Глава 1. Химия атмосферы_____________________________ 6
- •Глава 2. Химия гидросферы____________________________ 38
- •Введение
- •Глава 1. Химия атмосферы
- •1.1. Физико-химические свойства атмосферы
- •1.2. Химические процессы в атмосфере
- •1.3. Меры по предотвращению загрязнения воздуха.
- •1.4. Источники информации, ключевые слова, вопросы для самоконтроля
Глава 1. Химия атмосферы
1.1. Физико-химические свойства атмосферы
Атмосфера – мощная газовая оболочка Земли, характеризующаяся резко выраженной неоднородностью строения и состава. Толщина атмосферы примерно 1000 км. Масса атмосферного воздуха – около 5∙1015 (пять квадратильонов) т; 90% этой массы сосредоточенно в самом нижнем слое атмосферы толщиной 17 км.
Условия в различных областях атмосферы, в том числе и силы земного притяжения, резко отличаются (особенно по вертикали), и это является одной из предпосылок расслоения атмосферы. Кроме того, атмосфера представляет собой реактор, в котором протекает множество химических и фотохимических реакций, сопровождающихся выделением и поглощением энергии, также способствующих формированию атмосферных слоев. С высотой меняется не только концентрация основных газовых компонентов, но и такие параметры, как Р, t.
Слоистая структура атмосферы сохраняется, несмотря на высокую скорость перемешивания воздушных масс. В горизонтальном направлении перемешивание осуществляется благодаря вращению Земли, по вертикали - преимущественно за счет сил конвекции. На рис. 1.1 показаны слои атмосферы. Более хорошо перемешиваемая часть атмосферы называется гомосферой. Выше находится гетеросфера, где перемешивание осуществляется только под действием гравитации.
В свою очередь гомосфера делится на тропосферу, стратосферу и мезосферу. Воздушные массы тропосферы нагреваются от поверхности Земли и, поднимаясь вверх, вызывают конвекционное перемешивание. Температура при этом понижается, достигая первого минимума на высоте 12 км. В этой области, называемой тропопаузой, она составляет примерно 215 К ( - 60° С). На высоте около 15-25 км температура начинает увеличиваться за счет поглощения ультрафиолетового излучения кислородом и озоном и протекания реакций озонового цикла. Повышение температуры препятствует проникновению в стратосферу холодных слоев из тропосферы. На высоте около 50 км температура достигает максимума приблизительно 275 К (стратопауза), затем снова начинает уменьшаться, т.к. меняется характер процессов и их энергетический эффект. Область второго температурного минимума (190 К) называется мезопаузой и находится на высоте около 80 км. Выше находится термосфера (или ионосфера), в которой кинетическая температура равномерно возрастает с высотой до 1000 - 1500 К. С высоты ~ 1000 км начинается экзосфера, переходящая в межпланетное пространство.
Характер изменения t в различных слоях атмосферы зависит от особенностей химического состава воздуха в этих слоях, хотя в целом состав
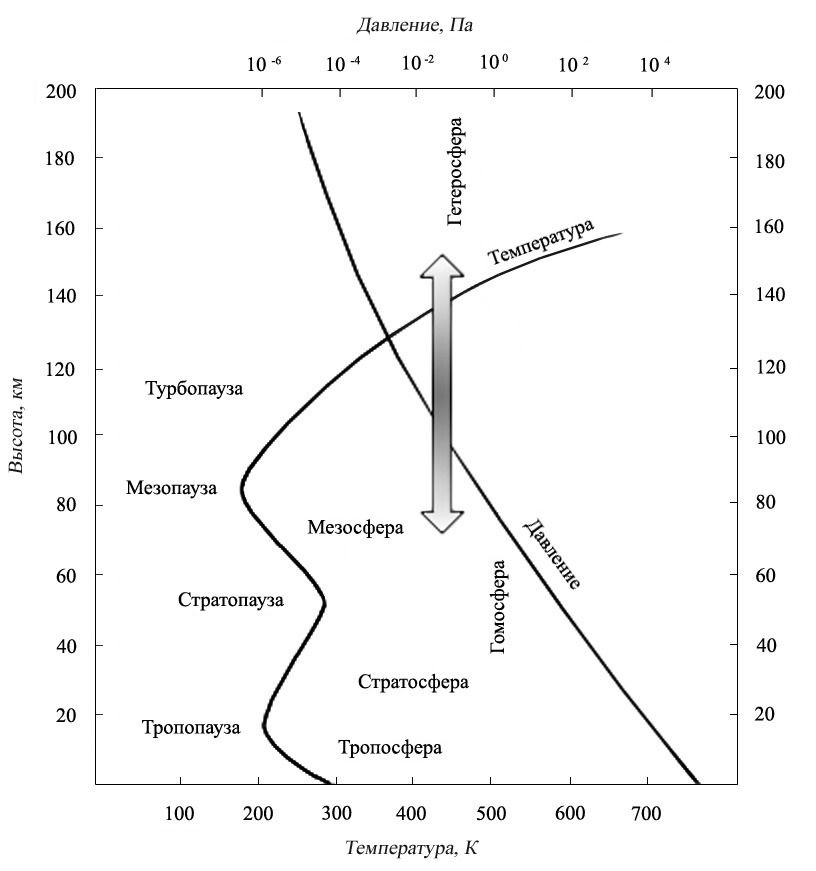
Рис. 1.1. Вертикальное строение атмосферы и соответствующие изменения температуры и давления. (Обратите внимание на логарифмический масштаб давления)
атмосферы почти одинаков вплоть до высоты 90 км. В табл. 1.1 приведены концентрации основных газов, составляющих средний фон, в среде которого происходят химические атмосферные процессы.
Можно выделить постоянные, переменные и случайные составляющие атмосферы. К первой группе относятся кислород, азот и инертные газы. Их содержание не зависит от места, где была взята проба воздуха.
Ко второй группе относятся углекислый газ и водяной пар. Так, концентрация воды в атмосфере сильно зависит от температуры. В тропических широтах она достигает 3%, тогда как в арктических уменьшается до 2∙10–3 %. Уменьшение концентрации водяных паров, равно как и диоксида углерода и других парниковых газов, а также аэрозольных частиц, является одной из причин снижения температуры в тропосфере.
Таблица 1.1. Валовой состав незагрязненного воздуха
Газ |
Концентрация |
Азот Кислород Аргон Вода Углекислый газ Неон Гелий Метан Криптон Водород Ксенон |
78,084% 20,946% 0,934% 0,5-0,4% 360 ppm * 18,18 ppm 5,24 ppm 1,7 ppm 1,14 ppm 0,5 ppm 0,087 ppm |
______________________
* ppm (partes pro million) – миллионная доля. Единица измерения относительной концентрации компонентов смеси, содержание которых очень мало. Концентрация в одну миллионную долю соответствует одной части (по объему) компонента на миллион частей смеси.
К третьей группе относятся компоненты, определяемые местными условиями. Это озон, диоксид серы, оксиды азота, монооксид углерода, углеводороды. Эти газы содержатся в незначительных количествах (в незагрязненном воздухе). Тем не менее их присутствие существенно влияет на состояние атмосферы. Многие из них обладают высокой реакционной способностью и вовлекаются в разнообразные химические реакции. По этой причине они представляют больший интерес для химиков, чем постоянные компоненты, точно так же как следовые количества в морской воде более важны, чем вода или NaCl. Следует помнить, что при этом содержание примесных газов в атмосфере регламентируется не константами химических равновесий, в которых может участвовать данный компонент, а такой характеристикой, как время пребывания в атмосфере.
Баланс между поступлением и выходом газа в атмосфере описывается с помощью уравнения:
Fвх = Fвых = A/τ, (1.1)
где Fвх, Fвых – это потоки в атмосферу и из нее; A – общее количество газа; τ –время его пребывания в атмосфере. В табл. 1.2 дано время пребывания некоторых газов в естественной атмосфере.
Из табл. 1.2 видно, что вещества с большим временем пребывания могут накапливаться в относительно высоких концентрациях по сравнению с теми, время пребывания которых меньше.
Таблица 1.2. Время пребывания следов газов в естественной атмосфере
Газ |
Время пребывания |
Концентрация,10–7% |
Диоксид углерода Оксид углерода Метан Азотистый ангидрид Оксид азота Диоксид азота Аммиак Диоксид серы Сероводород Сероуглерод Диметилсульфид Метилхлорид Серооксид углерода |
4 года 0,1 года 3,6 года 20-30 лет 4 дня 4 дня 2 дня 3-7 дней 1 день 40 дней 1 день 30 дней 1 год |
360000 100 1600 300 0,1 0,3 1 0,01-0,1 0,05 0,02 0,001 0,7 0,5 |
В такой смеси газов, как атмосфера, выполняется закон парциальных давлений Дальтона. Из него следует, что давление отдельных газов в атмосфере будет падать с той же скоростью, что и общее давление (см. рис. 1.1). Это можно представить в виде барометрического уравнения:
Pz = P0∙exp(-z/H), (1.2)
где Pz – давление на высоте z; P0 – давление на поверхности Земли и H – высота (около 8,4 км в нижней тропосфере), а также мера скорости, с которой падает давление с высотой. Из уравнения (1.2) видно, что давление падает по экспоненциальному закону. На высоте 5,8 км оно достигает 50% от своего значения на земной поверхности. Уравнению (1.2) отвечает около 90% всех атмосферных газов. Остальные находятся в верхних слоях атмосферы без перемешивания.
Так как состав атмосферы на высотах менее 90 км постоянен, средняя мо-лекулярная масса воздуха на этих высотах также практически не меняется и остается такой же, как и на уровне моря – 28,966. На высотах более 90 км она резко уменьшается (см. рис. 1.2). Изменение состава атмосферы в верхних слоях определяется двумя причинами: гравитационным эффектом и химичес-кими изменениями, связанными с поглощением электромагнитного излучения Солнца.
