
- •Вопросы по теме 4. Основы современных концепций микро - и наномира
- •3. Кратко сформулируйте, что такое атомная «орбиталь»? Какими формами характеризуют электронные орбитали, которые занимают определенное положение в пространстве (расположение в пространстве)?
- •4. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет главное квантовое число ?
- •5. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет орбитальное (побочное) квантовое число l?
- •14. Что характерно для атомных орбиталей металлов? Что характеризует энергия ионизации? Какие щелочные металлы обладают самыми малыми значениями энергии ионизации?
- •15. Что характерно для атомных орбиталей неметаллов? Что характеризует сродство к электрону? Какое вещество называют окислителем? Какие сильные окислители Вам известны?
- •16. Кратко опишите, что представляет в современном понимании такая сущность, как химическая связь. По какой причине образуется химическая связь между атомами водорода?
- •17. Кратко сформулируйте, какие бывают виды химической связи. Что такое ионная связь? Поясните, между какими атомами и как она образуется?
- •18. Кратко сформулируйте, какие бывают виды химической связи. Что такое ковалентная связь? Поясните, между какими атомами и как она образуется? Какие разновидности ковалентной связи Вам известны?
- •19. Кратко сформулируйте, что такое ковалентная связь? Поясните, как образуется σ - связь?
- •27. Кратко сформулируйте, какие бывают виды химической связи. Что такое молекулярная связь? Поясните, между какими атомами и как она образуется?
- •28. Какие разновидности молекулярного кислорода Вам известны? Как они различаются по химической активности?
- •32. На какие группы, по способности проводить ток, различаются кристаллические твердые тела? Что такое полупроводники и чем они характеризуются?
- •35. Что такое энергетическая диаграмма полупроводникового кристалла? Почему ее используют? Какими параметрами, на основании энергетической диаграммы, характеризуют полупроводниковые материалы?
- •36. Что такое энергетическая диаграмма полупроводникового кристалла? Почему ее используют? в чем различие энергетических диаграмм собственного и примесного полупроводников?
- •39. Поясните, что означает аллотропия веществ? Какие виды аллотропных форм углерода Вам известны? Чем характеризуется такая форма, как графит?
- •40. Поясните, что означает аллотропия веществ? Какие виды аллотропных форм углерода Вам известны? Чем характеризуется такая форма, как гексагональный алмаз (или лонсдейлит)?
- •43. Поясните, что означает аллотропия веществ? Чем характеризуется такая форма структур, как углеродные нанотрубки? Какими необычными физическими свойствами обладают нанотрубки?
- •44. Как меняются свойства объектов при уменьшении их наноразмеров? Что такое эффект лотоса? Как его можно использовать?
- •45. Кратко сформулируйте, почему человек стремится познать «тайны» наномира. Какие преимущества дает использование свойств наномира, и какие перспективы это открывает для нанотехнологий?
- •46. Кратко сформулируйте, почему человек стремится для решения проблемы энергопотребления использовать наномир и разрабатывать нанотехнологии.
- •48. Что представляет собой композиционный материал? Из каких двух основных компонент он состоит? Чего можно добиться комбинируя объемное содержание компонентов?
- •49. Какими свойствами, достоинствами и недостатками характеризуются современные композиционные материалы и в каких отраслях промышленности они находят применение?
- •50. Какие прогрессивные композитные материалы используют в автомобилестроении. В чем их достоинства и недостатки по сравнению с традиционными материалами, используемыми в автомобилях?
- •51. Какие прогрессивные композитные материалы используют в авиастроении. В чем их достоинства и недостатки по сравнению с традиционными материалами, используемыми в самолетах?
- •52. Какие преимущества получены в самолетах Boeing 787 Dreamliner, a350 xwb компании "Эрбас" за счет использования композиционных материалов?
3. Кратко сформулируйте, что такое атомная «орбиталь»? Какими формами характеризуют электронные орбитали, которые занимают определенное положение в пространстве (расположение в пространстве)?
Атомная орбиталь – Пространство вокруг ядра, в котором нахождение электрона наиболее вероятно (это пространство, которое включает в себя 90% электронного облака), называют орбиталью. С математической точки зрения орбиталь – это волновая функция, описывающая состояние электрона. Эта функция определяет форму поверхностей, ограничивающих пространство, в котором вероятность нахождения электрона составляет не менее 90%. С ее помощью можно рассчитать распределение электронной плотности в заданном пространстве. В этом случае «формы» орбиталей представляют собой графики функций, изображающие области математического пространства, где нахождение электрона в данной орбитали наиболее вероятно.
Электронные орбитали имеют разные размеры и форму, определенным образом расположены в пространстве (орбитали занимают определенное положение в пространстве). Размеры электронной орбитали определяются расстоянием, на котором электрон находится от ядра. При этом электроны находятся не на любых, а вполне определенных расстояниях от ядра. Электроны, которые находятся на одинаковом расстоянии от ядра, образуют один электронный слой. Электронные слои могут характеризоваться любыми целыми положительными значениями, начиная с единицы (n = 1,2,3, … ∞) или обозначаться латинскими буквами K, L, M, N, O, P, Q. Электронные орбитали имеют различную форму: сферы, гантели и др.
4. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет главное квантовое число ?
Четыре
параметра: 1. Главное
квантовое число
;
2. Орбитальное (побочное) квантовое
число l;
3. Магнитное
квантовое число
![]() ;
4. Спиновое квантовое число
;
4. Спиновое квантовое число
![]() .
.
Главное квантовое число
соответствует порядковому номеру
электронного слоя и характеризует
величину энергии электрона;
может принимать значения 1, 2, 3, 4, 5 , 6, 7.
Значения
соотносятся с обозначением атомных
электронных слоев. Электроны с
![]() образуют ближайший к ядру атома
электронный слой (энергетический
уровень). Электроны с
образуют ближайший к ядру атома
электронный слой (энергетический
уровень). Электроны с
![]() образуют второй от атома электронный
слой и т. д.
образуют второй от атома электронный
слой и т. д.
Значение |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
Обозначение электронного слоя |
K |
L |
M |
N |
O |
P |
Q |
5. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет орбитальное (побочное) квантовое число l?
Четыре параметра: 1. Главное квантовое число ; 2. Орбитальное (побочное) квантовое число l; 3. Магнитное квантовое число ; 4. Спиновое квантовое число .
Орбитальное
(побочное) квантовое число l
характеризует форму электронной орбитали
(и, соответственно, энергетические
подуровни) при заданном значении главного
квантового числа
.
Орбитальное число l
может принимать значения целых чисел
от 0 до
![]() .
Состояния электрона, которые
характеризуются различными значениями
числа l,
называют энергетическими подуровнями.
Орбитальное квантовое число определяет
также момент
импульса
электрона. Момент
импульса
при этом задаётся соотношением
.
Состояния электрона, которые
характеризуются различными значениями
числа l,
называют энергетическими подуровнями.
Орбитальное квантовое число определяет
также момент
импульса
электрона. Момент
импульса
при этом задаётся соотношением
![]() .
В одной и той же оболочке (уровне) энергия
подоболочек (подуровней) возрастает.
Орбитали с разным значением числа l
обозначаются
буквами s, p, d, f
.
В одной и той же оболочке (уровне) энергия
подоболочек (подуровней) возрастает.
Орбитали с разным значением числа l
обозначаются
буквами s, p, d, f
Значение числа l |
0 |
1 |
2 |
3 |
Обозначение орбитали |
s |
p |
d |
f |
6. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет магнитное квантовое число ?
Четыре параметра: 1. Главное квантовое число ; 2. Орбитальное (побочное) квантовое число l; 3. Магнитное квантовое число ; 4. Спиновое квантовое число .
Магнитное
квантовое число
характеризует ориентацию орбитали в
пространстве и может принимать значения
целых чисел от –![]() до +
,
в том числе и значение 0 (ml
= -l
… 0 … l).
до +
,
в том числе и значение 0 (ml
= -l
… 0 … l).
7. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Поясните, что определяет спиновое квантовое число ?
Четыре параметра: 1. Главное квантовое число ; 2. Орбитальное (побочное) квантовое число l; 3. Магнитное квантовое число ; 4. Спиновое квантовое число .
Спиновое
квантовое число
характеризует различие состояний двух
электронов, принадлежащих одной орбитали,
в зависимости от ориентировки их
собственных моментов количеств движения.
Число
может иметь только два значения:
![]() .
То есть, магнитное состояние квантуется,
и существуют только два возможных
состояния.
.
То есть, магнитное состояние квантуется,
и существуют только два возможных
состояния.
9. Какие 4 параметра используют в современной квантовой теории для полного описания состояния электрона в атоме? Какой вид будет иметь график общей энергии электрона на данной орбитали в зависимости от главного квантового числа n ? О чем свидетельствует данный график?
Четыре параметра: 1. Главное квантовое число ; 2. Орбитальное (побочное) квантовое число l; 3. Магнитное квантовое число ; 4. Спиновое квантовое число .
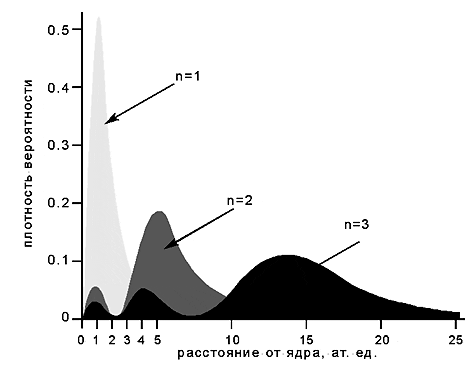
График распределения плотности вероятности в зависимости от числа и от расстояния от ядра. Свидетельствует о том, что характерный размер атома при увеличении числа быстро растет. При этом электронное облако по мере возбуждения атома (увеличении числа ) как бы выталкивается к периферии (уходит подальше от ядра). Иначе говоря, чем прочнее электрон связан с ядром, тем меньше должно быть электронное облако по размерам и более плотным по распределению заряда.
10. Орбитальное квантовое число определяет форму поверхности максимальной вероятности нахождения электрона и ее симметрию. Какую форму имеют s-орбитали (l = 0) и d-орбитали (l = 2) ?
Все s-орбитали (l = 0) сферические. d-орбитали (l = 2) – четырехлепестковой розы.

11. Орбитальное квантовое число определяет форму поверхности максимальной вероятности нахождения электрона и ее симметрию. Какую форму имеют s-орбитали (l = 0) и р-орбитали (l = 1)?
Все s-орбитали (l = 0) сферические. P-орбитали (l = 1) имеют форму гантели
12. Объясните, за счет чего происходит переход электрона с орбитали с на орбиталь, с номером большим единицы? Может ли осуществиться обратный переход? По каким причинам осуществляется обратный переход и что при этом происходит? Как они связаны между собой энергия в джоулях и в электрон-вольтах?
Это соответствует так называемому основному состоянию атома, то есть такому состоянию, когда он не подвергается никаким внешним воздействиям. Остальные уровни энергии называются возбужденными. Возбуждение атома, то есть «переход» электрона в состояние, которое характеризуется большим квантовым числом (переход на орбиталь с большим радиусом), требует сообщения ему дополнительной энергии и, следовательно, происходит в результате каких-либо внешних воздействий (к примеру, за счет теплового воздействия). Состояние 1s – основное. В этом состоянии атом имеет минимальную энергию. Чтобы перевести атом в одно из возбужденных состояний, ему надо сообщить энергию. Это можно осуществить за счет теплового удара (соударения с другим атомом в нагретом газе), за счет электронного удара (например, в электрическом разряде) или за счет поглощения атомом фотона.
Характерное время жизни атома в возбужденном состоянии составляет 10-8 с. Далее происходит спонтанный переход в одно из нижележащих состояний. Переход атома из состояния 2 в состояние 1 будет сопровождаться излучением кванта с энергией hν = W2 - W1, где W2 и W1 - энергии соответствующих состояний.
Электрон может возвращаться на основную
орбиталь не единым переходом, а через
промежуточные уровни. В этом случае при
переходе будут излучаться несколько
фотонов с энергиями![]() и
и
![]() ,
равными разности энергий этих уровней.
,
равными разности энергий этих уровней.
Поскольку, говоря об атомах, приходится иметь дело именно с такими энергиями, то уступая естественному человеческому желанию пользоваться числами в пределах от 0,1 до 100, часто отказываются от использования единиц энергии, установленных системой СИ. Вместо джоулей используют электрон-вольт – единицу, численно равную энергии, которую приобретает электрон под действием разности потенциалов 1 В (вольт). То есть используют 1 эВ=1,6х10-19 Дж.
13. Солнце является источником ультрафиолетового излучения (УФЛ). Какая разновидность УФЛ полезна, а какая вредна? Кратко поясните, почему уменьшение или исчезновение озона (образование озоновой «дыры») в стратосфере создает серьезную угрозу жизни на Земле?
УФ- излучение делится на ближнее, или
флуоресцентное, от 380 до 200 нм, и дальнее,
или вакуумное, от 200 до 10 нм. Органами
чувств человек его не воспринимает, но
на коже ближний ультрафиолет вызывает
появление загара. Это защитная реакция
кожи на определенные химические нарушения
под действием ультрафиолета. Чем короче
длина волны![]() ,
тем большие нарушения может вызывать
ультрафиолетовое излучение в биологических
молекулах. УФ-излучение оказывает
сильное биологическое воздействие на
живые организмы, которое может быть
полезным или вредным. Поэтому оно имеет
большое значение для жизни растений,
животных и людей. В ткани организма УФ-
излучение проникает очень неглубоко –
на 0,1- 1 мм, но при этом вызывает очень
сложную биологическую реакцию, которая
проявляется на месте действия излучения
эритемой. Эритемой называется интенсивное
покраснение кожи, которое проявляется
через 6-12 часов после действия излучения,
удерживается в течение нескольких дней
и оставляет на длительное время светло
коричневую пигментацию кожи, называемую
загаром.
,
тем большие нарушения может вызывать
ультрафиолетовое излучение в биологических
молекулах. УФ-излучение оказывает
сильное биологическое воздействие на
живые организмы, которое может быть
полезным или вредным. Поэтому оно имеет
большое значение для жизни растений,
животных и людей. В ткани организма УФ-
излучение проникает очень неглубоко –
на 0,1- 1 мм, но при этом вызывает очень
сложную биологическую реакцию, которая
проявляется на месте действия излучения
эритемой. Эритемой называется интенсивное
покраснение кожи, которое проявляется
через 6-12 часов после действия излучения,
удерживается в течение нескольких дней
и оставляет на длительное время светло
коричневую пигментацию кожи, называемую
загаром.
Озон
![]() существенно уменьшает поток квантов,
попадающий на земную поверхность.
Структура орбиталей и собственных
дискретных наборов (уровней) энергии
озона такова, что стратосферный озон
поглощает кванты, которые составляют
часть оптического излучения Солнца с
длинами волн менее 285 нм, и, кроме того,
значительно ослабляет поток излучения
в диапазоне 285 – 315 нм. Тем самым озоновая
оболочка предохраняет поверхность
Земли от так называемого жесткого
ультрафиолетового излучения Солнца,
которое разлагает хроматин клеточного
ядра, прекращает деление и размножение
клеток, оказывает бактерицидное (то
есть убивающее бактерии) действие. У
людей такое ультрафиолетовое излучение
повреждает ДНК, нарушает генетический
код и может привести к трагическим
последствиям. Эффект поражения наиболее
силен при действии оптического излучения
с длинами волн 255-265 нм и существенно
убывает после 290 нм. Иначе говоря, озон,
пропуская оптическое излучение с
длинами волн больше 290 нм, «задерживает»
опасное оптическое излучение.Таким
образом, уменьшение или исчезновение
озона в стратосфере создает серьезную
угрозу для регулирования потока
ультрафиолетовых квантов, задерживая
наиболее опасные из них. Проблема эта
настолько серьезная, что для ее решения
потребовалось принятие на международном
уровне политических соглашений,
непосредственно затрагивающих
экономические и жизненные интересы
многих миллионов людей.
существенно уменьшает поток квантов,
попадающий на земную поверхность.
Структура орбиталей и собственных
дискретных наборов (уровней) энергии
озона такова, что стратосферный озон
поглощает кванты, которые составляют
часть оптического излучения Солнца с
длинами волн менее 285 нм, и, кроме того,
значительно ослабляет поток излучения
в диапазоне 285 – 315 нм. Тем самым озоновая
оболочка предохраняет поверхность
Земли от так называемого жесткого
ультрафиолетового излучения Солнца,
которое разлагает хроматин клеточного
ядра, прекращает деление и размножение
клеток, оказывает бактерицидное (то
есть убивающее бактерии) действие. У
людей такое ультрафиолетовое излучение
повреждает ДНК, нарушает генетический
код и может привести к трагическим
последствиям. Эффект поражения наиболее
силен при действии оптического излучения
с длинами волн 255-265 нм и существенно
убывает после 290 нм. Иначе говоря, озон,
пропуская оптическое излучение с
длинами волн больше 290 нм, «задерживает»
опасное оптическое излучение.Таким
образом, уменьшение или исчезновение
озона в стратосфере создает серьезную
угрозу для регулирования потока
ультрафиолетовых квантов, задерживая
наиболее опасные из них. Проблема эта
настолько серьезная, что для ее решения
потребовалось принятие на международном
уровне политических соглашений,
непосредственно затрагивающих
экономические и жизненные интересы
многих миллионов людей.
