
- •2.5. Декарбоксилирование и трансаминирование, биологическое значение. Диагностическое значение определения активности трансаминаз.
- •2.6. Дезаминирование окислительное и непрямое аминокислот.
- •2. Непрямое дезаминирование – это процесс дезаминирования путем трансаминирования.
- •2.1. Образование аммиака в организме и пути его обезвреживания. Гипераммониемия.
- •2.2. . Биосинтез мочевины как основной механизм предотвращения накопления аммиака. Клиническое значение определения мочевины.
- •2.3. Синтез креатина, креатин-фосфата, значение этого синтеза для организма. Клиническое значение определения креатинина.
- •2.4. Особенности обмена отдельных аминокислот (глицин, метионин, глутаминовая и аспарагиновая кислоты, триптофан, фенилаланин).
- •2.5. Нарушения в обмене отдельных аминокислот.
- •2.6. Патология азотистого обмена.
2.6. Дезаминирование окислительное и непрямое аминокислот.
Дезаминирование – процесс потери аминокислотой аминогруппы. В организме подвергается этому процессу только глутаминовая кислота, т.к. в организме активен фермент глутаматдегидрогеназа (ГДГ). Фермент ГДГ активен в митохондриях клеток всех органов, кроме мышечной ткани.
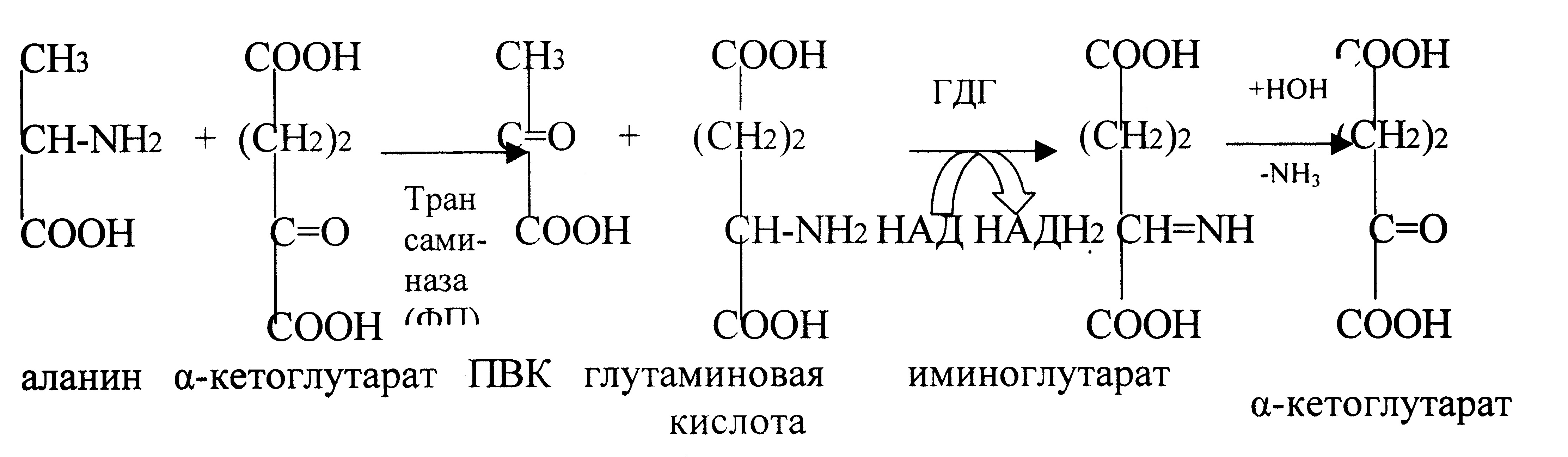
1. Окислительное дезаминирование.
 NН
NН
СООН – СН2 – СН2 – С – СООН
Н

 ООС–СН2-
СН2
- СН – СООН
ООС–СН2-
СН2
- СН – СООН
 NН2
NН2
О
ГДГ +НОН СООН-СН2-СН2-С-СООН
г

 лутаминовая
кислота иминоглутарат
NН3
+ -
лутаминовая
кислота иминоглутарат
NН3
+ -
α-кетоглутаровая кислота
 НАД
НАД
НАДН2
Остальные аминокислоты подвергаются непрямому дезаминированию.
2. Непрямое дезаминирование – это процесс дезаминирования путем трансаминирования.
2.1. Образование аммиака в организме и пути его обезвреживания. Гипераммониемия.
Аммиак в организме образуется в результате дезаминирования аминокислот, биогенных аминов и нуклеотидов. Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (гниение). Концентрация аммиака в крови в норме – 0,4-0,7мг/л. Это токсичное соединение, поэтому аммиак не накапливается, а вступает в реакцию с глутаминовой или аспарагиновой кислотами с образованием индифферентной транспортной формы – глутамина или аспарагина.
+NН3
Н ООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН
ООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН
NН2 АТФ NН2
-Н 2О
глутаминовая кислота глутамин
+NН3
 НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
АТФ
NН2 -Н 2О
NН2
аспарагиновая кислота аспарагин
В почках глутамин под влиянием глутаминазы расщепляется с образованием аммиака, идущего на нейтрализацию кислых соединений с образованием аммонийных солей. Этот процесс является одним из механизмов регуляции кислотно-щелочного равновесия в организме и сохранения важнейших катионов (Na+, K+) для поддержания осмотического давления. Глутамин – основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров, белков, глюкозы. Также источниками образования аммиака служат процессы:
дезаминирования биогенных аминов;
распад пиримидиновых оснований (урацил, тимин, цитозин);
дезаминирования аминокислот;
дезаминирования пуриновых оснований (гуанина и аденина).
Пути использования аммиака в организме:
Синтез аминокислот из соответствующих кетокислот:
АТФ
 СН3-С-СООН
+ NН3
СН3-СН-СООН
СН3-С-СООН
+ NН3
СН3-СН-СООН
О NН2
ПВК аланин
Синтез аммонийных солей в почках.
Синтез пуриновых и пиримидиновых нуклеотидов.
Синтез мочевины – основной путь обезвреживания аммиака.
ГИПЕРАММОНИЕМИЯ.
Повышение содержания аммиака в крови до 6000мкмоль/л (норма-60мкмоль/л) оказывает токсическое действие на организм.
Причины:
генетический дефект ферментов орнитинового цикла в печени;
вторичное поражение печени в результате цирроза, гепатита и др.
Симптомы: тошнота, повторяющаяся рвота, потеря сознания, отек мозга, отставание умственного развития. Все симптомы гипераммониемии – проявление действия аммиака на ЦНС.
Для диагностики производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активность ферментов печени.
