
- •Введение
- •Семестровая работа 1
- •Глава I. Механика § 1. Кинематика
- •§ 2. Динамика материальной точки и твердого тела
- •§ 3. Законы сохранения
- •§ 4. Элементы специальной теории относительности
- •§ 5. Элементы механики сплошных сpeд
- •§ 6. Гармонические колебания
- •§ 7. Волновые процессы
- •Глава II. Молекулярная физика и термодинамика § 8. Статистическая физика и термодинамика
- •§ 9. Молекулярно- кинетическая теория
- •§ 10. Статистические распределения
- •§ 11. Основы термодинамики
- •§ 12. Явления переноса
- •§ 13. Реальные газы
- •Семестровая работа 2
- •Глава III. Электричество и магнетизм § 14. Электростатика
- •§ 15. Свойства электростатических полей
- •§ 16. Проводники в электрическоМ поле
- •§ 17. Энергия взаимодействия электрических зарядов
- •§ 18. Постоянный электрический ток
- •§ 19. Магнитное поле
- •§ 20. Явление электромагнитной индукции
- •§ 21. Электромагнитные колебания
- •Cеместровая работа 3
- •Глава IV. Оптика § 22. Понятие о геометрической оптике
- •§ 23. Свойства световых волн
- •§ 24. Дифракция волн
- •§ 25. Электромагнитные волны в веществе
- •Глава V. Квантовая физика § 26. Тепловое излучение
- •§ 27. Экспериментальное обоснование основных идей квантовой теории
- •§ 28. Корпускулярно—волновой дуализм
- •§ 29. Уравнение Шредингера.
- •§ 30. Конденсированное состояние
- •§ 31. Атом и Молекула водорода в квантовой теории
- •Глава VI. Физика атомного ядра § 32. Атомное ядро
- •Приложения
- •Некоторые астрономические величины
- •Рекомендуемая литература
- •Содержание
- •2. Получить то же самое для точек оси отверстия, в которых наблюдаются минимумы интенсивности. 74
§ 13. Реальные газы
Эффективный диаметр молекул. Силы межмолекулярного взаимодействия. Уравнение Ван-дер-Ваальса. Изотермы Ван-дер-Ваальса. Фазовые переходы первого и второго рода. Фазовые равновесия и фазовые превращения. Уравнение Клайперона-Клаузиуса. Критическая точка. Метастабильные состояния, тройная точка.
Основные формулы
Уравнение состояния реальных газов (уравнение Ван-дер-Ваальса) для моля газа
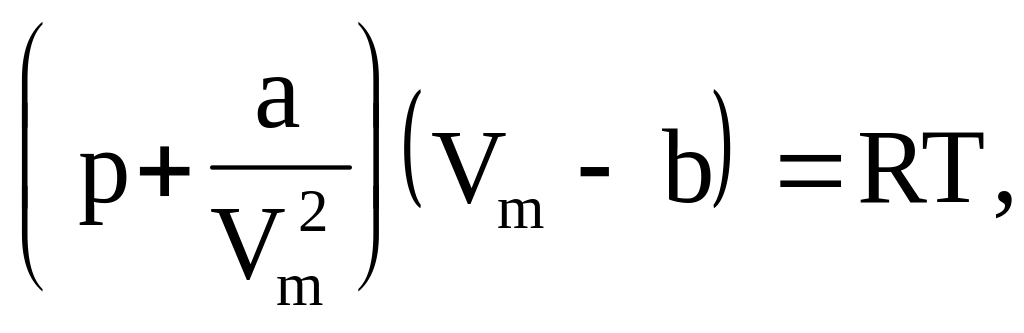
где Vm
- молярный объем:
![]() и b - постоянные
Ван-дер-Ваальса, различные для разных
газов.
и b - постоянные
Ван-дер-Ваальса, различные для разных
газов.
Уравнение Ван-дер-Ваальса для произвольной массы газа
(р +
2![]()
b) = RT,
b) = RT,
где
=
![]() - количество вещества.
- количество вещества.
Внутреннее давление, обусловленное силами межмолекулярного взаимодействия
![]() .
.
Связь
постоянных
![]() и b
данного газа с его критическими
параметрами
и b
данного газа с его критическими
параметрами
Vk
= 3b, рk
=![]() ; Тk
=
; Тk
=
![]() .
.
Решение этих уравнений относительно постоянных а и b
![]()
После введения приведенных величин
![]()
![]() ,
,
уравнение Ван-дер-Ваальса принимает вид
![]() .
.
Внутренняя энергия моля реального газа
![]() ,
,
где CV - молярная теплоемкость газа при постоянном объеме.
Семестровые задания
13.1. Какую температуру имеют 2 г азота, занимающего объем 820 см3 при давлении 0,2МПа? Газ рассматривать как реальный.
13.2. Какую температуру имеют 3,5 г кислорода, занимающего объем 90 см3, при давлении 2,8 МПа? Газ рассматривать как реальный.
13.3. 10 г гелия занимают объем 100 см3 при давлении 100 МПа. Найти темпе-ратуру газа, рассматривая его как реальный.
13.4. 1кмоль углекислого газа занимает объем V = 1м3при температуре 1000С. Найти давление газа, считая его реальным.
13.5. Углекислый газ массой 1 кг находится при температуре 290 К в сосуде вместимостью 20 л. Определить давление газа, если газ реальный. а =
=0,365 Н·м4/мол2 ; b = 4,3·10-5 м3/моль.
13.6. Определить постоянные а и b некоторого газа, если критические температура и давление соответственно равны 100К и 2 МПа.
13.7. Вычислить критическую температуру ТКР и давление рКР для азота.
13.8. Определить во сколько раз давление газа больше его критического давления, если известно, что его объем и температура вдвое больше критических значений этих параметров.
13.9. Вычислить молярный критический объем Vмкр кислорода, если его критическая температура ТКР.= 155 К, а его давление рКР .= 5,08 МПа.
13.10.Толстостенный стальной баллон частично заполняют водой. После этого баллон герметически закупоривают и нагревают. Определить, какую часть внутреннего объема баллона должна занимать вода, чтобы можно было наблюдать при нагревании переход вещества через критическую точку.
Семестровая работа 2
Таблица 2
|
Варианты |
|||||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Номера задач |
14.1 |
14.2 |
14.3 |
14.4 |
14.5 |
14.6 |
14.7 |
14.8 |
14.9 |
14.10 |
14.11 |
14.12 |
14.13 |
14.14 |
14.15 |
14.16 |
14.17 |
14.18 |
14.19 |
14.20 |
|
15.1 |
15.2 |
15.3 |
15.4 |
15.5 |
15.6 |
15.7 |
15.8 |
15.9 |
15.10 |
|
16.1 |
16.2 |
16.3 |
16.4 |
16.5 |
16.6 |
16.7 |
16.8 |
16.9 |
16.10 |
|
16.11 |
16.12 |
16.13 |
16.14 |
16.15 |
16.16 |
16.17 |
16.18 |
16.19 |
16.20 |
|
17.1 |
17.2 |
17.3 |
17.4 |
17.5 |
17.6 |
17.7 |
17.8 |
17.9 |
17.10 |
|
18.1 |
18.2 |
18.3 |
18.4 |
18.5 |
18.6 |
18.7 |
18.8 |
18.9 |
18.10 |
|
18.11 |
18.12 |
18.13 |
18.14 |
18.15 |
18.16 |
18.17 |
18.18 |
18.19 |
18.20 |
|
18.21 |
18.22 |
18.23 |
18.24 |
18.25 |
18.26 |
18.27 |
18.28 |
18.29 |
18.30 |
|
18.31 |
18.32 |
18.33 |
18.34 |
18.35 |
18.36 |
18.37 |
18.38 |
18.39 |
18.40 |
|
19.1 |
19.2 |
19.3 |
19.4 |
19.5 |
19.6 |
19.7 |
19.8 |
19.9 |
19.10 |
|
19.11 |
19.12 |
19.13 |
19.14 |
19.15 |
19.16 |
19.17 |
19.18 |
19.19 |
19.20 |
|
19.21 |
19.22 |
19.23 |
19.24 |
19.25 |
19.26 |
19.27 |
19.28 |
19.29 |
19.30 |
|
19.31 |
19.32 |
19.33 |
19.34 |
19.35 |
19.36 |
19.37 |
19.38 |
19.39 |
19.40 |
|
20.1 |
20.2 |
20.3 |
20.4 |
20.5 |
20.6 |
20.7 |
20.8 |
20.9 |
20.10 |
|
20.11 |
20.12 |
20.13 |
20.14 |
20.15 |
20.16 |
20.17 |
20.18 |
20.19 |
20.20 |
|
21.1 |
21.2 |
21.3 |
21.4 |
21.5 |
21.6 |
21.7 |
21.8 |
21.9 |
21.10 |
|
21.11 |
21.12 |
21.13 |
21.14 |
21.15 |
21.16 |
21.17 |
21.18 |
21.19 |
21.20 |
|
21.21 |
21.22 |
21.23 |
21.24 |
21.25 |
21.26 |
21.27 |
21.28 |
21.29 |
21.30 |
|
21.31 |
21.32 |
21.33 |
21.34 |
21.35 |
21.36 |
21.37 |
21.38 |
21.39 |
21.40 |
|
