
- •«Медицинская химия» для студентов медицинских факультетов
- •Сдвиг рН крови в кислую сторону;
- •Нет однозначного ответа
- •Приготовленный из стандартного вещества;
- •Нет однозначного ответа
- •Гипертонический раствор
- •Нет однозначного ответа
- •Гемолиз;
- •0,1 Моль/л;
- •Аммиачный буфер
- •Нужны дополнительные сведения
- •Нет однозначного ответа
- •Марганец.
- •Натрий.
- •Кальций.
- •Хлорид натрия;
- •Нет ответа
- •Нет ответа
- •Нет ответа
- •Нужны дополнительные сведения
- •Нет ответа
- •Нет ответа;
- •Нужны дополнительные сведения
- •Нет ответа;



Нужны дополнительные сведения
Нет однозначного ответа
Укажите интервал рН для случая «повышенная кислотность» желудочного сока:
1,0 –1, 5;
3 - 6;
6 – 6,5;
1,5 – 2,0;
2 - 4.
Чему равно осмотическое давление крови в норме?
700-800 кПа
600-700 кПа
500-600 кПа
800-900 кПа
900-950 кПа
Указать значение рН для случая «нулевой кислотности» желудочного сока:
6,0
4,0
2,0
8,0
10,0
Какой раствор надо добавить к воде, чтобы увеличить рН?
едкий калий;
азотную кислоту;
аммоний ацетат;
хлорид натрия
соляную кислоту
Какой способ выражения концентраций используется для расчета осмотического давления?
Молярная концентрация
Процентная концентрация
Моляльная концентрация
Мольная доля
Молярная концентрация эквивалента
Наибольшее значение буферной емкости крови обеспечивает:
Гемоглобиновый + Гидрокарбонатный буферы;
Гемоглобиновый буфер;
Ацетатный буфер + Гидрокарбонатный буфер
Фосфатный буфер;
Гидрокарбонатный буфер.
Растворимость газов в жидкостях с повышением температуры:
уменьшается;
увеличивается;
не изменяется
нет однозначного ответа
нужны дополнительные сведения
В каких единицах измеряется титр раствора?
г/мл;
кг;
г;
кг\л;
кг\дм3.
Изоэлектрическая точка белка, содержащего равные количества - NН2 и - СООН групп, соответствует:
рН = 7;
рН 7;
рН 7;
рН = 8;
рН = 5.
Гемолиз происходит вследствие:
Движения молекул воды из клетки
Движения внутриклеточных ионов из клетки
Движения воды в клетку
Движения внеклеточных ионов в клетку
Двустороннего движения молекул воды
Как рассчитать рН в растворе соляной кислоты?
рН = -lgCк-ты
pH = 14 – lgCк-ты
рН = -lgCк-ты
рН = lgCк-ты
формулы не существует
Что происходит с эритроцитом при помещении его в 0,2% раствор NаСl ?
Гемолиз;
Ничего не происходит;
Плазмолиз;
Нельзя дать ответ;
Нужны дополнительные сведения
Плазмолиз происходит при помещении эритроцита в:
Гипертонический раствор
Гипотонический раствор
Изотонический раствор
5%-ный раствор глюкозы
0,9 %-ный раствор хлорида натрия
Растворимость газов при повышении давления:
Растет
Падает
Не изменяется
Растет, а затем падает
Падает, а затем растет
Выберите раствор, изотоничный крови:
0,9%-ный раствор хлорида натрия
5%-ный раствор хлорида натрия
0,5%-ный раствор хлорида натрия
9%-ный раствор хлорида натрия
Дистиллированная вода
Выберите раствор, гипертоничный относительно крови:
5%-ный раствор хлорида натрия
0,5%-ный раствор хлорида натрия
0,9%-ный раствор хлорида натрия
0,2%-ный раствор хлорида натрия
Дистиллированная вода
Какую массу гидроксида натрия нужно взять для нейтрализации 36,5 г соляной кислоты?
40г
36,5г
80г
71г
4г
Если рН крови 7,5, какой препарат нужно ввести больному для коррекции кислотно-основного равновесия крови?
5%-ный раствор аскорбиновой кислоты
5%-ный раствор питьевой соды
Изотоничный раствор хлорида натрия
Изотоничный раствор глюкозы
Гипертоничный раствор глюкозы
Если рН крови 7,29, какой препарат нужно ввести больному для коррекции кислотно-основного равновесия крови?
4%-ный раствор питьевой соды
5%-ный раствор аскорбиновой кислоты
Изотоничный раствор хлорида натрия
Изотоничный раствор глюкозы
Гипертоничный раствор глюкозы
Укажите состояние алкалоза:
рН=7,55
рН=7,35
рН=7.45
рН=7,25
рН=7,15
Укажите состояние ацидоза:
рН=7,25
рН=7,55
рН=7,35
рН=7.45
рН=7,65
Какие растворы называются гипотоническими по отношению к крови?
Растворы с меньшим осмотическим давлением, чем крови в норме
Растворы с большим осмотическим давлением, чем крови в норме
Растворы с равными осмотическими давлениями
Растворы, содержащие одно и то же растворенное вещество
Растворы, имеющие одинаковые процентные концентрации разных растворенных веществ
Какие растворы называются гипертоническими по отношению к крови?
Растворы с большим осмотическим давлением, чем крови в норме
Растворы с меньшим осмотическим давлением, чем крови в норме
Растворы с равными осмотическими давлениями
Растворы, содержащие одно и то же растворенное вещество
Растворы, имеющие одинаковые процентные концентрации разных растворенных веществ
Выберите из приведеных систем фосфатную буферную систему организма:
NaH2PO4 + Na2HPO4.
NH4OH + NH4Cl;
H3BO3 + NaOH
KH2PO4 + NaOH;
CH3COOH + CH3COONa
В растворе какого вещества рН меньше?
Н2SO4
HCl
CH3COONa
Na2CO3
NaOH
В состав молекулы гемоглобина в качестве комплексообразователя входит:
Fe2+
Fe3+
Co2+
Co3+
Zn2+
Если активная кислотность желудочного сока составляет 20-40 титриметрических единиц, какое значение рН может соответствовать этому состоянию?
рН= 1,5 – 3,0;
рН= 1,0-1,5
рН= 3,0-4,0
рН= 4,0-5,0
рН= 5,0-6,0
Укажите в каком случае при титровании скачок титрования наибольший:
сильная кислоты сильным основанием;
сильной кислоты слабым основанием;
слабой кислоты сильным основанием;
сильного основания слабой кислотой;
слабой кислоты слабым основанием
Ковалентная неполярная связь имеется в молекуле:
Хлора;
Хлороводорода;
Воды;
Сероводорода.
Хлорэтана
К сильным электролитам относится:
Сульфат натрия;
Муравьиная кислота;
Сернистая кислота;
Уксусная кислота.
Угольная кислота
Молярная масса вещества измеряется в:
г/моль;
а.е.м.;
а.е.м/моль;
м3/моль.
м2/моль
При взаимодействии оснований с кислотами образуется:
Соль и вода;
Соль и новая кислота;
Две соли;
Оксиды и вода.
Соль и новое основание
Молекулярная масса вещества измеряется в:
А.е.м.;
г/моль;
а.е.м/моль;
м3/моль;
м2/моль
Укажите основной внутриклеточный ион:
К+
Na+
Li+
Fe2+
Ca2+
Укажите основной внеклеточный ион:
Na+
Li+
Fe2+
Co2+
К+
Присутствием каких катионов обусловлена общая жесткость воды?
Ca2+, Mg2+
Ca2+, Na+
Mg2+,Fe2+
Ca2+, К+
Mg2+,Co2+
Без присутствия какого катиона невозможен процесс свертывания крови?
Ca2+,
Mg2+
Na+
Fe2+
К+
В каком ряду представлены только элементы-органогены?
H, C, O, N, P, S
Na, H, P, S, Cl, Li
Fe, C, O, N, P, S
Ca, Fe, P, S, N, O
Mg, Cl, H, C, N, Ca
Выберите ряд, в котором указаны только лиганды:
SO42-, Cl-, H2O
H2O, Cl-, Na,
SO42-, F-, Fe2+
Ni2+, OH-, NH3
Br-, NH3, Ag+
Выберите ряд, в котором указаны только комплексообразователи:
Fe2+, Fe3+, Cr3+
Zn2+, Fe2+, Cl-
Cu2+, Fe3+, Na+
Co2+, Pt2+, Li+
Cr3+, Ag+, Cl-
Какой из перечисленных биогенных элементов, являясь макроэлементом, находится в организме в виде ионов?
Хлор;
Медь;
Фтор;
Азот.
Углерод;
Какой из перечисленных ионов активирует фермент амилазу, секретируемую слюнными железами?

 .
.
 .
.
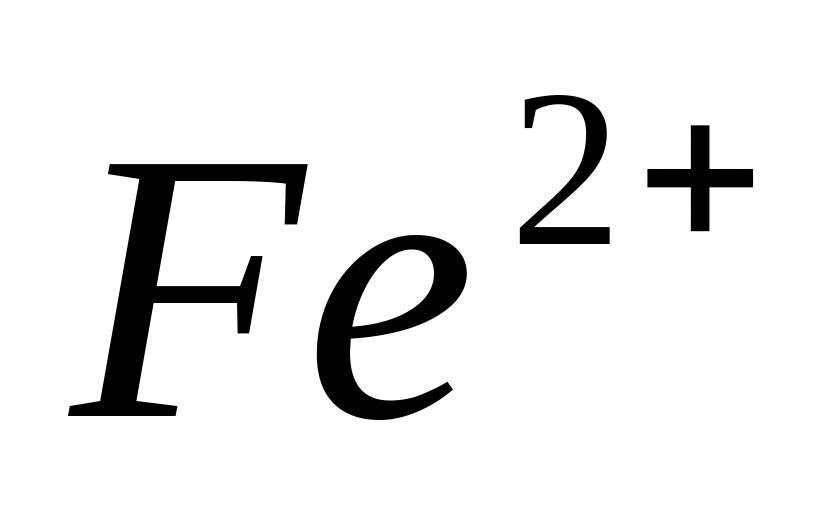 .
.
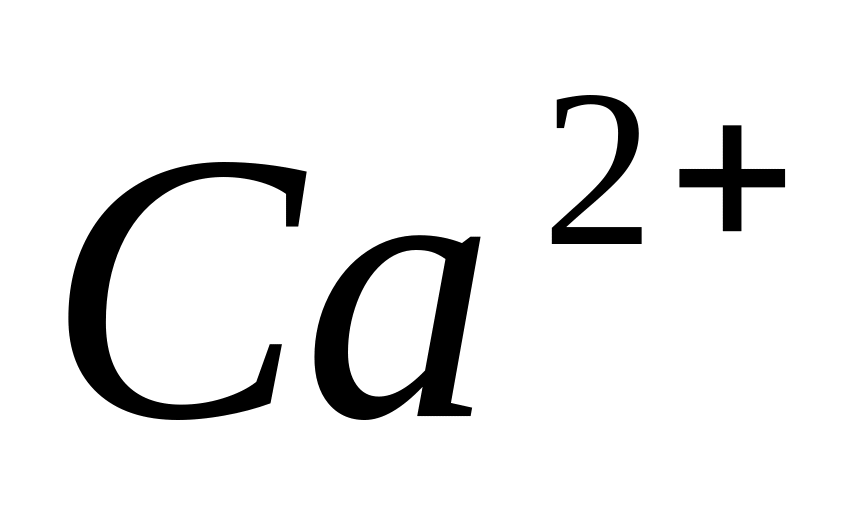 .
.
Какой элемент участвует в синтезе гормона поджелудочной железы – инсулина и является его незаменимым структурным компонентом?
Цинк
Сера.
Калий.
Кальций.
Йод
Дентатность лиганда определяется
Количеством -связей, образованных лигандом.
Количеством лигандов.
Зарядом комплексообразователя.
Координационным числом.
Количеством -связей, образованных комплексообразователем.
Какой из указанных металлов входит в состав ферментов, катализирующих окислительно-восстановительные процессы в организме:
