
- •20. Закон возрастания энтропии. Утверждение Клаузиуса о тепловой смерти Вселенной. Расширение газа в пустоту.
- •Парадокс Гиббса при диффузии газов.
- •Термодинамические функции: внутренняя энергия, энтальпия, свободная энергия Гельмгольца, термодинамический потенциал Гиббса. Соотношения Максвелла. Уравнения Гиббса - Гельмгольца.
- •23. Метод якобианов.
- •24. Максимальная работа. Уравнения Гиббса - Гельмгольца для максимальной и полезной работы.
- •25. Основные критерии устойчивости термодинамических систем. Принцип Ле-Шателье - Брауна.
- •27. Уравнение теплопроводности для случаев сферической и цилиндрической симметрии.
- •26. Теплопроводность. Вывод уравнения теплопроводности в общем виде. Принцип суперпозиций.
- •28. Вязкость газов. Скорость течения газа через трубу. Формула Пуазейля. Число Рейнольдса.
- •29. Отклонение свойств газов от идеальности. Молекулярные силы. Силы Ван-дер-Ваальса. Потенциал Леннарда - Джонса.
- •30. Уравнение Ван-дер-Ваальса.
- •31. Изотермы Ван-дер-Ваальса. Критические параметры.
- •32. Уравнение Ван-дер-Ваальса в приведенном виде. Закон соответственных состояний.
- •33. Правило Максвелла. Правило рычага.
- •34. Внутренняя энергия газа Ван-дер-Ваальса.
- •35.Эффект Джоуля - Томсона для газа Ван-дер-Ваальса. Случаи разреженного и плотного газов. Температура инверсии дифференциального эффекта Джоуля - Томсона.
- •36.Основные положения молекулярно-кинетической теории газов. Давление с точки зрения мкт.
- •37. Молекулярно-кинетический смысл температуры. Теорема о равномерном распределении кинетической энергии по степеням свободы.
20. Закон возрастания энтропии. Утверждение Клаузиуса о тепловой смерти Вселенной. Расширение газа в пустоту.
Рас-рим систему,к-я переходит из сост1 в сост2 необратимо, а из 2 в 1 –квазистатически. РИСУНОК
Для
этого процесса согласно неравенству
Клаузиуса, можно записать: .
Разобьем круговой интеграл на 2 интеграла:
.
Разобьем круговой интеграл на 2 интеграла:
 .
Т.к. переход из 2 в 1 – квст-й, то можем
воспользоваться определением разности
энтропий:
.
Т.к. переход из 2 в 1 – квст-й, то можем
воспользоваться определением разности
энтропий:
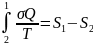 ;
;
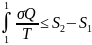 .
Рас-рим адиабатич процесс, для которого
σQ=0.
.
Рас-рим адиабатич процесс, для которого
σQ=0.
 .
.
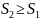 (1)
– закон возрастания энтропии.
(1)
– закон возрастания энтропии.
Энтропия адиабатически изолированной системы не может убывать: она либо возрастает либо остается постоянной. Закон возрастания энтропии наряду с определением энтропии также называется 2м началом ТД. Закон показывает направление процесса, к-й мог бы происходить в природе, т.к. обратимый процее – идеальзация.
Для необратимых процессов в замкнутых системах энтропия всегда возрастает. Рост энтропии в любом процессе происходит лишь до определенного максимального значения. Smax. Это знач-е соответствует состояниюравновесия.
Клаузиус, рассматривая Вселенную как замкнутую систему, свел содержание 2 н ТД к утверждению: «Энтропия Вселенной стремится к максимуму». Когда этот максимум будет достигнут, во Вселенной прекратятся какие бы то ни было процессы,т.е. согласно Клаузиусу во Вселенной наступит абсолютно равновесное состояние. Это состояние назвали тепловой смертью Вселенной. Однако, все законы были получены для ограниченных систем. Поэтому распространять их на бесконечную Вселенную нет оснований. Вселенная может эволюционировать непрерывно, никогда не приходя в равновесие, т.к. такого сост-я вообще не сущ-т. Такая возможность допускается общей теориет относительности.
Расширение газа в пустоту.
Рас-рим цилиндр, заключенный в адиабатическую оболочку, разделенный перегородкой на 2 части. В одной части объема V1 находится ид.газ, в др части объема V2 – вакуум. Затем перегородку квст-ки убирают, газ расширяется в пустоту. Обратим ли этот процесс?
РИС
Для ответа на этот вопрос необходимо
понять как ведет себя энтропия в этом
процессе. Запишем диф-й вид энтропии:
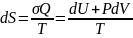 .
Т.к. сосуд заключен в адиабатич оболочку,
т.е. подвода тепла извне нет, то при
расширении газа его тем-ра не изменится.
dU=CVdT=0,
т.к. dT=0.
.
Т.к. сосуд заключен в адиабатич оболочку,
т.е. подвода тепла извне нет, то при
расширении газа его тем-ра не изменится.
dU=CVdT=0,
т.к. dT=0.
След-но:
 .
Запишем разность энтропий:
.
Запишем разность энтропий:
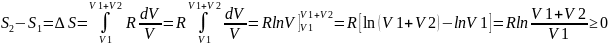
Т.е. энтропия при расширении газа в пустоту возрастает. След-но данный процесс необратим.
Парадокс Гиббса при диффузии газов.
РИСУНОК Рас-рим сосуд, разделенный перегородкой на 2 части, в обной части сосуда нах-ся ид.газ, а в др части – другой газ. Перегородку убирают, газы перемешиваются. Для обеспечения квазистатичности процесса предполагается, что перегородка состоит из 2х полупроницаемых перегородок, каждая из к-х проницаема только для одного газа. Будем квст-ки отодвигать перегородку I, заставляя расширяться 1й ид.газ (т.е. газ расширяется бесконечно медленно, проходя через последовательность равновесных состояний) Для этого процесса можем записать разность энтропий:

Теперь будем квст-ки отодвигать перегородку 2, заставляя расширяться 2й ид.газ.
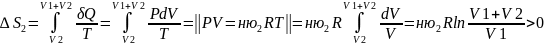
Тогда для процесса перемешивания газов можем записать:
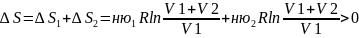 (*)
След-но, процесс взаимной диффузии
газов необратим.
(*)
След-но, процесс взаимной диффузии
газов необратим.
Ф-ла
(*) приводит к парадоксальному выводу,
называемому парадоксом Гиббса.
Предположим, что газы 1 и 2 одинаковы,
т.е. ню1=ню2. Пусть они занимают одинаковые
объемы в сосуде V1=V2=1/2V.
Подставим эти усл-я в (*):
 .
Т.е., согласно (*), диффузия одинаковых
газов – необратимый процесс. Однако,
конечное сост-е системы после того как
убрали перегородку макроскопически
ничем не отличается от начального.
Т.е. энтропия возросла, а сот-е системы
не изменилось. В этом и заключается
парадокс Гиббса.
.
Т.е., согласно (*), диффузия одинаковых
газов – необратимый процесс. Однако,
конечное сост-е системы после того как
убрали перегородку макроскопически
ничем не отличается от начального.
Т.е. энтропия возросла, а сот-е системы
не изменилось. В этом и заключается
парадокс Гиббса.
Разрешение парадокса: рассуждения были выполнены для существенно различных газов. На самом деле не возможно квст-ки перемешать одинаковые газы, т.к. для них не сущ-т полупроницаемых перегородок. След-но, нельзя воспользоваться определением разности энтропий.
