
лекция 20
.pdf
Раздел 2 Неорганическая химия
Тема 6 Основные классы неорганических соединений Лекция 20 Оксиды, гидроксиды
План лекции:
1)Классификация неорганических веществ
2)Бинарные соединения: классификация и номенклатура
3)Оксиды: классификация и номенклатура; методы получения; физические и химические свойства; применение
4)Гидроксиды (основания): классификация и номенклатура; методы получения; физические и химические свойства; применение
5)Характер изменения свойств оксидов и гидроксидов в периодической системе элементов

ПЕРВАЯ ПОПЫТКА КЛАССИФИКАЦИИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Антуан Лоран Лавуазье
1787 г.
•простые вещества;
•оксиды (продукты горения простых веществ);
•кислоты и основания (продукты взаимодействия оксидов с водой)
•соли (продукты взаимодействия кислот и оснований)
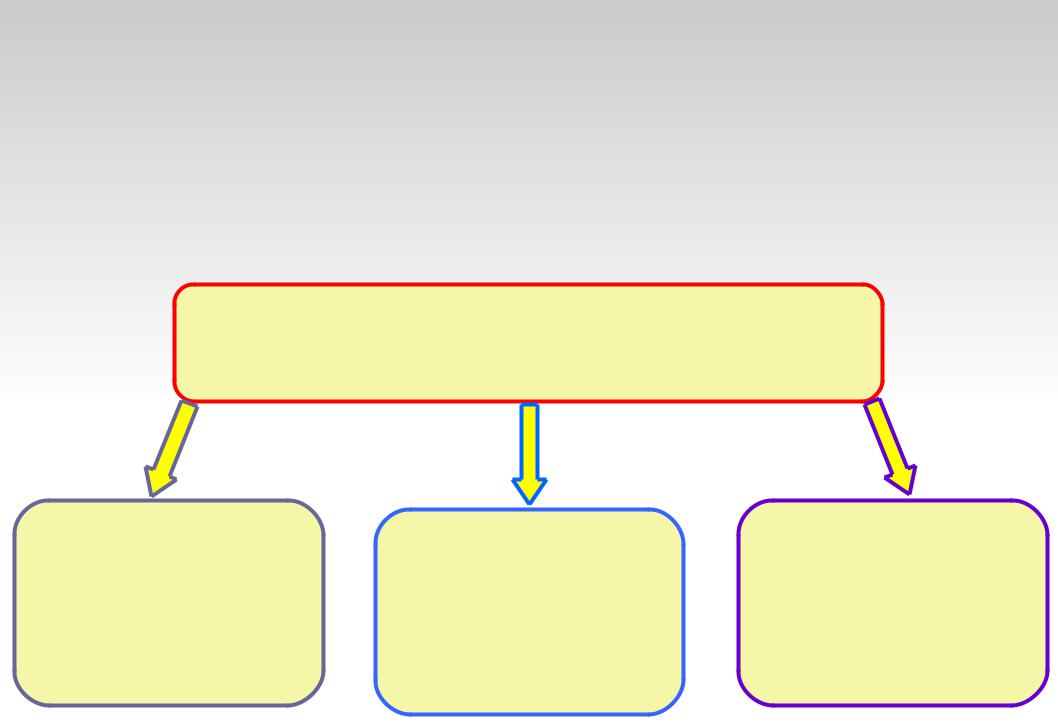
КЛАССИФИКАЦИЯ ПО ЧИСЛУ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ,
ВХОДЯЩИХ В СОСТАВ СОЕДИНЕНИЯ
Неорганические соединения
Одноэлементные |
Двухэлементные |
Многоэлементные |
||
(простые) |
||||
(бинарные) |
||||
соединения |
|
|||
вещества |
|
|||
соединения |
|
|||
(H2, O3, S8 ) |
(Ca (PO ) , H [PtCl ] ) |
|||
(NH3, NaCl, Fe2O3 ) |
||||
|
3 4 2 2 |
6 |
||

В простых веществах молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях они не могут разлагаться с образованием других веществ.
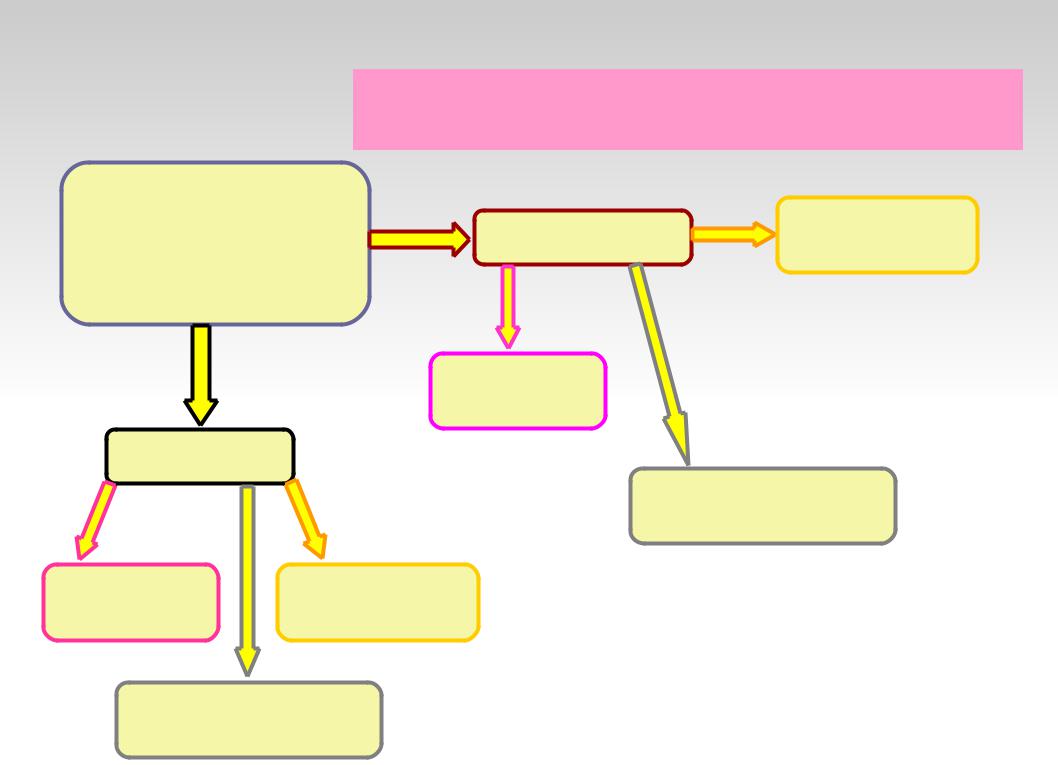
КЛАССИФИКАЦИЯ ПРОСТЫХ ВЕЩЕСТВ
•классификация на s-, p-, d- и f-элементы
•классификация на металлы и неметаллы
Одноэлементные |
Неметаллы |
Благородные |
|
(простые) |
|||
(He, Ne) |
|||
вещества |
|
|
Активные (F2, O2 )
Металлы
Среднеактивные (N2, Si)
Активные |
Благородные |
(Na, Ca) |
(Au, Rh) |
Среднеактивные (Fe, Ni)

В сложных веществах (или химических соединениях) молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях они разлагаются с образованием нескольких других веществ.

Бинарные вещества (бинарные соединения) – сложные вещества, в состав которых входят атомы двух элементов.
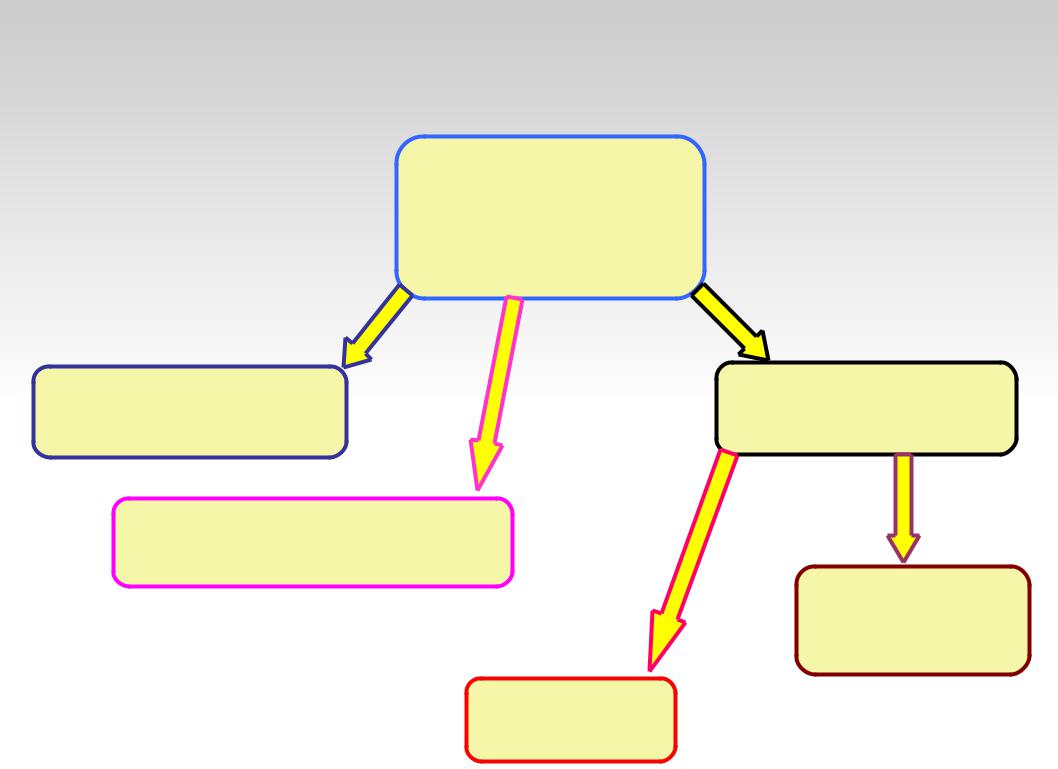
КЛАССИФИКАЦИЯ БИНАРНЫХ ВЕЩЕСТВ
Двухэлементные
(бинарные)
соединения
Интерметаллиды (Cu3Au, Tl2Hg5 )
Соединения неметаллов (S2Cl2, BN)
Соединения металл-неметалл
Ионные (бинарные соли) (NaBr, SnCl2 )
Ковалентные (SnCl4, TiCl4 )

НОМЕНКЛАТУРА СОЕДИНЕНИЙ ДВУХ МЕТАЛЛОВ (ИНТЕРМЕТАЛЛИДЫ)
запись формулы: первым (слева в формуле) записывают символ металла, который стоит левее в длиннопериодном варианте ПС
название дают справа налево в одно слово: Mg2Sn – оловодимагний NaZn4 – тетрацинкнатрий
Ag5Al3 – триалюминийпентасеребро Rb7Hg8 – октартутьгептарубидий NiCu3Al6 – гексаалюминийтримедьникель

НОМЕНКЛАТУРА СОЕДИНЕНИЙ ДВУХ НЕМЕТАЛЛОВ ИЛИ МЕТАЛЛ-НЕМЕТАЛЛ
название (по правилам ИЮПАК) дают справа налево в два слова:
первое слово – корень латинского названия более ЭО элемента (анион) + суффикс -ид
второе слово – русское название элемента в родительном падеже,
если менее ЭО элемент (катион) имеет несколько степеней окисления,
указывают его степень окисления
или с помощью числовых приставок указывают число атомов аниона
