
- •Применение
- •Аномалии воды
- •Кислотно-основные свойства
- •Окислительно-восстановительные свойства
- •Физические свойства
- •Химические свойства
- •Получение
- •Применение
- •ОБЩАЯ ХАРАКТЕРИСТИКА
- •ФТОР И ЕГО СОЕДИНЕНИЯ
- •Физические свойства
- •Химические свойства
- •Фтористый водород
- •Физические свойства
- •Химические свойства
- •ХЛОР И ЕГО СОЕДИНЕНИЯ
- •Физические свойства
- •Химические свойства
- •Соединения хлора Хлористый водород
- •Физические свойства
- •Химические свойства
- •Кислородсодержащие кислоты хлора
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •БРОМ И ЕГО СОЕДИНЕНИЯ
- •Физические свойства
- •Химические свойства
- •Бромистый водород HBr
- •Физические свойства
- •Химические свойства
- •ИОД И ЕГО СОЕДИНЕНИЯ
- •Физические свойства
- •Химические свойства
- •Иодистый водород
- •Физические свойства
- •Химические свойства
- •Кислородные кислоты йода
- •ОБЩАЯ ХАРАКТЕРИСТИКА
- •КИСЛОРОД
- •Физические свойства
- •Способы получения
- •Способы собирания
- •Химические свойства
- •Горение в кислороде
- •Озон O3
- •Физические свойства
- •Химические свойства
- •СЕРА И ЕЕ СОЕДИНЕНИЯ
- •СЕРА
- •Физические свойства
- •Аллотропия
- •Строение атома
- •Получение
- •Химические свойства
- •Реакции диспропорционирования:
- •Применение
- •СЕРОВОДОРОД
- •Физические свойства
- •Получение
- •Химические свойства
- •Сульфиды
- •Получение
- •Химические свойства
- •ОКСИДЫ СЕРЫ
- •Оксид серы IV
- •Физические свойства
- •Получение
- •Химические свойства
- •Оксид серы VI
- •Физические свойства
- •Получение
- •Химические свойства
- •СЕРНАЯ КИСЛОТА
- •Физические свойства
- •Производство серной кислоты
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •ОБЩАЯ ХАРАКТЕРИСТИКА
- •Общая характеристика элементов главной подгруппы V группы (подгруппы азота)
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •АЗОТ И ЕГО СОЕДИНЕНИЯ
- •ПОДГРУППА АЗОТА
- •АЗОТ
- •Физические свойства
- •Получение
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •АММИАК
- •Строение
- •Физические свойства
- •Получение
- •Химические свойства
- •Образование ковалентной связи по донорно-акцепторному механизму.
- •Аммиак - восстановитель (окисляется до N2+1O или N+2O)
- •ПОДГРУППА АЗОТА
- •СОЛИ АММОНИЯ
- •Физические свойства
- •Получение
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •ОКСИДЫ АЗОТА
- •Оксид азота (I)
- •N2+1O закись азота, "веселящий газ"
- •Физические свойства
- •Получение
- •Химические свойства
- •Оксид азота (II)
- •N+2O окись азота
- •Получение
- •Химические свойства
- •Оксид азота (III)
- •Физические свойства
- •Получение
- •Химические свойства
- •Оксид азота (IV)
- •N+4O2 двуокись азота, диоксид азота
- •Физические свойства
- •Получение
- •Химические свойства
- •Оксид азота (V)
- •N2+5O5 азотный ангидрид
- •Физические свойства
- •Получение
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •АЗОТИСТАЯ КИСЛОТА
- •HNO2 Азотистая кислота
- •Физические свойства
- •Получение
- •Химические свойства
- •ПОДГРУППА АЗОТА
- •АЗОТНАЯ КИСЛОТА
- •HNO3 Азотная кислота
- •Физические свойства
- •Получение
- •Химические свойства
- •Специфические свойства азотной кислоты
- •Сильный окислитель
- •ПОДГРУППА АЗОТА
- •РАЗЛОЖЕНИЕ НИТРАТОВ
- •Реакции разложения нитратов при нагревании
- •ПОДГРУППА АЗОТА
- •ФОСФОР И ЕГО СОЕДИНЕНИЯ
- •Важнейшие аллотропные модификации
- •Получение
- •Химические свойства.
- •Соединения фосфора
- •Получение
- •Химические свойства.
- •P2+3 O3 Фосфористый ангидрид (оксид фосфора (III)).
- •Получение
- •Химические свойства
- •P2+5O5 Фосфорный ангидрид (оксид фосфора (V)).
- •Получение
- •Химические свойства
- •HP+5O3 Метафосфорная кислота.
- •Получение
- •Химические свойства
- •H3P+5O3 Фосфористая кислота
- •Получение
- •Химические свойства
- •H3P+5O4 Ортофосфорная кислота.
- •Диссоциация:
- •Получение
- •Химические свойства
- •Фосфорные удобрения
- •Фосфоритная мука
- •УГЛЕРОД
- •Аллотропия
- •Алмаз
- •Карбин
- •Адсорбция
- •Химические свойства
- •Химические свойства
- •Способы собирания
- •Химические свойства
- •Качественная реакция
- •Угольная кислота и её соли
- •КРЕМНИЙ
- •Аллотропия
- •Химические свойства
- •Химические свойства
- •Физические свойства
- •Кислотный оксид
- •Кремниевые кислоты
- •ОБЩИЕ СВОЙСТВА
- •Положение металлов в периодической таблице
- •Общие свойства металлов Виды кристаллических решеток
- •Общие физические свойства
- •Общие химические свойства металлов
- •ЩЕЛОЧНЫЕ МЕТАЛЛЫ
- •Общая характеристика
- •Свойства щелочных металлов
- •Физические свойства
- •Химические свойства
- •Нахождение в природе
- •Химические свойства
- •Оксиды щелочных металлов – R2O
- •Получение
- •Химические свойства
- •Пероксид натрия Na2O2
- •Получение
- •Химические свойства
- •Надпероксид калия KO2
- •Получение
- •Химические свойства
- •Гидроксиды щелочных металлов – ROH
- •Получение
- •Химические свойства
- •МЕТАЛЛЫ
- •ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
- •Свойства щелочноземельных металлов
- •Физические свойства
- •Химические свойства
- •Нахождение в природе
- •Получение
- •Оксиды щелочноземельных металлов
- •Получение
- •Химические свойства
- •Гидроксиды щелочноземельных металлов R(OH)2
- •Получение
- •Химические свойства
- •Жесткость воды
- •ПОДГРУППА АЛЮМИНИЯ
- •Свойства элементов подгруппы алюминия
- •Физические свойства
- •Химические свойства
- •Алюминий
- •Физические свойства
- •Нахождение в природе
- •Получение
- •Химические свойства
- •Применение
- •Получение
- •Гидроксид алюминия
- •Получение
- •ПЕРЕХОДНЫЕ МЕТАЛЛЫ
- •Общие свойства
- •ПОДГРУППА ЖЕЛЕЗА
- •Свойства элементов подгруппы железа
- •Получение металлов подгруппы железа
- •Железо и его соединения
- •Химические свойства
- •Соединения двухвалентного железа
- •Гидроксид железа (II)
- •Качественная реакция на Fe2+
- •Соединения трёхвалентного железа
- •Оксид железа (III)
- •Гидроксид железа (III)
- •Качественные реакции на Fe3+
- •Кобальт и его соединения
- •Гидроксид кобальта (II)
- •Никель и его соединения
- •ПОДГРУППА МЕДИ
- •Подгруппа меди – побочная подгруппа I группы
- •Свойства элементов подгруппы меди
- •Физические свойства
- •Химические свойства
- •Медь и её соединения
- •Получение
- •Химические свойства
- •Соединения одновалентной меди
- •Соединения двухвалентной меди
- •Серебро и его соединения
- •Золото и его соединения
- •ПОДГРУППА МАРГАНЦА
- •Подгруппа марганца
- •Побочная подгруппа VII группы
- •Свойства элементов подгруппы марганца
- •Физические свойства
- •Химические свойства
- •Марганец и его соединения
- •Марганец
- •Получение
- •Химические свойства
- •Соединения Mn(II)
- •ПОДГРУППА ХРОМА
- •Подгруппа хрома - побочная подгруппа VI группы
- •Свойства элементов подгруппы хрома
- •Физические свойства
- •Химические свойства
- •Хром и его соединения
- •Получение
- •Соединения хрома
- •Соединения двухвалентного хрома
- •Соединения трёхвалентного хрома
- •Соединения шестивалентного хрома
- •ПОДГРУППА ЦИНКА
- •Физические свойства
- •Химические свойства
- •Цинк и его соединения
- •Кадмий и его соединения
- •Ртуть и ее соединения
- •Получение
- •Химические свойства.
- •Галогениды ртути (II)
- •Получение
- •Химические свойства:
Неустойчива, при затвердевании превращается в ромбическую.
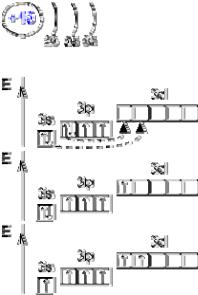
Строение атома
Размещение электронов по уровням и подуровням
1s22p22p63s23p4
Размещение электронов по |
Степень |
Валентность |
орбиталям (последний слой) |
окисления |
|
+2, -2 II
+4 IV
+6 VI
Получение
1.Промышленный метод - выплавление из руды с помощью водяного пара.
2.Неполное окисление сероводорода (при недостатке кислорода).
2H2S + O2 → 2S + 2H2O
3. Реакция Вакенродера
2H2S + SO2 → 3S + 2H2O
Химические свойства
Окислительные свойства серы
(S0 + 2ē → S-2)
1) Сера реагирует со щелочными металлами без нагревания:
2Na + S → Na2S
c остальными металлами (кроме Au, Pt) - при повышенной t°:
2Al + 3S –t°→ Al2S3
Zn + S –t°→ ZnS
2) С некоторыми неметаллами сера образует бинарные соединения:
H2 + S → H2S 2P + 3S → P2S3 C + 2S → CS2
Восстановительные свойства сера проявляет в реакциях с сильными окислителями: (S - 2ē → S+2; S - 4ē → S+4; S - 6ē → S+6)
