
Обмен веществ как важнейшая особенность живой матери. Единство процессов ассимиляции и диссимиляции.
Биологическое окисление, его роль в процессе обмена веществ. Тканевое дыхание. Дыхательная цепь митохондрий. Пиридинзависимые дегидрогеназы, флавиновые ферменты, кофермент Q, цитохромы. Макроэргические соединения. АТФ и ее роль в процессах биологического окисления. Окислительное и субстратное фосфорилирование. Свободное окисление.
ОБМЕН ВЕЩЕСТВ И ЭНЕРГИИ В ЖИВЫХ ОРГАНИЗМАХ. БИОЭНЕРГЕТИКА
Живые организмы находятся в постоянной и неразрывной связи с окружающей средой. Эта связь осуществляется в процессе обмена веществ. Обмен веществ включает 3 этапа: поступление веществ в организм, метаболизм или промежуточный обмен и выделение конечных продуктов из организма.
Поступление веществ в организм происходит в результате дыхания (кислород) и питания. В ЖКТ продукты питания перевариваются (расщепляются до простых веществ), всасывающихся в кровь и включающихся в промежуточный обмен. Промежуточный обмен (внутриклеточный метаболизм) включает 2 типа реакций: катаболизм и анаболизм.
Катаболизм — процесс расщепления органических молекул до конечных продуктов. Конечные продукты превращений органических веществ у животных и человека — СО2, Н2О и мочевина. В процессы катаболизма включаются метаболиты, образующиеся как при пищеварении, так и при распаде структурно-функциональных компонентов клеток. Реакции катаболизма сопровождаются выделением энергии.
Анаболизм объединяет биосинтетические процессы, в которых молекулы-предшественники соединяются в сложные макромолекулы, необходимые для организма. В анаболических реакциях используется энергия, освобождающаяся при катаболизме.
С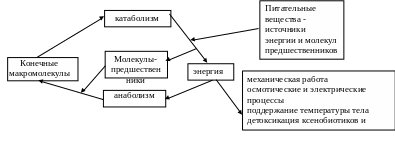 вязь
процессов катаболизма и анаболизма
можно представить следующей схемой:
вязь
процессов катаболизма и анаболизма
можно представить следующей схемой:
Образование молекулы АТР, главного источника энергии для совершения работы в биологических системах, сегодня не может быть описано в терминах точного химического механизма элементарных стадий, однако ясно, что движущей силой процесса служит энергия электрического поля, существующего на внутренней мембране митохондрий. Возникает естественный вопрос: что служит источником этой энергии? В самом общем виде ответ можно сформулировать так. Питательные вещества (белки, жиры и углеводы) в конечном счете превращаются в ограниченный набор низкомолекулярных соединений — органических кислот. Углеродные атомы, из которых построены эти кислоты, окисляются (у аэробных организмов кислородом) до углекислого газа и воды. Процесс окисления органических кислот кислородом происходит в митохондриях — клеточных органеллах, обеспечивающих бóльшую часть синтеза АТР в клетках. Потребление кислорода в качестве окислителя обычно называют внутриклеточным дыханием. Энергия, освобождающаяся в результате химической реакции окисления, превращается в электрохимическую и в таком виде используется для синтеза АТР.
Биологическое окисление определяется как совокупность реакций окисления органических веществ (субстратов), выполняющих функцию энергетического обеспечения потребностей организма.
Согласно СОВРЕМЕННОЙ ТЕОРИИ БИООКИСЛЕНИЯ окисление может происходить двумя способами:
1. Путем отнятия водорода от окисляемого субстрата: сюда относятся МИТОХОНДРИАЛЬНОЕ ОКИСЛЕНИЕ и ВНЕМИТОХОНДРИАЛЬНОЕ ОКИСЛЕНИЕ ОКСИДАЗНОГО ТИПА.
2. Путем присоединения кислорода к окисляемому субстрату - так происходит внемитохондриальное ОКИСЛЕНИЕ ОКСИГЕНАЗНОГО ТИПА ИЛИ СВОБОДНОЕ ОКИСЛЕНИЕ.
Митохондриальное окисление
Система митохондриального окисления - мультиферментная система, постепенно транспортирующая протоны и электроны на кислород с образованием молекулы воды. Все ферменты митохондриального окисления (кроме, никотинамидной дегидрогеназы) встроены во внутреннюю мембрану митохондрий. Полный комплекс таких ферментов образует «дыхательную цепь», в пределах которой атомы водорода отнимаются от субстрата, затем передаются последовательно от одного переносчика к другому, и, наконец, на кислород воздуха с образованием воды.
Существует строгая последовательность работы каждого звена в цепочке переносчиков. Эта последовательность определяется величиной ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ПОТЕНЦИАЛА, сокращенно - ОВП каждого звена. ОВП - это химическая характеристика способности вещества принимать и удерживать электроны. Самый низкий ОВП имеет начальное звено цепи, самый высокий - у кислорода, расположенного в конце цепочки переносчиков. Таким образом, передача водорода идет от более низкого к более высокому ОВП.
Кислород является конечным акцептором электронов. O2 + 4e -----> 2O-2 (полное восстановление кислорода)
В настоящее время различают три варианта дыхательных цепей:
Главная (полная) цепь. 2.Укороченная (сокращенная) цепь. 3.Максимально укороченная (максимально сокращенная) цепь.
ГЛАВНАЯ ДЫХАТЕЛЬНАЯ ЦЕПЬ
Главная дыхательная цепь - это три мультиферментных комплекса, встроенных во внутреннюю мембрану митохондрии. Обозначаются они латинскими цифрами – I, III и IV.
Субстратами главной дыхательной цепи являются:
изолимонная кислота (изоцитрат) фермент - изоцитратдегидрогеназа,
яблочная кислота (малат), фермент - малатдегидрогеназа,
глутаминовая кислота (глутамат), фермент – глутаматдегидрогеназа,
β-гидроксиацил-КоА, фермент - β-гидроксиацил-КоА-дегидрогеназа.
С хема главной (полной) дыхательной цепи митохондриального окисления Этапы дыхательной цепи
1. Дегидрирование субстрата (отнятие от него 2 протонов и 2 электронов) первичными дегидрогеназами. Чаще всего их роль выполняют никотинамидные ферменты.
Небелковая часть этих ферментов представляет собой динуклеотид: НИКОТИНАМИД-АДЕНИНДИНУКЛЕОТИД (НАД+) или НИКОТИНАМИДАДЕНИНДИНУКЛЕОТИДФОСФАТ (НАДФ+).
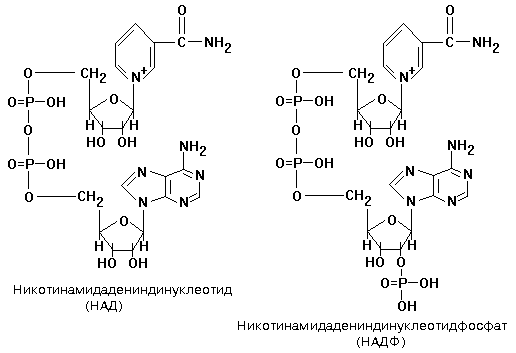
НАД+ и НАДФ+ входят в состав каталитического центра никотинамидных дегидрогеназ. Они являются КОФЕРМЕНТАМИ, и присоединяются к белковой части только в момент реакции окисления субстрата, протекающего обычно по механизму:
R1-CH2-R2+ НАД++1/2O- = R1-CO-R2+ НАДH∙H
Из матрикса митохондриальный НАДН2 отдает два атома водорода на «комплекс I», встроенный во внутреннюю мембрану митохондрий.
2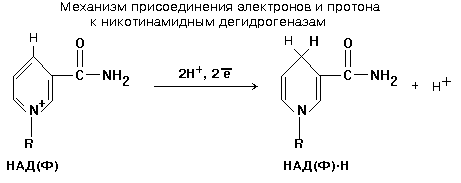 .
Передача протонов и электронов на
флавиновые ферменты, выполняющие роль
вторичных дегидрогеназ (комплекс1).
.
Передача протонов и электронов на
флавиновые ферменты, выполняющие роль
вторичных дегидрогеназ (комплекс1).
Из небелковых компонентов КОМПЛЕКС I содержит флавинмононуклеотид (ФМН) и пять железо-серных центров FeS.
В транспорте водорода по дыхательной цепи в этом комплексе принимает участие ФМН.
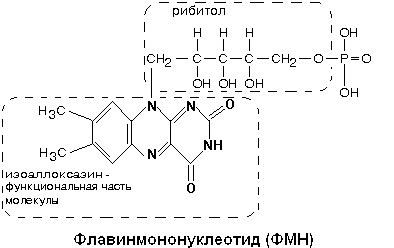
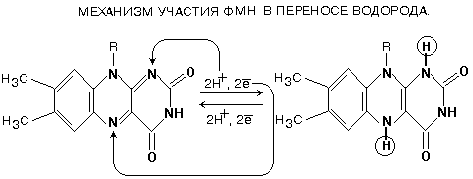
Одновременно с протонами транспортируются и электроны.
И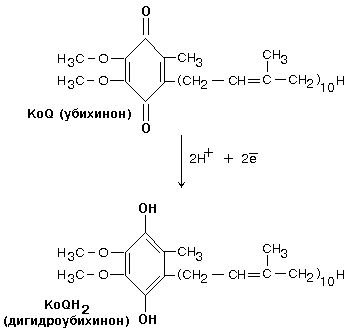 спользуя
энергию, выделяющуюся при переносе
электронов по дыхательной цепи, Комплекс
I
транспортирует 4 протона из матрикса в
межмембранное пространство – работает
как протонный генератор. Точный механизм
этого транспорта до сих пор неизвестен.
спользуя
энергию, выделяющуюся при переносе
электронов по дыхательной цепи, Комплекс
I
транспортирует 4 протона из матрикса в
межмембранное пространство – работает
как протонный генератор. Точный механизм
этого транспорта до сих пор неизвестен.
3. Передача протонов и электронов от флавиновых ферментов на кофермент Q.
Кофермент Q - это жирорастворимое низкомолекулярное вещество, содержащее длинную изопреновую цепь, не имеет белковой части. КоQ принимает водород от комплекса I. Образовавшийся КоQH2 отдает водород на комплекс III.
4. Передача электронов от КоQ на О по системе цитохромов.
В своем составе комплекс III содержит: цитохромы – сложные белки, содержащие небелковый компонент - простетическую группу, сходную по строению с небелковой частью гемоглобина – гемом и FeSIII – железо-серный кластер.
Цитохромы расположены в дыхательной цепи в следующей последовательности:
цит С1 цит А цит аа3 цит В
Цитохромы А, В, С различаются строением гемма. Цитохромы С и С1, а и а3 различаются белковой частью.
О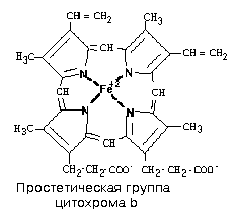 т
двух атомов водорода, которые переносятся
на комплекс III
от KoQ,
дальше по цепи транспортируются только
электроны, два протона (H+)
комплекс III
выбрасывает в межмембранное пространство
вместе с еще одной парой протонов,
которые подхватываются комплексом из
матрикса. Таким образом, комплекс III
в сумме выбрасывает в межмембранное
пространство 4 протона.
протонным генератором,
т
двух атомов водорода, которые переносятся
на комплекс III
от KoQ,
дальше по цепи транспортируются только
электроны, два протона (H+)
комплекс III
выбрасывает в межмембранное пространство
вместе с еще одной парой протонов,
которые подхватываются комплексом из
матрикса. Таким образом, комплекс III
в сумме выбрасывает в межмембранное
пространство 4 протона.
протонным генератором,
Комплекс IV называется цитохромоксидазой. Это единственный цитохром, обладающий каталитическими, т. е. ферментативными, свойствами, другие цитохромы не являются ферментами. Он способен захватывать из матрикса 4 протона. Два из них он отправляет в межмембранное пространство, а остальные передает на образование воды.
СОКРАЩЕННАЯ (УКОРОЧЕННАЯ) ДЫХАТЕЛЬНАЯ ЦЕПЬ
Принимают участие два субстрата.
Сукцинат (янтарная кислота), который окисляется ферментом сукцинатдегидрогеназой и ацил-Ко А – ацил-Ко А-дегидрогеназа.
Эти субстраты передают атомы водорода на комплекс II, который в укороченном варианте цепи является начальным звеном окисления. В составе комплекса – простетическая группа ФАД и FeSII железо-серный кластер.
От ФАД.Н2 два атома водорода переносятся на KoQ. Значит, первое звено, которое имеется в полной цепи - исключается. Перепад окислительно-восстановительного потенциала между ФАД и KoQ невелик. Поэтому переноса H+ в межмембранное пространство в этой точке не происходит.
Затем окисление проходит аналогично главной дыхательной цепи.
МАКСИМАЛЬНО СОКРАЩЕННАЯ (МАКСИМАЛЬНО УКОРОЧЕННАЯ) ДЫХАТЕЛЬНАЯ ЦЕПЬ.
Она представлена только цитохромной частью. Здесь может быть окислен только один субстрат - аскорбиновая кислота. С участием фермента, восстановленные эквиваленты витамина С включаются в цепь на уровне цитохрома С.
