
Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Московский институт стали и сплавов (технологический университет)
Новотроицкий филиал
Электропроводность электролитов Расчетно-графическая работа 3 по физической химии
Выполнил студент гр. МЧМ-05-22 /./
Принял доцент /Шерстобитов М. А./
Новотроицк, 2007
Расчетно-графическая работа 3
Задача 1
-
Рассматривается водный раствор слабого электролита АВ при температуре 25оС.
- определить степень диссоциации электролита в растворе концентрации Со, моль/дм3;
-
определить эквивалентную и удельную электропроводность;
-
определить скорости движения (подвижности ионов) при предельном разбавлении раствора;
-
определить числа переноса ионов.
Решение
Вариант 13
Рассматривается водный раствор слабого электролита C2H5COOH при температуре 25оС.
-
определить степень диссоциации электролита в растворе концентрации
Со=0.1 моль/дм3;
-
определить эквивалентную и удельную электропроводность;
-
определить скорости движения (подвижности ионов) при предельном разбавлении раствора;
-
определить числа переноса ионов.
Электролитическая диссоциация пропионовой кислоты описывается уравнением:
C2H5COOH = H+ + C2H5COO–
Константа диссоциации имеет вид:
![]() Где α – степень
диссоциации электролита; С0
– валовая концентрация электролита.
Где α – степень
диссоциации электролита; С0
– валовая концентрация электролита.
При малой степени диссоциации 1 – α ≈ 1 , поэтому получаем:
![]()
![]() При 25 С0
константа диссоциации пропионовой
кислоты равна
1.34 * 10-5
[1].
При 25 С0
константа диссоциации пропионовой
кислоты равна
1.34 * 10-5
[1].
В растворе концентрации С0=0.1 моль/л степень диссоциации кислоты составит:
α=( 1.34*10-5/0.1)1/2=1.16*10-2=1.16 %.
Эквивалентной электропроводностью λ раствора электролита называют количество электричества, перенесенного одним моль-эквивалентом электролита за единицу времени при единичном градиенте электрического потенциала.
Удельной электропроводностью χ называют количество электричества перенесенного через единичную площадь за единицу времени при единичном градиенте потенциала.
Эти электропроводности связаны уравнением λ = 1000 (χ/С0).
Эквивалентная электропроводность монотонно уменьшается с концентрацией электролита. При концентрации, стремящейся к нулю, предельное значение электропроводности обозначают λ∞. По закону Кольрауша: λ∞= λ+ + λ- ,
т.е предельная электропроводность раствора равна сумме эквивалентных электропроводностей и ионов (подвижностей ионов).
Подвижностью ионов в бесконечно разбавленном растворе называется количество электричества, перенесенного одним моль-эквивалентом ионов данного сорта в электрическом поле при единичном градиенте потенциала (напряженности). Подвижности связаны с абсолютными скоростями движения ионов уравнениями: λ+ =F • υ+0 ; λ- - = F• υ-0, где F-константа Фарадея, т.е. электрический заряд моля электронов.
Недиссоциированные молекулы электролита не переносят электричества, поэтому эквивалентная электропроводность одно-одновалентного электролита связана с предельной электропроводностью уравнением:
λ = α· λ∞
Числом переноса ионов данного сорта t+ или t- называют долю (часть) электричества, перенесенного ионами данного сорта:
t![]()
![]() +
= Q+
/ (Q++Q-)
= λ+
/ (λ+
+ λ--)
= υ+./
(υ+
υ-)
+
= Q+
/ (Q++Q-)
= λ+
/ (λ+
+ λ--)
= υ+./
(υ+
υ-)
t![]()
![]() -
= Q-
/ (Q++Q-)
= λ--
/ (λ+
+ λ--)
= υ-./
(υ+
υ-)
-
= Q-
/ (Q++Q-)
= λ--
/ (λ+
+ λ--)
= υ-./
(υ+
υ-)
t+ + t - =1
Таблица 2. Предельная электрическая проводимость ионов в водном растворе при 25 0С
|
Катионы |
Λ+ , См*см2/моль |
Анионы |
Λ- , См*см2/моль |
|
H+ |
349.6 |
HCO3- |
44.5 |
|
NH4+ |
50.1 |
OH- |
198.3 |
|
|
|
HS- |
65 |
|
|
|
HCOO- |
54.6 |
|
|
|
CH3COO- |
40.9 |
|
|
|
C2H5COO- |
35.6 |
|
|
|
C3H7COO- |
32.6 |
|
|
|
C4H9COO- |
28.8 |
В нашем случае (водный раствор пропионовой кислоты концентрации 0.1 M)
α = 0.0116.
В таблице 2 приведены подвижности ионов в бесконечно разбавленном водном по данным [1].
Таблица 3. Константы диссоциации слабых кислот и оснований в водных растворах при 25 0С
|
Кислоты |
Kд |
Основания |
Kд |
|
Масляная С4H8O2 |
1.51*10-5 |
Гидроксид аммония NH4OH |
1.77*105 |
|
Молочная C3H6O3 |
1.7*10-4 |
|
|
|
Муравьиная CH2O2 |
1.77*10-4 |
|
|
|
Пропионовая C3H6O2 |
1.34*10-5 |
|
|
|
Cероводородная H2S |
(I)1.1*10-2 (II)3.6*10-12 |
|
|
|
Угольная H2CO3 |
(I)4.45*10-7 (II)4.7*10-11 |
|
|
|
Уксусная C2H4O2 |
1.75*10-5 |
|
|
По данным таблицы 2 подвижности ионов в водном растворе равны 349.6 См * см2 для H+ и 35.6 См * см2 для C2H5COO–. Тогда предельная эквивалентная электропроводность определится:
Λ0= Λ+ + Λ-=349.6+3.6=385.2 См*см2/моль
Определим эквивалентную электропроводность раствора:
Λ= Λ0 * α = 385.2*0.0116 = 4.47 См*см2/моль
Удельная электропроводность составит:
Χ = С * Λ = 0.1*4.47 = 0.447 См/см2
Определим числа переноса ионов:
t+ = Λ+ / (Λ+ + Λ- ) = 349.6 / (349.6+35.6 ) = 0.91
t- = Λ- / (Λ+ + Λ- ) = 35.6 / (349.6+35.6 ) = 0.09
Скорость и движение ионов:
V+ = Λ+ / F = 349.6 / 96500 = 0.007 cм2/В*с
V- = Λ- / F = 35.6 / 96500 = 3.69*10-4 cм2/В*с
Задача 2
Вариант 26
Определить влияние температуры на удельную электрическую проводимость расплавов системы CaO-Al2O3-SiO2, содержащего 41.6 %СаО, 11.4 %Al2O3, 47 %SiO2.
Содержание работы
Расплавленные оксидные расплавы (шлаки) обладают сравнительно хорошей электрической проводимостью. Измерения электропроводности расплавленных шлаков явились одним из основных доказательств их ионной природы. Согласно современным представлениям о строении оксидных расплавов, за редким исключением это ионные системы. Они состоят из катионов одно- и двухзарядных металлов (Na+, K+, Ca2+ , Mg2+, Fe2+, Mn2+ и других) и анионов (одноатомных: O2-, S2- и комплексных: SiO44-, PO44-, AlO2-). Согласно полимерной теории анионы могут быть представлены полимеризованными комплексными анионами, состоящими из кремнекислородных тетраэдров, объединенных в цепочки или кольца.
Одноатомные катионы наиболее подвижны, поэтому силикатные расплавы преимущественно имеют катионную проводимость, т.е. в них число переноса катионов близко к единице. Исключение составляют расплавы с высоким содержанием оксидов железа и марганца, проявляющие полупроводниковые свойства. В них высока доля электронной или дырочной проводимости.
Количественной характеристикой электрической проводимости шлака является удельная электропроводность - количество электричества, проходящего через единицу площади сечения проводника за единицу времени при единичном градиенте электрического потенциала.
Электрическое сопротивление R проводника длиной L c площадью поперечного сечения S и с удельным сопротивлением определяется известным выражением:
![]() (1)
(1)
Удельная электропроводность - величина, обратная удельному сопротивлению электрического проводника:
=1/
= (L/S)/R
= C/R![]() (2)
(2)
Электроперенос в шлаках осуществляется перемещением ионов, и для совершения элементарного акта необходима дополнительная энергия E, называемая энергией активации электропроводности. Температурная зависимость удельной электропроводности шлака выражается уравнением экспоненты:
= 0 exp(-E / RT) (3)
В уравнении (3) 0 –предэкспоненциальный множитель, зависящий от природы шлака:
R – универсальная газовая постоянная (8,31 Дж/моль К).
В отличие от металлических проводников, ионные имеют положительный температурный коэффициент электрической проводимости (d/dT 0), т.е. величина возрастает с температурой.
Об ионном характере электропроводности шлаковых расплавов можно утверждать также по величине , составляющей 10-2 – 10 Ом-1см-1. С учетом вязкости шлаков их электропроводность превышает таковую для типично ионных солевых расплавов, например, хлоридов.
Измерения электропроводности шлаков выполняют, определяя электрическое сопротивление ячейки из инертных электродов известной геометрии. В качестве материала электродов применяют платину, измерение сопротивления ячейки выполняют с помощью четырехплечевого моста переменного тока звуковой частоты. Геометрическая постоянная ячейки C, т.е. отношение L/S определяется градуировкой по раствору с известной электропроводностью, например, водному раствору хлорида калия.
Таким методом была определена, в частности, электрическая проводимость расплавов системы CaO-Al2O3-SiO2, основы доменных шлаков. В таблице 1 приведены результаты измерения величины шлака, содержащего 45 %CaO, 10 %Al2O3 45 %SiO2 при 1350 – 1550 0С.
Таблица 4. Удельная электропроводность шлака при различных температурах
|
t, 0C |
T, K |
1000/T |
, Ом-1см-1 |
lg |
|
1350 |
1623 |
0,6161 |
0,055 |
-1,26 |
|
1400 |
1673 |
0,5977 |
0,078 |
-1,108 |
|
1450 |
1723 |
0,5803 |
0,109 |
-0,963 |
|
1500 |
1773 |
0,5640 |
0,146 |
-0,836 |
|
1550 |
1823 |
0,5485 |
0,187 |
-0,728 |

Рисунок 1. Удельная электропроводность шлака
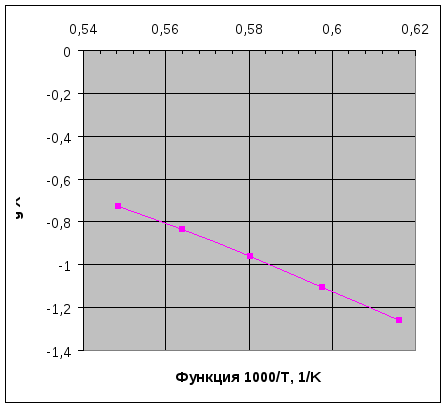
Рисунок 2. Определение энергии активации электропереноса
На рисунке 2 видно, что зависимость электропроводности от температуры в координатах lg - 1/T спрямилась. Получим уравнение прямой lg = A/T + B, для чего воспользуемся двумя крайними точками с координатами:
X1=0,5485, Y1= -0,728; X2= 0,6161, Y2= -1,26.
A = (Y2 – Y1)/(X2 – X1) = (-1,26 + 0,728)/(0,6161 – 0,5485)= -8,270
B = Y1 – AX1 = -0,728 + 8,2700,5485 = 3,83.
Таким образом, уравнение зависимости от температуры имеет вид: lg = -8,270 X + 3,83 = -8230/T + 3,83.
Энергия активации электропереноса составляет:
E = 2,3 8,318230 = 157300 Дж/мол = 157,3 кДж/мол.
В явном виде (рисунок 1) зависимость электропроводности от температуры принимает вид
= 10B exp (-E/RT) = 6,8103 exp (-157300/RT) Ом-1см-1
Выводы
1 Обработаны справочные результаты об измерении удельной электрической проводимости расплава системы CaO-Al2O3-SiO2 в температурном интервале 1350 – 1550 0С.
2. Зависимость удельной электропроводности от температуры описывается уравнениями:
lg = -8230/T + 3,83. = 6,8103 exp (-157300/RT) Ом-1см-1.
3. Энергия активации электропереноса составляет 157,3 кДж/мол.
4. Положительный температурный коэффициент электропроводности и порядок величины подтверждают ионное строение расплава.
Контрольные вопросы
-
Каковы основные компоненты металлургических шлаков?
-
Каковы экспериментальные доказательства ионного строения шлаков?
-
Дайте определение понятия "удельная электрическая электропроводность".
-
Из каких частиц состоят металлургические шлаки?
-
Как определяют удельную электрическую проводимость расплавов?
-
Что такое энергия активации электропереноса, и как она может быть определена?
-
Почему рисунок 2 назван "Определение энергии активации"?
