
- •Введение
- •2.1.3. Материальный баланс
- •2.1.4. Построение рабочей лини.
- •2.2. Расчет движущей силы массопередачи
- •2.3.Коэффициента массопередачи
- •2.3.1. Расчет скорости газа
- •2.3.2. Диаметр абсорбера
- •2.3.3. Расчет плотности орошения и активной поверхности насадки
- •2.3.4. Расчет коэффициента массоотдачи
- •2.3.4.1. Расчет коэффициента диффузии в газе
- •2.3.4.2. Расчет коэффициента диффузии в жидкой фазе
- •2.4. Расчет поверхности массопередачи и высоты абсорбера
- •2.5. Расчет гидравлического сопротивления абсорбера
- •3.Прочностной расчет
- •3.1.Выбор конструкционных материалов
- •3.2.Расчет толщины стенки обечайки
- •3.3.Расчет толщины стенки крышки и днища
- •3.4.Расчет аппарата на ветровую нагрузку
- •3.5.Расчет опоры аппарата
- •4. Расчет и подбор вспомогательного оборудования
- •4.1. Выбор трубопровода.
- •4.2.Определение потерь на трение и местные сопротивления.
- •4.3. Выбор насоса.
- •4.4. Определение предельной высоты всасывания
- •4.5. Расчет газодувки
- •4.6.Расчет и подбор емкостей
- •4.7.Расчет и подбор подогревателя
- •4.8. Расчет и подбор холодильника
- •4.9. Десорбер
Введение
 Абсорбция
широко применяется в химической и
смежных отраслях промышленности. При
этом преследуются две главные цели:
извлечение ценных компонентов из газовой
смеси; очистка газовых смесей от примесей
перед их использованием в технологических
процессах или перед их выбросом в
атмосферу.
Абсорбция
широко применяется в химической и
смежных отраслях промышленности. При
этом преследуются две главные цели:
извлечение ценных компонентов из газовой
смеси; очистка газовых смесей от примесей
перед их использованием в технологических
процессах или перед их выбросом в
атмосферу.
Укажем некоторые области применения процессов абсорбции:
- получение готовых продуктов в виде насыщенных абсорбентов. Это, например, абсорбция хлороводорода водой с получением соляной кислоты, абсорбция серного ангидрида в производстве серной кислоты;
- разделение газовых смесей при помощи селективных поглотителей. Например, извлечение бензола из коксовых газов, ацетилена – из газов крекинга, бутадиена- из контактного газа после разложения этилового спирта;
- очистка газов от нежелательных примесей. Например, очистка нефтяных и коксовых газов от сероводорода, очистка азотоводородной смеси от диоксида углерода при синтезе аммиака;
- обезвреживание производственных газовых выбросов. Сюда относятся очистка топочных газов от сернистого ангидрида, улавливание хлора, фтористых соединений и т.д.
В абсорбционных процессах (абсорбция, десорбция) участвуют две фазы - жидкая и газовая, происходит переход вещества из газовой в жидкую или наоборот, из жидкой в газовую при десорбции. Таким образом, абсорбционные процессы являются одним из видов процессов массопередачи.
На практике абсорбции подвергают на отдельные газы, а газовые смеси, состоящие из одной или нескольких компонентов, могут поглощаться в заметных количествах.
Жидкая фаза состоит из поглотителя и абсорбируемого компонента. Большей частью поглотителя представляет собой раствор активного компонента, вступающего в химическую реакцию с абсорбируемым компонентом, при этом вещество, в котором растворен активный компонент будем называть растворителем.
Инертный газ и поглотитель являются носителями компонента, соответственно в газовой и жидкой фазах. При физической абсорбции инертный газ и (поглотители компонента) поглотитель не расходуется и не участвует в процессе перехода из одной фазы в другую.
Протекание абсорбционных процессов характеризуется статикой и кинетикой процесса.
Статика абсорбции, то есть равновесие между жидкой и газовой фазами определяет состояние, которое устанавливается при весьма продолжительном соприкосновении фаз. Равновесие между фазами определяется термодинамическими свойствами компонента и поглотителя и зависит от свойства одной из фаз, температуры и давления.
Кинетика абсорбции, то есть скорость процесса массообмена, определяющий степень отклонения системы от равновесного состояния, свойства поглотителя, компонента и инертного газа, а так же способом соприкосновения фаз (устройством аппарата, и режимом его работы). В абсорбционных аппаратах движущая сила, как правило, измеряется по их длине и зависит от характера взаимного движения (противоток, прямоток, и т.д.). Прямолинейное (движение) поведение абсорбции может сочетаться с десорбцией. Если десорбцию не производят, поглотитель используется однократно. При этом в результате абсорбции получают готовый продукт, полупродукт, или если абсорбция производится с целью санитарной очистки газов, раствор (обезвреженный) сливают в канализацию.
Сочетание абсорбции с десорбцией позволяет многократно использовать поглотитель и выделять абсорбированный компонент в чистом виде. Для этого раствор после абсорбента отправляют на десорбцию, где происходит выделение компонента, а регенерированный (освобожденный от компонента) раствор вновь возвращают на абсорбцию. При такой схеме (круговой процесс) поглотитель не расходуется, если не считать малых, очень не значительных его потерь, все время циркулирует через систему абсорбер-десорбер-абсорбер. В некоторых случаях (при наличии дешевого поглотителя), в процессе десорбции отказываются, при этом поглотитель сбрасываю в канализацию, а в абсорбер подают свежий.
При абсорбционных
процессах массообмен происходит на
поверхности соприкосновения фаз. Поэтому
абсорбционные аппараты должны иметь
развитую поверхность соприкосновения
между газом и жидкостью, такие аппараты
называют абсорберами. Выбор типа
абсорбера определяется видом контакта
потоков газа и жидкости. Для создания
развитой поверхности контакта фаз, газ
пропускают через колону с тарелкой
(насадкой и т.д.). Тарельчатые абсорберы
представляют собой колонны, заполненные
тарелками, которые укладывают в один
или несколько слоев. Жидкость стекает
по тарелки в виде плитки, газ движется
противотоком. В качестве тарелок
используют тарелки: клапанные, ситчатые,
колпачковые, балластные и т.д. Выбор
тарелки (насадки)  как
ее химической и механической стойкостью,
так и характеристиками тарелок (насадок).
как
ее химической и механической стойкостью,
так и характеристиками тарелок (насадок).
Описание технологической схемы

 2.Расчет
основного аппарата
2.Расчет
основного аппарата
2.1.Масса поглощаемого вещества и расход поглотителя
2.1.1. Относительная массовая концентрация
Относительную массовую концентрацию газа найдем из соотношения:
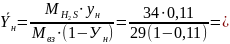 0,145
кг
H2S/кг
Вз;
0,145
кг
H2S/кг
Вз;
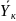 =
= 0,00725
кг H2S
/кгВз;
0,00725
кг H2S
/кгВз;
Относительную массовую концентрацию жидкости:
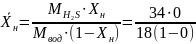 =0
кг H2S/кг
Н2О;
=0
кг H2S/кг
Н2О;
2.1.2. Построение равновесной линии
Выберем
ряд значений
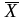 и подставим в уравнение, описывающее
равновесную линию (приложение 2), до
пересечения линии
и подставим в уравнение, описывающее
равновесную линию (приложение 2), до
пересечения линии
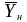 :
:

где Е=0,617 МПа – коэффициент Генри для газовой смеси[5]; Р=0,1 МПа - давление в абсорбере. Результаты расчета сведем в таблицу (табл. 1).
Таблица 1.
Зависимость содержания сероводорода в воздухе от его концентрации в воде
|
0,0000 |
0,0100 |
0,0200 |
0,0300 |
|
0,0000 |
0,0526 |
0,1052 |
0,1578 |
Уравнение, описывающее рабочую линию процесса абсорбции, имеет вид:
 .
.
где L, G – расходы чистого поглотителя и инертной части газа, кг/с.
Подставляя данные графика зависимости содержания сероводорода в воздухе и воде (приложение 2) в уравнение, находим конечную концентрацию сероводорода в воде:

где
 концентрация сероводорода в жидкости,
равновесная с воздушной смесью начального
состава.
концентрация сероводорода в жидкости,
равновесная с воздушной смесью начального
состава.

