
- •5. Переход от т.Карно к осн форм-ке 2го нач тд. Рав-во–нер-во Клаузиуса. Энтропия. Осн форм-ка 2го нач.
- •6 . Некот. След-я из 2го нач. Тд. Др. Форм-ки 2го нач. Как след-я из осн. Обоснование тд-шкалы темп-р.
- •7. 3Е нач. Тд. Осн. Форм-ка. Некот. Следствия из нее и эмпир. Обосн-е 3го нач. Недост-ть абс. Нуля.
- •1 0. Устойч-ть равнов. Сост-й. Крит-ии наличия равнов-я и его уст-ти в разл. Случаях. Огранич-я, налаг. На измен-я пар-ров устойчиво равнов. Тд-с-м. Положит-ть cv и βТ.
- •11. Равнов-е в 2-фазн. С-ме. Усл-я наличия равнов-я. Хим. Пот-л как пар-р, определяющий возм-ть и напр-е диффузии. Кривая равнов-я двух фаз.
- •15. Изуч-е поверхн. Явл-й с пом. Метода тд-ф-ций. Осн. Пар-ры, хар-щие явл-е пов. Натяж-я. Связь м/у ними.
- •16. Связь т-емк. Cp и cv д/простой с-мы. Ф-ла Майера.
- •17. Соотнош-е, связыв. Термич. И калорич. Ур-я сост-я.
7. 3Е нач. Тд. Осн. Форм-ка. Некот. Следствия из нее и эмпир. Обосн-е 3го нач. Недост-ть абс. Нуля.
Ф![]()
![]() орм-ка:
по мере прибл-я с-мы к абс. нулю энтр.
стрем к опред. пост. знач-ю, одному и тому
же д/всех с-м и не зав. от спос. охл-я.
Знач-е этой конст. важно в химич. превращ-х.
По предлож-ю Планка S0=0
(согл-е). 3е нач. ТД: →
S0=0,
но это не обязат. Энтр. всякой равнов.
с-мы стрем. к 0, а неравнов. – не обязат.
Эксп. базой 3го нач. ТД будут опыты,
показ. повед-е с-мы вблизи абс. нуля.
-
этот рез-т получ. незав. от спос. перехода,
если проц. равнов. δQ=CdT
C(T)
=a + bT + cT2
+ …
Очевидно, что а=0; С(0)=0. Иначе
интеграл расходится, а S
не м.б. равно ∞. Т.о. надо измерять
Т-емкости при низких Т. У диэл-ков: С(Т)
~ Т3, у металлов С(Т) ~ b*T+d*Т3.
Более сложно устан. повед-е др. физич.
вел-н. Все подоб. опыты дают рез-ты,
соглас. с форм-кой Нерста-Планка. Физ.
знач-е 3го нач. ТД менее сущ-но, чем
1го и 2го нач. Первые два
предст. собой фунд. з-ны прир., а 3е
нач. ТД есть лишь следствие квант. св-в
α-ч-ц. Его роль в Ф. огранич. тем, что оно
позв. выяснить повед-е ч-ц вблизи абс.
нуля. Тем не менее б/него обойтись нельзя.
орм-ка:
по мере прибл-я с-мы к абс. нулю энтр.
стрем к опред. пост. знач-ю, одному и тому
же д/всех с-м и не зав. от спос. охл-я.
Знач-е этой конст. важно в химич. превращ-х.
По предлож-ю Планка S0=0
(согл-е). 3е нач. ТД: →
S0=0,
но это не обязат. Энтр. всякой равнов.
с-мы стрем. к 0, а неравнов. – не обязат.
Эксп. базой 3го нач. ТД будут опыты,
показ. повед-е с-мы вблизи абс. нуля.
-
этот рез-т получ. незав. от спос. перехода,
если проц. равнов. δQ=CdT
C(T)
=a + bT + cT2
+ …
Очевидно, что а=0; С(0)=0. Иначе
интеграл расходится, а S
не м.б. равно ∞. Т.о. надо измерять
Т-емкости при низких Т. У диэл-ков: С(Т)
~ Т3, у металлов С(Т) ~ b*T+d*Т3.
Более сложно устан. повед-е др. физич.
вел-н. Все подоб. опыты дают рез-ты,
соглас. с форм-кой Нерста-Планка. Физ.
знач-е 3го нач. ТД менее сущ-но, чем
1го и 2го нач. Первые два
предст. собой фунд. з-ны прир., а 3е
нач. ТД есть лишь следствие квант. св-в
α-ч-ц. Его роль в Ф. огранич. тем, что оно
позв. выяснить повед-е ч-ц вблизи абс.
нуля. Тем не менее б/него обойтись нельзя.
С
![]() ущ-т
другие форм-ки, из них наиб. важная –
недост-ть абс. нуля. Рассм. прост. с-му,
кот охл. при расшир.
ущ-т
другие форм-ки, из них наиб. важная –
недост-ть абс. нуля. Рассм. прост. с-му,
кот охл. при расшир.
![]() dSV
≥ 0; CV>0
dSV
≥ 0; CV>0
![]() Способы
охл-я: 1) Контакт с более хол. телом; 2)
Расширение газа. Охладим до миним. т-ры
– дальнейшее невозм. Остается охл-ть
расшир-ем. Наиб. эфф. расш-е им. место при
адиаб. проц. δQ=0; dU=-δA;
dU=m/μCVdT;
V2>V1
(гр.) Из т.А надо попасть в нач. СК. Самый
эфф. проц. – адиаб. (dT=0).
А→В – адиаб. расшир-е (охл-е). При др.
спос. прридем в В’.[δQ=0,
dS=0]; [δQ>0,
dS>0]. dSравнов.>dSнеравнов.
Никаким спос. из А мы не м. попасть в нач.
СК. Т.о. расшир-ем достичь абс. нуля
невозм. Ни одно из окруж. тел не им. т-ры,
равной т-ре абс. нуля.
Способы
охл-я: 1) Контакт с более хол. телом; 2)
Расширение газа. Охладим до миним. т-ры
– дальнейшее невозм. Остается охл-ть
расшир-ем. Наиб. эфф. расш-е им. место при
адиаб. проц. δQ=0; dU=-δA;
dU=m/μCVdT;
V2>V1
(гр.) Из т.А надо попасть в нач. СК. Самый
эфф. проц. – адиаб. (dT=0).
А→В – адиаб. расшир-е (охл-е). При др.
спос. прридем в В’.[δQ=0,
dS=0]; [δQ>0,
dS>0]. dSравнов.>dSнеравнов.
Никаким спос. из А мы не м. попасть в нач.
СК. Т.о. расшир-ем достичь абс. нуля
невозм. Ни одно из окруж. тел не им. т-ры,
равной т-ре абс. нуля.
8. ТД-ф-ции. Понятие ТД-ф-ции. Опред-я осн. ТД-ф-ций. Разбор св-в своб эн.
Все иссл-я в обл. ТД опир., как правило, на 1е и 2е нач. ТД. 3е нач. им. огр. примен-ть ввиду его специфики (иссл-е с-м вблизи абс. нуля). dU=δQ- δA (I), dS≥ δQ/T (II) → δQ=TdS («=» при равнов. проц.) (ф-ла позв. расчит. получ. тепло при люб. проц.). dU≤TdS- δA. Данное соотн-е охват. одноврем. 1е и 2е нач. ТД. Оно имен. основным ТД-рав-вом–нер-вом. δA=pdV; dU≤TdS-pdV. S(V,T) – наличие таких зав-стей. постулир. в ТД. S=S(V,T) ↔ V=V(T,S) ↔ T=T(V,S). М. взять люб. пар-ры. Единств. огранич-е – число незав. перем. мен. не м. Число незав. перем. м.б. уменьш., если к.-то св-ва газов не изуч. В этом случае соотв-е пар-ры счит. пост. Сущ-т особо удобные физ. вел. – характеристич. ф-ции или ТД-потенциал. Требования: 1) Это д.б. ондознач. и аддит. ф-ция сост-я с-мы; 2) При некот. выборе незав. перем-х ее производные д. им. простой физ. смысл; 3) При некот. усл-х измен-е ф-ции опред. работу с-мы; 4) При некот. усл-х. ф-ция им. экстремум в сост-ии равнов-я. F=U-ST – своб эн., H=U+pV – энтальпия, G=U-ST+pV – ТД-потенциал Гиббса.
F=U-ST
– однознач. и адд. ф-ция сост-я с-мы.
Адд-сть своб. эн. есть следствие адд-сти
внут. эн. и энтр. Т-ра Т строго опред.
только д/равнов. с-м. В некот. частн. случ.
Т м. вывести и д/неравнов. с-м. Выясним,
какие перем. д/своб. эн. явл. естеств.
dF=dU-dST-SdT.
Д/прост. с-мы сущ. только две незав. перем.
dU=TdS-pdV;
dF=-Sdt-pdV.
![]()
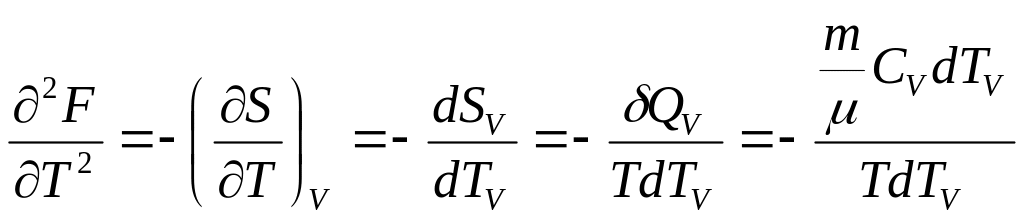

![]() 2я
ф-ла -пред. собой з-н прир., справедл.
д/люб. прост. с-мы – есть следствие 1го
и 2го нач. ТД, и вып. столь же
неукосн-но как и эти нач. dF=-Sdt-pdV.
T=const:
dFT=-pdVT=-δAT.
Измен-е своб. эн. осущ. за счет соверш-я
работы. F=U-ST; dF=dU-dST-sdT;
dU<TdS-pdV;dF<-SdT-pdV. T=const,
V=const: dF<0. В
изотермо-изохорич. с-ме б. происх. уменьш-е
своб. эн. Равов-ю соотв. Fmin.
ТД-потенциал Гиббса:
G=U+pV-ST;
dG=dU+pdV+Vdp-dST-SdT;
dU=TdS-pdV;
dG≤-SdT+Vdp
T=const,
p=const: dG ≤ 0, т.е. в сост-ии
равнов-я пот-л Гиббса им. минимум.
dG=-SdT+Vdp;
T,p:
2я
ф-ла -пред. собой з-н прир., справедл.
д/люб. прост. с-мы – есть следствие 1го
и 2го нач. ТД, и вып. столь же
неукосн-но как и эти нач. dF=-Sdt-pdV.
T=const:
dFT=-pdVT=-δAT.
Измен-е своб. эн. осущ. за счет соверш-я
работы. F=U-ST; dF=dU-dST-sdT;
dU<TdS-pdV;dF<-SdT-pdV. T=const,
V=const: dF<0. В
изотермо-изохорич. с-ме б. происх. уменьш-е
своб. эн. Равов-ю соотв. Fmin.
ТД-потенциал Гиббса:
G=U+pV-ST;
dG=dU+pdV+Vdp-dST-SdT;
dU=TdS-pdV;
dG≤-SdT+Vdp
T=const,
p=const: dG ≤ 0, т.е. в сост-ии
равнов-я пот-л Гиббса им. минимум.
dG=-SdT+Vdp;
T,p:
![]()
![]()
![]()
9. С-мы с перем. числом ч-ц. Обобщ-е осн. з-нов ТД на с-мы с перем. числом ч-ц. Хим. пот-л. Зав-сть ТД-ф-ций от числа ч-ц. Хим. пот-л как уд. ТД-пот-л Гиббса.
N
 1,
N2 … – число ч-ц кажд.
сорта (1, 2, …). N – ч-цы
одного сорта, хим. проц. нет. Постулат
равнов-я не изм. Т-обмен – спос. передачи
эн., кот. м. происх. при неизм. внеш. пар-рах
и числа ч-ц.
λ1=const,
N1=const
λ2=const, N2=const
f=f(T,
λ, N) – внут. пар-ры
f=f(T,
λ, N1, N2,
…)
Ч-ца, приходя в с-му, приносит эн.,
уходя – уносит. В ТД рассм. не направл.
дв-е ч-ц, а скрытое – диффузия. Измен-е
эн. происх. за счет:
dU=δQ-δA+dUN,
dUN=μdN
– диффузное измен-е эн.,
μ – хим. пот-л
с-мы, он равен порции эн., кот. в с-му
приносит одна ч-ца, если Т-обмен и работа
отсутствуют.
- опред-е энтр. не изм.,
второе нач. ост. прежним. Неизм. ост. и
3е нач.
dU ≤
TdS-pdV+μdN
– объед. ТД-рав-во–нер-во. dU=TdS-pdV+μdN
(3 степ. своб.). U(S,V,N).
μ=(∂U/∂N)S,V;
F=U-ST;
dF=
1,
N2 … – число ч-ц кажд.
сорта (1, 2, …). N – ч-цы
одного сорта, хим. проц. нет. Постулат
равнов-я не изм. Т-обмен – спос. передачи
эн., кот. м. происх. при неизм. внеш. пар-рах
и числа ч-ц.
λ1=const,
N1=const
λ2=const, N2=const
f=f(T,
λ, N) – внут. пар-ры
f=f(T,
λ, N1, N2,
…)
Ч-ца, приходя в с-му, приносит эн.,
уходя – уносит. В ТД рассм. не направл.
дв-е ч-ц, а скрытое – диффузия. Измен-е
эн. происх. за счет:
dU=δQ-δA+dUN,
dUN=μdN
– диффузное измен-е эн.,
μ – хим. пот-л
с-мы, он равен порции эн., кот. в с-му
приносит одна ч-ца, если Т-обмен и работа
отсутствуют.
- опред-е энтр. не изм.,
второе нач. ост. прежним. Неизм. ост. и
3е нач.
dU ≤
TdS-pdV+μdN
– объед. ТД-рав-во–нер-во. dU=TdS-pdV+μdN
(3 степ. своб.). U(S,V,N).
μ=(∂U/∂N)S,V;
F=U-ST;
dF=TdS-pdV+μdN-dST-dTS;
F(T,V,N);
μ=(∂F/∂N)T,V.
Ч-цы сохр-ся: м. уходить/прих., но вцелом
их число неизм. Как быть, если ч-цы м.
исчез./появл.? Надо обесп. ситуацию к.-то
ср-вом, кот. см. добиться з-на сохр. эн.
Что б. соотв. сост-ю равнов-я? Микроскопически
сохр-я ч-ц добиться нельзя (напр., распад
U238). Макроск-ки
добиться пост-ва ч-ц можно. Число появл-ся
д.б. равно числу исчез-х. Равнов-ю соотв.
именно такая ситуация. При этом в с-ме
б. вполне опред. число ч-ц. Из каких
сообр-й это число м. опред.? Сост-е равнов-я
отвеч. экстремуму ТД-ф-ции. При пост. Т
и V своб. эн. д.б. миним.:
Fmin.
(∂F/∂N)T,V=0.
G=U-ST+pV – ТД-пот-л
Гиббса.
dG=dU-SdT-TdS+dpV+pdV;
dG=-SdT+Vdp+μdN;
G(T,p,N); μ=(∂G/∂N)p,T.
Зав-сть ТД-ф-ций от числа ч-ц: Рассм. ф-цию внут. эн. U=U(S,V,N); U=Nφ(V/S) – прямая зав-сть (если удваив. с-ма, то удваив. и внут. эн.); F=F(T,V,N); F=Nψ(T,V/N); G=G(T,p,N); G=Nη(T,p); η=(∂G/∂N)p,T=μ; μ=G/N→μ=μ(T,p). Хим. пот-л как ф-ция давл-я и т-ры – есть удел. пот-л Гиббса из расчета на одну ч-цу.
