
- •5. Растворы полимеров
- •5.1. Термодинамическая характеристика раствора
- •5.2. Ограниченная растворимость. Фракционирование
- •5.3. Свойства растворов полимеров
- •5.3.3. Вязкость разбавленных растворов полимеров
- •5.4. Концентрированные растворы полимеров
- •5.5. Полиэлектролиты -
- •5.5.1. Коллапс полимерных сеток
- •5.5.2. Свойства растворов полиэлектролитов
5.2. Ограниченная растворимость. Фракционирование
Для растворов ВМС, как и для смесей низкомолекулярных веществ, характерно явление ограниченной растворимости. При достижении предельной растворимости полимеров в результате изменения температуры или концентрации раствор разделяется на 2 фазы. Возможны 2 случая: если полимер способен кристаллизоваться, то выделяется твердая кристаллическая фаза. Растворы аморфных полимеров разделяются на 2 жидкие фазы: разбавленную и концентрированную. Такое разделение называется жидкостным. На рис. 1 приведены типичные фазовые диаграммы состояния растворов полимеров в координатах температура - состав. Кривые, называемые бинодалью, разделяют каждую из диаграмм на 2 области. Область внутри бинодали соответствует двухфазному раствору. При определенных температурах ветви бинодали сходятся. Такие температуры называются критическими, в этих точках составы фаз равны. Максимум бинодали отвечает верхней критической температуре смешения (ВКТС), а минимум - нижней (НКТС).
Однако, если для смесей низкомолекулярных жидкостей ВКТС НКТС и диаграмма состояния раствора является замкнутой фигурой, близкой к овалу, то для растворов полимеров часто характерно НКТС ВКТС, что и приводит к необычному виду диаграммы (рис. 1).
В зависимости от температуры растворитель может быть плохим, идеальным и хорошим для одного и того же полимера. Ясно, например, что, в окрестности ВКТС, когда полимер выделяется из раствора, растворитель является плохим (А2 0). Это условие не может реализоваться в широком температурном интервале, поэтому -температура (А2 = 0) должна быть достаточно близка к ВКТС. Для систем с ВКТС и НКТС существуют две -температуры: та, что соответствует ВКТС, называется -температурой Флори, вторая - -температурой Роулинса. Последняя обычно близка к критической температуре растворителя.
Термодинамическим условием существования ВКТС и НКТС является соответственно ΔН 0, ΔS 0 и ΔН 0, ΔS 0.
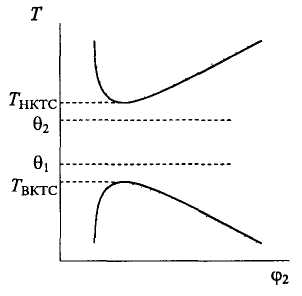
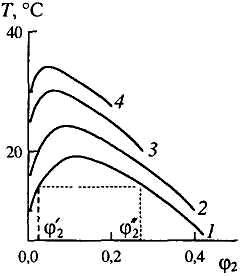
Рис. 1. Общий вид фазовых диаграмм растворов полимеров. |
Рис. 2. Раствор полистирола в циклогексане. Молярные массы М104: 1 – 4,4; 2 – 8,9; 3 – 25; 4 – 127. 2 и 2 - объемные доли полимера в менее и более концентрированных фазах. |
Из
рис. 2 видно, что растворимость полимера
зависит от его молекулярной массы. Это
широко используется на практике для
фракционирования – разделения
полидисперсного полимера по молекулярным
массам. Теория фракционирования
разработана Бренстедом и Шульцем.
Согласно
теории фракционирования:
![]() ,
где
,
где
φ2//,
φ2/
- объемные доли полимера в концентрированной
и разбавленной фазах, х
– параметр, пропорциональный молярной
массе полимера. Величина параметра σ
связана с термодинамическим качеством
растворителя, из которого выделяется
полимер. Из уравнения следует, что
отношение
![]() растет экспоненциально с увеличением
молекулярной массы, следовательно,
наиболее высокомолекулярные макромолекулы
будут находиться в концентрированной
фазе.
растет экспоненциально с увеличением
молекулярной массы, следовательно,
наиболее высокомолекулярные макромолекулы
будут находиться в концентрированной
фазе.
На практике фракционирование из раствора проводят, уменьшая термодинамическое качество растворителя, путем изменения температуры или добавлением осадителя. При этом фракции полимера выделяются в порядке уменьшения их средней молекулярной массы, но выделяющиеся фракции не являются монодисперсными.
