ВВЕДЕНИЕ. НАУЧНЫЕ НАПРАВЛЕНИЯ АНАТОМИИ ЧЕЛОВЕКА
Анато́мия челове́ка (от др.-греч. ἀνατομή — рассечение < др.-греч. ἀνά сверху и др.-греч. τομή, tomé — разрезание) — раздел биологии, изучающий морфологию человеческого организма, его систем и органов. Анатомия — наука о форме и строении органов, систем и организма в целом; часть морфологии. Анатомия человека изучает форму, строение, положение и взаимоотношение частей тела и органов с учетом возрастных, половых и индивидуальных особенностей. Форма и строение тела человека познаются как результат длительной эволюции его в филогенезе и онтогенезе. Сравнение строения тела человека и животных позволяет объяснить общность анатомических признаков и их различия, определяющие особое положение человека в природе.
Предметом изучения анатомии человека являются форма и строение, происхождение и развитие человеческого организма. Анатомия человека — одна из фундаментальных дисциплин в системе медицинского и биологического образования, тесно связанная с такими отделившимися от неё дисциплинами, как антропология и физиология человека, а также сравнительной анатомией, эволюционным учением и генетикой. Выделение анатомии человека из сферы анатомии живых организмов обусловлено не только наличием у человека характерных анатомических признаков, но и формированием у человека мышления, сознания и членораздельной речи.
Нормальная (систематическая) анатомия человека — раздел анатомии человека, изучающий строение «нормального», то есть здорового человека по системам органов, органам и тканям. Орган — часть тела определённой формы и конструкции, имеющая определённую локализацию в организме и выполняющая определённую функцию (функции). Каждый орган образован определёнными тканями, имеющими характерный клеточный состав. Органы, которые объединены анатомически и функционально, имеющие единое происхождение и общий план строения, составляют систему органов.
Разделами нормальной (систематической) анатомии человека являются: остеология — учение о костях, синдесмология — учение о соединениях частей скелета, миология — учение о мышцах, спланхнология — учение о внутренних органах пищеварительной, дыхательной и мочеполовой систем, ангиология — учение о кровеносной и лимфатической системах, анатомия нервной системы (неврология) — учение о центральной и периферической нервной системах, эстезиология — учение об органах чувств.[2]
Патологическая анатомия — научно-прикладная дисциплина, изучающая патологические процессы и болезни с помощью научного, главным образом микроскопического, исследования изменений, возникающих в клетках и тканях организма, органах и системах органов. Основателем современной патологической анатомии считается Рудольф Вирхов — немецкий исследователь, создавший учение о целлюлярной (клеточной)патологии. Помимо сущности микроскопических изменений в тканях, современная патологическая анатомия включает в себя изучение причин (этиологию), механизмов развития (патогенез), а также осложнений и исходов заболеваний. Она занимается также исследованием причин и механизмов смерти (танатогенез) при разных болезнях, изменчивостью заболеваний (патоморфоз) и патологией, вызываемой лечением (ятрогенная патология, ятрогения).
Топографическая анатомия (хирургическая анатомия) — научно-прикладная дисциплина, раздел анатомии, изучающий послойное строение анатомических областей, взаиморасположение (синтопию) органов, их проекцию на кожу (голотопию), отношение к скелету (скелетотопию), кровоснабжение, иннервацию и лимфоотток в условиях нормы и патологии, с учётом возрастных, половых и конституциональных особенностей организма.
Топографическая анатомия изучает строение человеческого организма по условно выделяемым известным частям тела (голова, шея, туловище и конечности), каждая из которых дифференцируется на относительно небольшие анатомические области.
Методы анатомических исследований.
Все анатомические методы можно условно разделить на макроскопические, которые изучают весь организм целиком, системы органов, отдельные органы или их части, и на микроскопические, объектом которых являются ткани и клетки организма человека и клеточные органеллы. В последнем случае анатомические методы смыкаются с методами таких наук, как гистология (наука о тканях) и цитология (наука о клетке).
В свою очередь, макроскопические и микроскопические исследования состоят из набора различных методических приемов, позволяющих изучать различные аспекты морфологических образований в нервной системе в целом, в отдельных участках нервной ткани или даже в отдельном нейроне. Соответственно, можно выделить набор макроскопических и микроскопических методов исследования морфологии ЦНС.
Основные
группы методов исследования морфологии
ЦНС:

Макроскопические
методы исследования нервной системы:
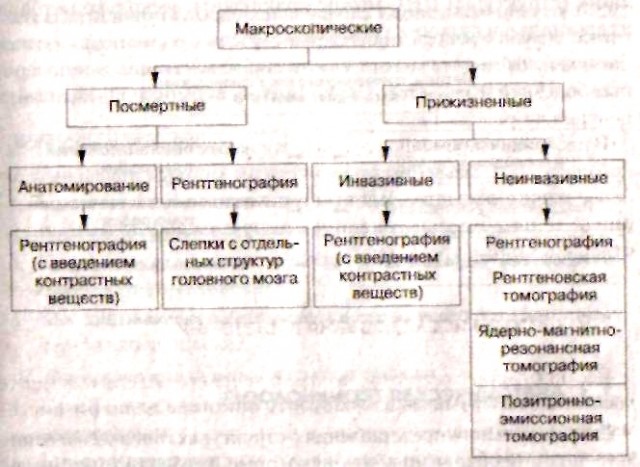
Рентгеногра́фия (англ. projection radiography, plain film radiography, roentgenography,) — исследование внутренней структуры объектов, которые проецируются при помощи рентгеновских лучей на специальную плёнку или бумагу. Наиболее часто термин относится к медицинскому неинвазивному исследованию, основанному на получении суммационного проекционного изображения анатомических структур организма посредством прохождения через них рентгеновских лучей и регистрации степени ослабления рентгеновского излучения.
Компью́терная томогра́фия — метод неразрушающего послойного исследования внутренней структуры объекта, был предложен в 1972 году Годфри Хаунсфилдом и Алланом Кормаком, удостоенными за эту разработку Нобелевской премии. Метод основан на измерении и сложной компьютерной обработке разности ослабления рентгеновского излучения различными по плотности тканями.
Компьютерная томография (КТ) — в широком смысле, синоним термина томография (так как все современные томографические методы реализуются с помощью компьютерной техники); в узком смысле (в котором употребляется значительно чаще), синоним термина рентгеновская компьютерная томография, так как именно этот метод положил начало современной томографии.
Рентгеновская компьютерная томография — томографический метод исследования внутренних органов человека с использованием рентгеновского излучения.Магнитно-резонансная томография
ЯМР – общепризнанное сокращение словосочетания «ядерный магнитный резонанс». ЯМР – томография (или МРТ) – это относительно новый вид получения изображения внутренних органов, который начал входить в медицинскую практику в 80-х годах прошлого столетия.
ЯМР-томография принципиально отличается от рентгеновской компьютерной томографии, но тоже относится к лучевой диагностике.
Позитро́нно-эмиссио́нная томогра́фия (позитронная эмиссионная томография, сокращ. ПЭТ), она же двухфотонная эмиссионная томография — радионуклидный томографический метод исследования внутренних органов человека или животного. Метод основан на регистрации пары гамма-квантов, возникающих при аннигиляции позитронов. Позитроны возникают при позитронном бета-распаде радионуклида, входящего в состав радиофармпрепарата, который вводится в организм перед исследованием.
. В основе этого метода лежит возможность при помощи специального детектирующего оборудования (ПЭТ-сканера) отслеживать распределение в организме биологически активных соединений, меченных позитрон-излучающими радиоизотопами. Потенциал ПЭТ в значительной степени определяется арсеналом доступных меченых соединений — радиофармпрепаратов (РФП). Именно выбор подходящего РФП позволяет изучать с помощью ПЭТ такие разные процессы, как метаболизм, транспорт веществ, лиганд-рецепторные взаимодействия, экспрессию генов и т. д. Использование РФП, относящихся к различным классам биологически активных соединений, делает ПЭТ достаточно универсальным инструментом современной медицины. Поэтому разработка новых РФП и эффективных методов синтеза уже зарекомендовавших себя препаратов в настоящее время становится ключевым этапом в развитии метода ПЭТ.
На сегодняшний день в ПЭТ в основном применяются позитрон-излучающие изотопы элементов второго периода периодической системы:
углерод-11 (T½= 20,4 мин.)
азот-13 (T½=9,96 мин.)
кислород-15 (T½=2,03 мин.)
фтор-18 (T½=109,8 мин.)
Фтор-18 обладает оптимальными характеристиками для использования в ПЭТ: наибольшим периодом полураспада и наименьшей энергией излучения. С одной стороны, относительно небольшой период полураспада фтора-18 позволяет получать ПЭТ-изображения высокой контрастности при низкой дозовой нагрузке на пациентов. Низкая энергия позитронного излучения обеспечивает высокое пространственное разрешение ПЭТ-изображений. С другой стороны, период полураспада фтора-18 достаточно велик, чтобы обеспечить возможность транспортировки РФП на основе фтора-18 из централизованного места производства в клиники и институты, имеющие ПЭТ-сканеры (т. н. концепция сателлитов), а также расширить временны́е границы ПЭТ-исследований и синтеза РФП.
Микроскопические методы весьма разнообразны. К ним относятся методы световой и электронной микроскопии, гистохимии, иммугистохимии, радиоавтографии, методы прижизненных исследований клеток и тканей. Эта группа методов подробно описывается в пособиях по гистологии и цитологии.
Микроскопические
методы исследования нервной системы:
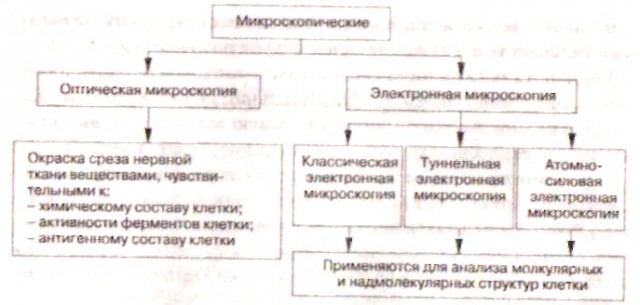
Электронная микроскопия позволяет с помощью электронного микроскопа исследовать микроструктуру тел при увеличениях до многих сотен тысяч раз (вплоть до атомно-молекулярного уровня), изучить их локальный состав и локализованные на поверхностях или в микрообъёмах тел электрические и магнитные поля (микрополя).
Сканирующий туннельный микроскоп (СТМ, англ. STM — scanning tunneling microscope) — вариант сканирующего зондового микроскопа, предназначенный для измерения рельефа проводящих поверхностей с высоким пространственным разрешением. В СТМ острая металлическая игла подводится к образцу на расстояние нескольких ангстрем. При подаче на иглу относительно образца небольшого потенциала возникает туннельный ток. Величина этого тока экспоненциально зависит от расстояния образец-игла. Типичные значения 1—1000 пА при расстояниях около 1 Å. Сканирующий туннельный микроскоп первый из класса сканирующих зондовых микроскопов; атомно-силовой и сканирующий ближнепольный оптический микроскопы были разработаны позднее.
В процессе сканирования игла движется вдоль поверхности образца, туннельный ток поддерживается стабильным за счёт действия обратной связи, и показания следящей системы меняются в зависимости от топографии поверхности. Такие изменения фиксируются, и на их основе строится карта высот. Другая методика предполагает движение иглы на фиксированной высоте над поверхностью образца. В этом случае фиксируется изменение величины туннельного тока и на основе данной информации идет построение топографии поверхности.
Таким образом сканирующий туннельный микроскоп (СТМ) включает следующие элементы:
зонд (иглу),
систему перемещения зонда относительно образца по 2-м (X-Y) или 3-м (X-Y-Z) координатам,
регистрирующую систему.
Регистрирующая система фиксирует значение функции, зависящей от величины тока между иглой и образцом, либо перемещения иглы по оси Z. Обычно регистрируемое значение обрабатывается системой отрицательной обратной связи, которая управляет положением образца или зонда по одной из координат (Z). В качестве системы обратной связи чаще всего используется ПИД-регулятор. Ограничения на использование метода накладываются, во-первых, условием проводимости образца (поверхностное сопротивление должно быть не больше 20 МОм/см²), во-вторых, условием «глубина канавки должна быть меньше её ширины», потому что в противном случае может наблюдаться туннелирование с боковых поверхностей. Но это только основные ограничения. На самом деле их намного больше. Например, технология заточки иглы не может гарантировать одного острия на конце иглы, а это может приводить к параллельному сканированию двух разновысотных участков. Кроме ситуации глубокого вакуума, во всех остальных случаях мы имеем на поверхности осаждённые из воздуха частицы, газы и т. д. Технология грубого сближения также оказывает колоссальное влияние на действительность полученных результатов. Если при подводе иглы к образцу мы не смогли избежать удара иглы о поверхность, то считать иглу состоящей из одного атома на кончике пирамиды будет большим преувеличением.
Атомно-силовая микроскопия — один из видов сканирующей зондовой микроскопии, основанный на ван-дер-ваальсовских взаимодействиях зонда с поверхностью образца. Принцип действия атомного силового микроскопа (АСМ) основан на использовании сил атомных связей, действующих между атомами вещества. На малых расстояниях между двумя атомами действуют силы отталкивания, а на больших – силы притяжения. Совершенно аналогичные силы действуют и между любыми сближающимися телами. В сканирующем атомном силовом микроскопе такими телами служат исследуемая поверхность и скользящее над нею острие. Обычно в приборе в качестве зонда используется игла с площадью острия в один или несколько атомов, закрепленная на кантилевере, который плавно скользит над поверхностью образца. На выступающем конце кантилевера (над шипом) расположена зеркальная площадка, на которую падает и от которой отражается луч лазера. Когда зонд опускается и поднимается на неровностях поверхности, отраженный луч отклоняется, и это отклонение регистрируется фотодетектором, а сила, с которой шип притягивается к близлежащим атомам – пьезодатчиком. Данные фотодетектора и пьезодатчика используются в системе обратной связи, которая может обеспечивать, например, постоянную величину силу взаимодействия между микрозондом и поверхностью образца. В результате, можно строить объёмный рельеф поверхности образца в режиме реального времени. Разрешающая способность данного метода составляет примерно 0,1-1 нм по горизонтали и 0,01 нм по вертикали. Так как задачей анатомического исследования (с точки зрения психологии) является выявление связей анатомических структур с психическими процессами, то к методам исследования морфологии (структуры) ЦНС можно подключить несколько методов из арсенала физиологии (рис.).
Общие методы для физиологии и анатомии
ЦНС:
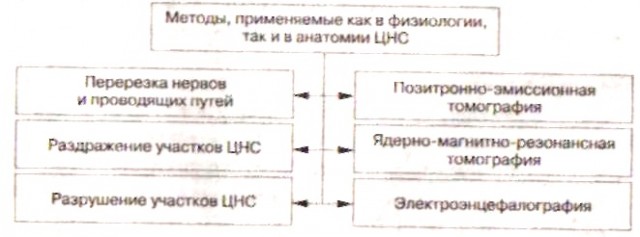
Выделяют методы описательные, сравнительно-анатомические и экспериментальные. Наиболее старым является метод препарирования или рассечения. От названия этого метода появился термин "анатомия" (от греч. anatomia – рассекаю, расчленяю). С его помощью изготавливаются анатомические макропрепараты (например, мышц или нервов руки и др.).
Метод инъекции или наливки применяется при приготовлении препаратов для выявления и изучения строения полых структур, например, сосудистой системы органа. Его можно применять совместно с методом коррозии, когда орган после наливки полых структур окрашенной массой погружают в кислоту или щелочь для растворения всех остальных тканей. В результате остается только цветной слепок сосудов органа.
Наибольшую ценность представляют методы, позволяющие исследовать строение органов живого человека при различных функциональных состояниях. Таков метод компьютерной томографии. С помощью специального аппарата получают снимки органа, или их группы, например, головного мозга или органов брюшной полости живого человека. Таким образом можно оценить полноценность кровоснабжения или целостность органов (при травмах). Широко используется в медицине метод рентгеноскопии, например, при исследовании костей скелета, органов желудочно-кишечного тракта, почек и т.д.
Все виды морфологических исследований сопровождаются количественной обработкой данных, проводимой с помощью специальных устройств.
Некоторые специальные термины, принятые в анатомии. Анатомия, как и любая другая наука, использует свою терминологию (номенклатуру). Терминология имеет большое значение для правильного толкования строения любой структуры при ее изучении и описании. Международная анатомическая номенклатура была принята в г. Базеле (Швейцария) в 1885 г. (BNA). Она изменялась и дополнялась в Париже в 1955 г. (PNA), Ленинграде (1970), Ташкенте (1974) и Токио (1975). В анатомии традиционно используются латинские термины.
Для точного представления о топографии органа или его отдела условно выделяют различные плоскости сечения тела человека
Так, сагиттальная плоскость (от лат. sagitta – стрела) проходит через середину тела, рассекая его на правую и левую половины.
Фронтальная плоскость (от лат./rons – лоб) параллельна плоскости лба и делит тело на брюшную или вентральную (от лат. venter – живот), и спинную, или дорсальную (от лат. dorsum – спина), половины. Третья плоскость – перпендикулярная обеим предыдущим – горизонтальная. Она рассекает тело на поперечные отрезки – сегменты.
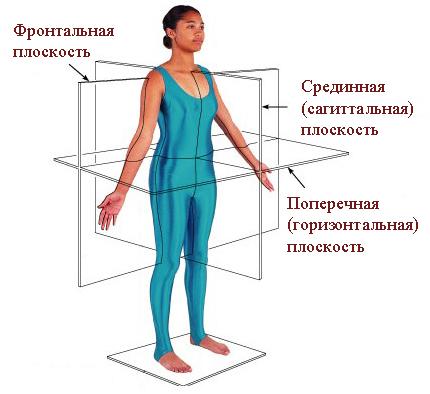
В анатомии приняты следующие обозначения: anterior – передний, posterior – задний, inferior – нижний, superior – верхний, dexter – правый, sinister – левый и т.д. Участки органов, обращенные к срединной плоскости называются медиальными, к периферии – латеральными.
Положение органов ближе к головному концу тела называется краниальным (cranium – череп) или оральным (or – рот), ближе к заднему концу – каудальным (cauda – хвост). На конечностях ближайшую к туловищу часть называют проксимальной, удаленную от него – дистальной (distantio – расстояние).
«Афферентный» – приносящий (употребляется применительно к нейрону, по которому импульсы поступают в ЦНС);
«Эфферентный» – выносящий (употребляется применительно к нейрону, по которому импульсы покидают ЦНС)
Структура и функции эукариотических клеток
Открытие клетки
Открытие клетки принадлежит английскому ученому Р.Гуку, который в 1665 г. в сконструированном им микроскопе впервые рассматривал тонкий срез пробки. На срезе четко просматривалась структура, похожая на пчелиные соты, построенные из ячеек. Элементы тонкого слоя пробки Р.Гук назвал латинскими словом се11ula, что означает ячейка, или клетка. Значительный вклад в изучение клетки внес А. Левенгук, открывший в 1674 г. одноклеточные организмы, в том числе бактерии. В 1831 г. английский ботаник Р.Броун обнаружил в клетках ядро. Это открытие послужило важной предпосылкой для установления сходства между клетками растений и животных. В 1838-1839 гг. немецкие ученые ботаник М.Шлейден и зоолог Т.Шванн обобщили имевшиеся знания о клетке в единую теорию, утверждавшую, что клетки, содержащие ядра, представляют собой структурную и функциональную основу всех живых существ. Клеточная теория получила дальнейшее развитие в трудах немецкого ученого Р.Вирхова, внесшего в 1858 г. существенное дополнение: клетка может возникнут только из предшествующей клетки в результате ее деления. Кроме того, русский ученый К. Бэр открыл яйцеклетку млекопитающих и установил, что все многоклеточные организмы начинают свое развитие из одной клетки. Это открытие показало, что клетка ? не только единица строения, но и единица развития всех живых организмов. Идея о том, что все организмы построены из клеток стала одним из наиболее важных теоретических достижений в истории биологии, поскольку создала единую основу для изучения всех живых существ. На клеточном уровне даже наиболее отдаленные виды весьма схожи по строению и биохимическим свойствам, что указывает на общность их происхождения и эволюционного развития. Дальнейшие успехи науки о клетке связаны с усовершенствованием приборов и развитием физических и химических методов исследования. Комплексное использование электронного микроскопирования и микрохимических методов анализа позволило в мельчайших деталях изучить строение и химический состав всех структурных компонентов клетки ? ядра, митохондрий, хлоропластов, рибосом и др. Кроме того, это дало возможность доказать неразрывную связь между структурой клетки и ее функцией. С самого начала развития представлений о клеточном строении возникал вопрос о соотношении клетки и целого организма. С одной стороны, предполагалось, что жизнедеятельность организма представляет собой сумму функционирующих клеток, с другой ? утверждалось, что их существование является качественно отличным и обусловлено ?жизненной силой?. Благодаря открытию митотического деления и молекулярной биологии сформировали современные представления о структуре и функциях клетки, о клеточном уровне в иерархии живой природы.
Современная клеточная теория включает следующие положения: 1) клетка как элементарная живая структура, способная к самообновлению, саморегуляции и самовоспроизведению, лежит в основе строения и развития живых организмов; 2) клеткам присуще мембранное строение; 3) размножение клеток происходит путем их деления и каждая новая клетка образуется в результате деления исходной (материнской) клетки; 4) у всех организмов клетки построены по единому принципу, сходны по химическому составу и характеру химических реакций, основным явлениям жизнедеятельности и обмену веществ. Цитология бурно развивается и в наши дни, благодаря чему мы имеем достаточно точные представления о химическом составе, строении и функциях всех частей тела клетки.
Организация органелл
Клетки, образующие ткани животных и растений, значительно различаются по
форме, размерам и внутреннему строению. Однако все они обнаруживают сходство
в главных чертах процессов жизнедеятельности, обмена веществ, в
раздражимости, росте, развитии, способности к изменчивости.
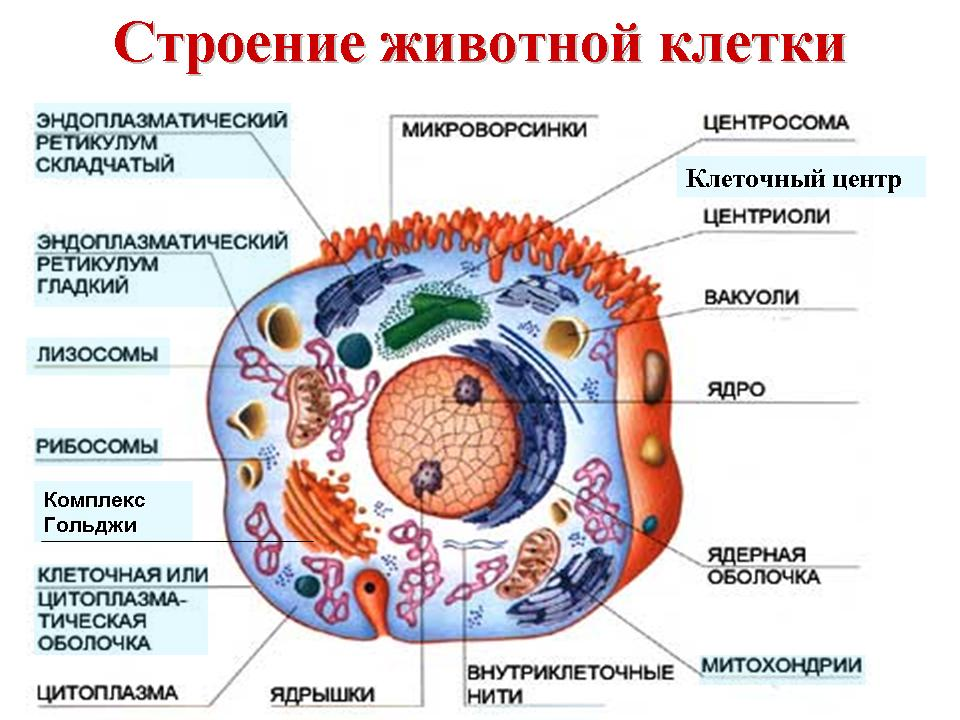
Клетки всех типов содержат два основных компонента, тесно связанных между собой,
— цитоплазму и ядро. Ядро отделено от цитоплазмы пористой мембраной и содержит
ядерный сок, хроматин и ядрышко. Полужидкая цитоплазма заполняет всю клетку и
пронизана многочисленными канальцами. Снаружи она покрыта цитоплазматической
мембраной. В ней имеются специализированные структуры-органоиды,
присутствующие в клетке постоянно, и временные образования — включения.
Мембранные органоиды: наружная цитоплазматическая мембрана (HЦM),
эндоплазматическая сеть (ЭПС), аппарат Гольджи, лизосомы, митохондрии и
пластиды. В основе строения всех мембранных органоидов лежит биологическая
мембрана. Все мембраны имеют принципиально единый план строения и состоят из
двойного слоя фосфолипидов, в который с различных сторон ива разную глубину
погружены белковые молекулы. Мембраны органоидов отличаются друг от друга лишь
наборами входящих в них белков.
Цитоплазматическая мембрана. У всех клеток растений, многоклеточных
животных, у простейших и бактерий клеточная мембрана трехслойна: наружный и
внутренний слои состоят из молекул белков, средний — из молекул липидов. Она
ограничивает цитоплазму от внешней среды, окружает все органоиды клетки и
представляет собой универсальную биологическую структуру. В некоторых клетках
наружная оболочка образована несколькими мембранами, плотно прилегающими друг к
другу. В таких случаях клеточная оболочка становится плотной и упругой и
позволяет сохранить форму клетки, как, например, у эвглены и инфузории
туфельки. У большинства растительных клеток, помимо мембраны, снаружи имеется
еще толстая целлюлозная оболочка — клеточная стенка. Она хорошо
различима в обычном световом микроскопе и выполняет опорную функцию за счет
жесткого наружного слоя, придающего клеткам четкую форму.
На поверхности клеток мембрана образует удлиненные выросты — микроворсинки,
складки, впячивания и выпячивания, что во много раз увеличивает всасывающую или
выделительную поверхность. С помощью мембранных выростов клетки соединяются
друг с другом в тканях и органах многоклеточных организмов, на складках мембран
располагаются разнообразные ферменты, участвующие в обмене веществ.
Отграничивая клетку от окружающей среды, мембрана регулирует направление
диффузии веществ и одновременно осуществляет активный перенос их внутрь клетки
(накопление) или наружу (выделение). За счет этих свойств мембраны концентрация
ионов калия, кальция, магния, фосфора в цитоплазме выше, а концентрация натрия
и хлора ниже, чем в окружающей среде. Через поры наружной мембраны из внешней
среды внутрь клетки проникают ионы, вода и мелкие молекулы других веществ.
Проникновение в клетку относительно крупных твердых частиц осуществляется путем
фагоцитоза (от греч. “фаго” — пожираю, “питое” — клетка).
При этом наружная мембрана в месте контакта с частицей прогибается
внутрь клетки, увлекая частицу в глубь цитоплазмы, где она подвергается
ферментативному расщеплению. Аналогичным путем в клетку попадают и капли жидких
веществ; их поглощение называется пиноцитозом (от греч. “пино” — пью,
“цитос” — клетка). Наружная клеточная мембрана выполняет и другие важные
биологические функции.
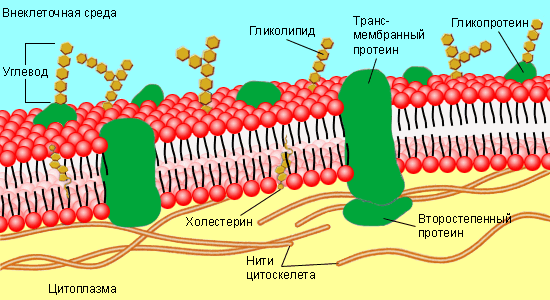
Важной проблемой является транспорт веществ через плазматические мембраны. Он необходим для доставки питательных веществ в клетку, вывода токсичных отходов, создания градиентов для поддержания нервной и мышечной активности. Существуют следующие механизмы транспорта веществ через мембрану:
диффузия (газы, жирорастворимые молекулы проникают прямо через плазматическую мембрану); при облегчённой диффузии растворимое в воде вещество проходит через мембрану по особому каналу, создаваемому какой-либо специфической молекулой;
осмос (диффузия воды через полунепроницаемые мембраны);
активный транспорт (перенос молекул из области с меньшей концентрацией в область с большей, например, посредством специальных транспортных белков, требует затраты энергии АТФ);
при эндоцитозе мембрана образует впячивания, которые затем трансформируются в пузырьки или вакуоли. Различают фагоцитоз – поглощение твёрдых частиц (например, лейкоцитами крови) – и пиноцитоз – поглощение жидкостей;
экзоцитоз – процесс, обратный эндоцитозу; из клеток выводятся непереварившиеся остатки твёрдых частиц и жидкий секрет.
Первые два процесса в отличие от остальных не требуют дополнительной энергии.
Над плазматической мембраной клетки могут располагаться надмембранные структуры. Их строение является влажным классификационным признаком. У животных это гликокаликс (белково-углеводный комплекс), у растений, грибов и бактерий – клеточная стенка. В состав клеточной стенки растений входит целлюлоза, грибов – хитин, бактерий – белково-полисахаридный комплекс муреин.
Цитоплазма на 85 % состоит из воды, на 10 % — из белков, остальной объем
приходится на долю липидов, углеводов, нуклеиновых кислот и минеральных
соединений; все эти вещества образуют коллоидный раствор, близкий по
консистенции глицерину. Коллоидное вещество клетки в зависимости от ее
физиологического состояния и характера воздействия внешней среды имеет свойства
и жидкости, и упругого, более плотного тела.
Цитоплазма пронизана каналами различной формы и величины, которые получили название эндоплазматической сети. Их стенки представляют собой мембраны, тесно контактирующие со всеми органоидами клетки и составляющие вместе с ними единую
функционально-структурную систему для осуществления обмена веществ и энергии и
перемещения веществ внутри клетки.
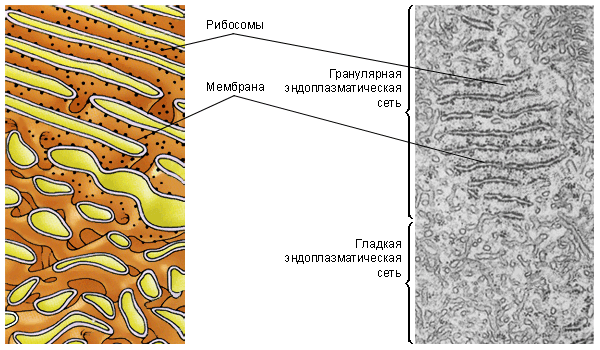
В стенках канальцев располагаются мельчайшие зернышки—гранулы, называемые
рибосомами. Такая сеть канальцев называется гранулярной. Рибосомы могут
располагаться на поверхности канальцев разрозненно или образуют комплексы из
пяти-семи и более рибосом, называемые полисомами. Другие канальцы
гранул не содержат, они составляют гладкую эндоплазматическую сеть. На стенках
располагаются ферменты, участвующие в синтезе жиров и углеводов.
Внутренняя полость канальцев заполнена продуктами жизнедеятельности клетки.
Внутриклеточные канальцы, образуя сложную ветвящуюся систему, регулируют
перемещение и концентрацию веществ, разделяют различные молекулы органических
веществ и этапы их, синтеза. На внутренней и внешней поверхности мембран,
богатых ферментами, осуществляется синтез белков, жиров и углеводов, которые
либо используются в обмене веществ, либо накапливаются в цитоплазме в
качестве включений, либо выводятся наружу.
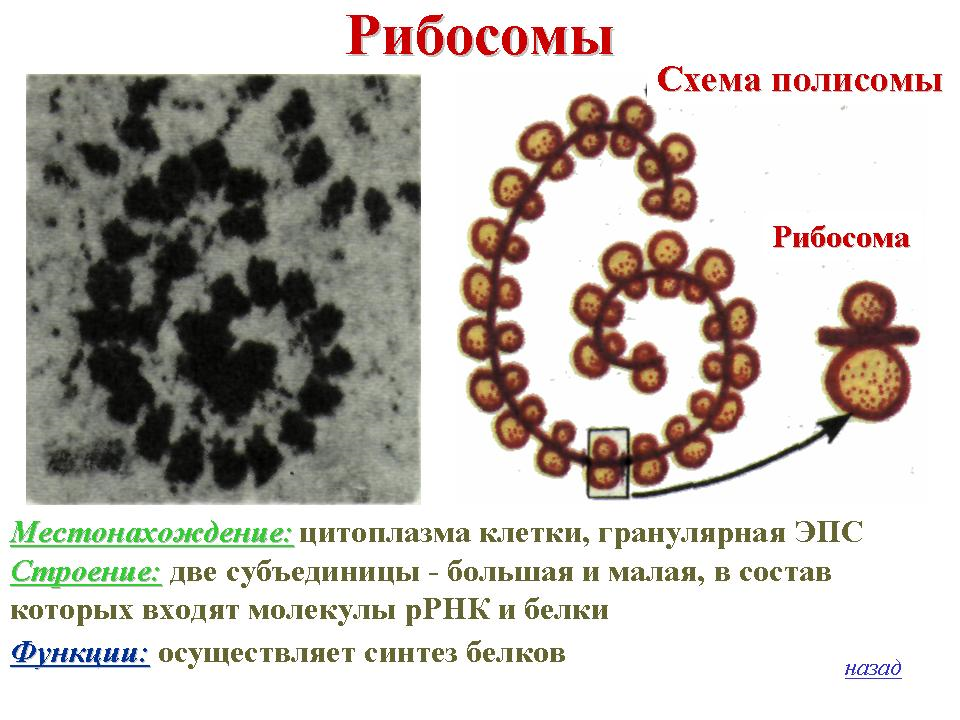
Рибосомы встречаются во всех типах клеток — от бактерий до клеток
многоклеточных организмов. Это округлые тельца, состоящие из рибонуклеиновой
кислоты (РНК) и белков почти в равном соотношении. В их состав непременно
входит магний, присутствие которого поддерживает структуру рибосом. Рибосомы
могут быть связаны с мембранами эндоплазматической сети, с наружной клеточной
мембраной или свободно лежать в цитоплазме. В них осуществляется синтез белков.
Рибосомы кроме цитоплазмы встречаются в ядре клетки. Они образуются в ядрышке и
затем поступают в цитоплазму.
Комплекс Гольджи в растительных клетках имеет вид отдельных телец,
окруженных мембранами. В животных клетках этот органоид представлен цистернами,
канальцами и пузырьками. В мембранные трубки комплекса Гольджи из канальцев
эндоплазматической сети поступают продукты секреции клетки, где они химически
перестраиваются, уплотняются, а затем переходят в цитоплазму и либо
используются самой клеткой, либо выводятся из нее. В цистернах комплекса
Гольджи происходит синтез полисахаридов и их объединение с белками, в
результате чего образуются гликопротеиды.

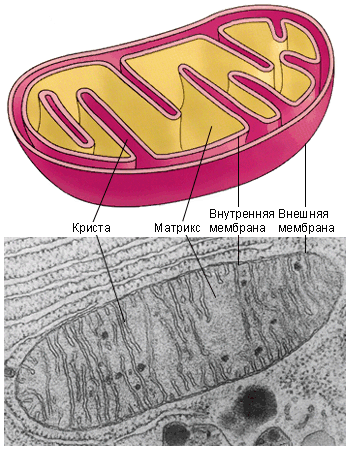
Митохондрии — небольшие тельца палочковидной формы, ограниченные двумя
мембранами. От внутренней мембраны митохондрии отходят многочисленные складки —
кристы, на их стенках располагаются разнообразные ферменты, с помощью которых
осуществляется синтез высокоэнергетического вещества — аденозинтрифосфорной
кислоты (АТФ). В зависимости от активности клетки и внешних воздействий митохондрии могут перемещаться, изменять свои размеры, форму. В митохондриях найдены рибосомы, фосфолипиды, РНК и ДНК. С присутствием ДНК в митохондриях связывают способность этих органоидов к размножению путем образования перетяжки или почкованием в период деления клетки, а также синтез части митохондриальных белков.
Лизосомы - мелкие овальные образования, ограниченные мембраной и
рассеянные по всей цитоплазме. Встречаются во всех клетках животных и растений.
Они возникают в расширениях эндоплазматической сети и в комплексе Гольджи,
здесь заполняются гидролитическими ферментами, а затем обособляются и поступают
в цитоплазму. В обычных" условиях лизосомы переваривают частицы, попадающие в
клетку путем фагоцитоза, и органоиды отмирающих клеток. Продукты лизиса
выводятся через мембрану лизосомы в цитоплазму, где они включаются в состав
новых молекул. При разрыве лизоеомной мембраны ферменты поступают в цитоплазму
и переваривают ее содержимое, вызывая гибель клетки.

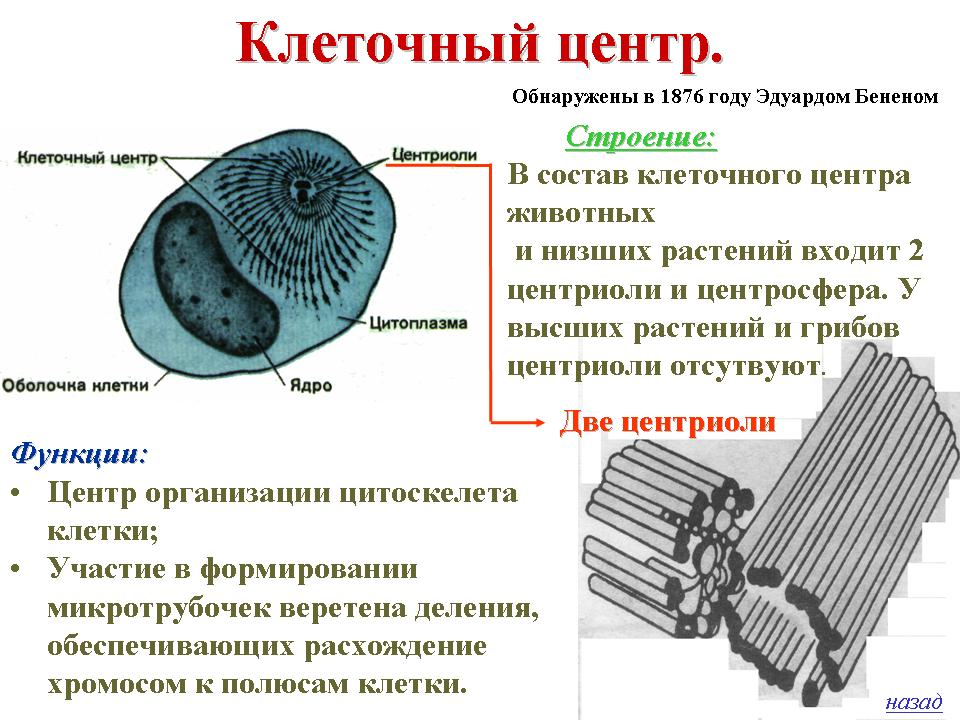
Клеточный центр, или центросома, играет важную роль при делении, клетки и
состоит из двух центриолей. Он встречается у всех клеток животных и
растений, кроме цветковых, низших грибов и некоторых, простейших. Центриоли в
делящихся клетках принимают участие в формировании веретена деления и
располагаются на его полюсах. В делящейся клетке первым делится клеточный
центр, одновременно образуется ахроматиновое веретено, ориентирующее хромосомы
при расхождении их к полюсам. В дочерние клетки отходит по одной центриоле.
У многих растительных и животных клеток имеются органоиды специального
назначения: реснички, выполняющие функцию движения (инфузории,
клетки дыхательных путей), жгутики (простейшие одноклеточные, мужские
половые клетки у животных и растений и др.).
Включения - временные элементы, возникающие в клетке на определенной
стадии ее жизнедеятельности в результате синтетической функции. Они либо
используются, либо выводятся из клетки. Включениями являются также запасные
питательные вещества: в растительных клетках—крахмал, капельки жира, белки,
эфирные масла, многие органические кислоты, соли органических и неорганических
кислот; в животных клетках - гликоген (в клетках печени и мышцах), капли жира
(в подкожной клетчатке); Некоторые включения накапливаются в клетках как
отбросы — в виде кристаллов, пигментов и др.
Вакуоли — это полости, ограниченные мембраной; хорошо выражены в клетках
растений и имеются у простейших. Возникают в разных участках расширений
эндоплазматической сети. И постепенно отделяются от нее. Вакуоли поддерживают
тургорное давление, в них сосредоточен клеточный или вакуолярный сок, молекулы
которого определяют его осмотическую концентрацию. Считается, что
первоначальные продукты синтеза - растворимые углеводы, белки, пектины и др. —
накапливаются в цистернах эндоплазматической сети. Эти скопления и представляют
собой зачатки будущих вакуолей.
Цитоскелет. Одной из отличительных особенностей
эукариотической клетки является развитие в ее цитоплазме скелетных образований
в виде микротрубочек и пучков белковых волокон. Элементы цитоскелета тесно
связаны с наружной цитоплазматической мембраной и ядерной оболочкой, образуют
сложные переплетения в цитоплазме. Опорные элемеиты цитоплазмы определяют форму
клетки, обеспечивают движение внутриклеточных структур и перемещение всей
клетки.
Ядро клетки играет основную роль в ее жизнедеятельности, с его удалением
клетка прекращает свои функции и гибнет. В большинстве животных клеток одно
ядро, но встречаются и многоядерные клетки (печень и мышцы человека, грибы,
инфузории, зеленые водоросли). Эритроциты млекопитающих развиваются из
клеток-предшественников, содержащих ядро, но зрелые эритроциты утрачивают его и
живут недолго.
Ядро окружено двойной мембраной, пронизанной порами, посредством которых оно
тесно связано с каналами эндоплазматической сети и цитоплазмой. Внутри ядра
находится хроматин — спирализованные участки хромосом. В период деления
клетки они превращаются в палочковидные структуры, хорошо различимые в световой
микроскоп. Хромосомы — это сложный комплекс белков с ДНК, называемый
нуклеопротеидом.
Функции ядра состоят в регуляции всех жизненных отправлений клетки, которую
оно осуществляет при помощи ДНК и РНК-материальных носителей наследственной
информации. В ходе подготовки к делению клетки ДНК удваивается, в процессе
митоза хромосомы расходятся и передаются дочерним клеткам, обеспечивая
преемственность наследственной информации у каждого вида организмов.
Кариоплазма — жидкая фаза ядра, в которой в растворенном виде
находятся продукты жизнедеятельности ядерных структур.
Ядрышко — обособленная, наиболее плотная часть ядра.
В состав ядрышка входят сложные белки и РНК, свободные или связанные фосфаты
калия, магния, кальция, железа, цинка, а также рибосомы. Ядрышко исчезает
перед началом деления клетки и вновь формируется в последней фазе деления.
Таким образом, клетка обладает тонкой и весьма сложной организацией. Обширная
сеть цитоплазматических мембран и мембранный принцип строения органоидов
позволяют разграничить множество одновременно протекающих в клетке химических
реакций. Каждое из внутриклеточных образований имеет свою структуру и
специфическую функцию, но только при их взаимодействии возможна гармоничная
жизнедеятельность клетки. На основе такого взаимодействия вещества из
окружающей среды поступают в клетку, а отработанные продукты выводятся из нее
во внешнюю среду — так совершается обмен веществ. Совершенство структурной
организации клетки могло возникнуть только в результате длительной
биологической эволюции, в процессе которой выполняемые ею функции постепенно
усложнялись.
Основы биохимии
|
|
|
|
В земной коре встречается около сотни химических элементов. Из них в организмах обнаружено 60, но только 16 элементов являются необходимыми для жизни. Более 99 % органической массы приходится на долю четырёх веществ – водорода, углерода, кислорода и азота. Важное значение также имеют фосфор, сера, натрий, магний, железо, хлор, калий, кальций, марганец, медь, кобальт и цинк.
Химические элементы входят в состав соединений, которые можно разбить на две группы:
неорганические (вода, соли и т. д.);
органические (белки, углеводы, липиды, нуклеиновые кислоты и т. д.).
2 |
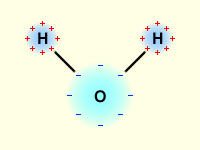
Рисунок 1.2. Молекула воды. |
вода является универсальным растворителем для полярных веществ. Это свойство также означает, что вода служит средой для транспорта различных веществ внутри организма;
вода обладает большой теплоёмкостью; благодаря этому биохимические процессы идут в малом диапазоне температур;
вода имеет большую теплоту испарения; это используется при терморегуляции у животных (потоотделение) и растений (охлаждение листьев);
у воды большая теплота плавления; это препятствует образованию кристаллов льда в клетках при понижении температуры;
плотность льда меньше плотности воды, поэтому он не тонет, и водоёмы промерзают сверху вниз. В противном случае реки и озера холодных и умеренных поясов промёрзли бы за зиму насквозь;
значительное поверхностное натяжение играет важную роль при движении воды по капиллярам организмов;
вода является необходимым компонентом метаболических реакций (например, в процессе фотосинтеза).
Также в клетке содержится много различных солей в диссоциированном состоянии. Для процессов жизнедеятельности из входящих в состав солей катионов наиболее важны K+, Na+, Ca2+, Mg2+, из анионов – HPO42–, H2PO4–, Cl–, HCO3–.
Водно-электролитный обмен это совокупность процессов поступления, всасывания, распределения и выделения из организма воды и электролитов. Он обеспечивает постоянство ионного состава, кислотно-основного равновесия и объема жидкостей внутренней среды организма. Ведущую роль в нем играет вода.
Вода –главный составной элемент минеральной природы организма.
Функции воды: 1) внутренняя среда организма; 2) структурная; 3) всасывание и транспорт веществ; 4) участие в биохимических реакциях (гидролиз, диссоциация, гидратация, дегидратация); 5) конечный продукт обмена; 6) выделение при участии почек конечных продуктов обмена.
Содержание воды в организме варьирует в зависимости от органов и тканей. Мозг – 70-84%, почки – 82%, сердце и легкие – 79%, мышцы – 76%, кожа – 72%, печень – 70%, костная ткань – 10%.
Вода, которая поступает алиментарным (с пищей) путем называется экзогенной, а образовавшаяся в качестве продукта биохимических превращений – эндогенной.
Строение молекул воды и их ассоциаты
Молекула воды (1H216O) состоит из двух атомов водорода (1H) и одного атома кислорода (16O). Оказывается, что едва ли не все многообразие свойств воды и необычность их проявления определяется, в конечном счете, физической природой этих атомов, способом их объединения в молекулу и группировкой образовавшихся молекул.
В отдельно рассматриваемой молекуле воды атомы водорода и кислорода, точнее их ядра, расположены так, что образуют равнобедренный треугольник. В вершине его - сравнительно крупное кислородное ядро, в углах, прилегающих к основанию, - по одному ядру водорода..
В соответствии с электронным строением атомов водорода и кислорода молекула воды располагает пятью электронными парами. Они образуют электронное облако. Облако неоднородно - в нем можно различить отдельные сгущения и разрежения. У кислородного ядра создается избыток электронной плотности. Внутренняя электронная пара кислорода равномерно обрамляет ядро: схематически она представлена окружностью с центром - ядром O2-. Четыре внешних электрона группируются в две электронные пары, тяготеющие к ядру, но частично не скомпенсированные. Схематически суммарные электронные орбитали этих пар показаны в виде эллипсов, вытянутых от общего центра - ядра O2-. Каждый из оставшихся двух электронов кислорода образует пару с одним электроном водорода. Эти пары также тяготеют к кислородному ядру. Поэтому водородные ядра - протоны - оказываются несколько оголенными, и здесь наблюдается недостаток электронной плотности.
Таким образом, в молекуле воды различают четыре полюса зарядов: два отрицательных (избыток электронной плотности в области кислородного ядра) и два положительных (недостаток электронной плотности у двух водородных ядер). Для большей наглядности можно представить, что полюса занимают вершины деформированного тетраэдра, в центре которого находится ядро кислорода.
Каждая молекула воды является миниатюрным диполем с высоким дипольным моментом. Под воздействием диполей воды в 80 раз ослабевают межатомные или межмолекулярные силы на поверхности погруженного в нее вещества. Во многом благодаря этому, вода проявляет себя как универсальный растворитель. Ее растворяющему действию в той или иной мере подвластны и твердые тела, и жидкости, и газы.
Постоянно соприкасаясь со всевозможными веществами, вода фактически всегда представляет собой раствор различного, зачастую очень сложного состава.
Полярность молекул воды, наличие в них частично нескомпенсированных электрических зарядов порождает склонность к группировке молекул в укрупненные "сообщества" - ассоциаты. Оказывается, полностью соответствует формуле Н2O лишь вода, находящаяся в парообразном состоянии.
Непосредственной причиной образования ассоциатов являются водородные связи. Они возникают между ядрами водорода одних молекул и электронными "сгущениями" у ядер кислорода других молекул воды. Правда, эти связи в десятки раз слабее, чем "стандартные" внутримолекулярные химические связи, и достаточно обычных движений молекул, чтобы разрушить их. Но под влиянием тепловых колебаний так же легко возникают и новые связи этого типа.
С водой мы получаем до 25% суточной потребности химических веществ". Причем эта цифра кочует по разным изданиям. Тем не менее, в разговорах специалистов в ходу больше цифра 6-8% со ссылкой на ВОЗ (Всемирная организация здравоохранения). Наиболее достоверные данные сведены в таблицу. Объяснение содержимого ее колонок:
Функции минеральных веществ: 1) пластическая (кальций, фосфор, магний); 2) поддержание осмотического давления (калий, натрий, хлор); 3) поддержание буферности биологических жидкостей (фосфор, калий, натрий); 4) поддержание коллоидных свойств тканей (все элементы); 5) детоксикационная (железо в составе цитохрома Р-450, сера в составе глутатиона); 6) проведение нервного импульса (натрий, калий); 7) участие в ферментативном катализе в качестве кофактора или ингибитора; 8) участие в гормональной регуляции (йод, цинк и кобальт входят в состав гормонов).
Промежуточный и конечный обмен минеральных веществ
Поступают минеральные вещества в организм в свободном или связанном виде. Ионы всасываются уже в желудке, основная часть минеральных веществ – в кишечнике путем активного транспорта при участии белков – переносчиков. Из желудочно-кишечного тракта поступают в кровь и лимфу, где связываются со специфическими транспортными белками. Выделяются минеральные вещества главным образом в виде солей и ионов.
С мочой: натрий, калий, кальций, магний, хлор, кобальт, йод, бром, фтор.
С калом: железо, кальций, медь, цинк, марганец, молибден, и тяжелые металлы.
Характеристика отдельных элементов
Натрий – основной катион внеклеточного отдела. Составляет 0.08 % от массы тела. Играет главную роль в поддержании осмотического давления. При отсутствии или ограничении в поступлении натрия в организм его выделение с мочой почти полностью прекращается. Всасывается в верхнем отделе тонкого кишечника при участии белков-переносчиков и требует затраты АТФ. Суточная потребность варьирует в зависимости от водно-солевого обеспечения организма. Депонируется в коже и мышцах. Кишечная потеря натрия происходит при диареях. 1) участвует в возникновении и поддержании электрохимического потенциала на плазматических мембранах клеток; 2) регулирует состояние водно-солевого обмена; 3) участвует в регуляции работы ферментов; 4) компонент K+ - Na+ насоса.
Хлор – важнейший анион внеклеточного пространства. Составляет 0,06% от массы тела. Большая часть его содержится в желудочном соке. Участвует в поддержании осмотического равновесия. Активирует амилазу и пептидазы. Всасывается в верхних отделах кишечника, выделяется в основном с мочой. Концентрация хлора и натрия обычно изменяются параллельно.
Калий – составляет 0,25% от массы тела. Во внеклеточном пространстве содержится только 2% от общего количества, а остальное - в клетках, где связан с углеводными соединениями. Всасывается на протяжении всего желудочно-кишечного тракта. Часть калия откладывается в печени и коже, а остальная поступает в общий кровоток. Обмен очень быстро протекает в мышцах, кишечнике, почках и печени. В эритроцитах и нервных клетках более медленный обмен калия. Играет ведущую роль в возникновении и проведении нервного импульса. Необходим для синтеза белков (на 1г белка – 20 мг ионов калия), АТФ, гликогена, принимает участие в формировании потенциала покоя. Выделяется в основном с мочой и меньше с калом.
Кальций – внеклеточный катион. Составляет 1,9 % от массы тела. Содержание повышается в период роста или беременности. Функционирует как составная часть опорных тканей или мембран, участвует в проведении нервного импульса и инициации мышечного сокращения, является одним из факторов гемокоагуляции. Обеспечивает целостность мембран (влияет на проницаемость), т. к. способствует плотной упаковке мембранных белков. Кальций ограничено участвует в поддержании осмотического равновесия. Вместе с инсулином активирует проникновение глюкозы в клетки. Всасывается в верхнем отделе кишечника. Степень его усвоения зависит от рН среды (соли кальция в кислой среде нерастворимы). Жиры и фосфаты препятствуют всасыванию кальция. Для полного усвоения из кишечника необходимо наличие активной формы витамина Д3 .
Большая часть кальция содержится в костной ткани (99%) в составе микрокристаллов карбонатапатита 3Са2(РО4)2 ( СаСО3 и гидроксилапатита 3Са2(РО4)2 ( СаОН. Общий кальций крови включает три фракции: белоксвязанный, ионизированный и неионозированный (который находится в составе цитрата, фосфата и сульфата).
Магний – составляет 0.05% от массы тела. В клетках его содержится в 10 раз больше, чем во внеклеточной жидкости. Многого магния в мышечной и костной ткани, также в нервной и печеночной. Образует комплексы с АТФ, цитратом, рядом белков. 1) входит в состав почти 300 ферментов; 2) комплексы магния с фосфолипидами снижают текучесть клеточных мембран; 3) участвует в поддержании нормальной температуры тела; 4) участвует в работе нервно-мышечного аппарата.
Неорганический фосфор - содержится преимущественно в костной ткани. Составляет 1% от массы тела. В плазме крови при физиологических рН фосфор на 80 % представлен двухвалентным и на 20 % одновалентным анионом фосфорной кислоты. Фосфор входит в состав коферментов, нуклеиновых кислот, фосфопротеинов, фосфолипидов. Вместе с кальцием фосфор образует апатиты – основу костной ткани.
Медь входит в состав многих ферментов и биологически активных металлопротеинов. Участвует в синтезе коллагена и эластина. Является компонентом цитохрома с электронтранспортной цепи.
Сера – составляет 0.08%. Поступает в организм в связанном виде в составе АК и сульфат-ионов. Входит в состав желчных кислот и гормонов. В составе глутатиона участвует в биотрансформации ядов.
Железо входит в состав железосодержащих белков и гема гемоглобина, цитохромов, пероксидаз.
Цинк – является кофактором ряда ферментов.
Кобальт входит в состав витамина В12.
|
|
|
Основы биохимии
|
|
|
|
Переходя к рассмотрению органических веществ, нельзя не отметить значение углерода для жизни. Вступая в химические реакции, углерод образует прочные ковалентные связи, обобществляя четыре электрона. Атомы углерода, соединяясь между собой, способны образовывать стабильные цепи и кольца, служащие скелетами макромолекул. Углерод также может образовывать кратные ковалентные связи с другими углеродными атомами, а также с азотом и кислородом. Все эти свойства обеспечивают уникальное разнообразие органических молекул.
Макромолекулы, составляющие около 90 % массы обезвоженной клетки, синтезируются из более простых молекул, называемых мономерами. Существуют три основных типа макромолекул: полисахариды, белки и нуклеиновые кислоты; мономерами для них являются, соответственно, моносахариды, аминокислоты и нуклеотиды.
Углеводами называют вещества с общей формулой Cx(H2O)y, где x и y – натуральные числа. Название «углеводы» говорит о том, что в их молекулах водород и кислород находятся в том же отношении, что и в воде.
В животных клетках содержится небольшое количество углеводов, а в растительных – почти 70 % от общего количества органических веществ.
|
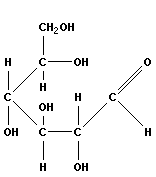
Рисунок .2.1. Глюкоза. |
Углеводы делятся на простые (моносахариды) и сложные (дисахариды и полисахариды). Моносахариды имеют общую формулу (CH2O)n, где n изменяется от 3 до 9. Самые распространённые моносахариды – глюкоза и фруктоза, имеющие формулу (CH2O)6. Все моносахариды имеют сладкий вкус, кристаллизуются и легко растворяются в воде.
1 |
|
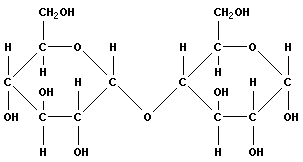
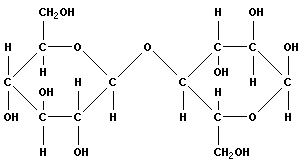
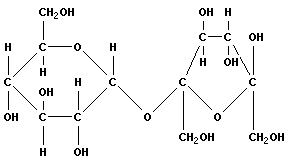
Дисахариды образуются в результате реакции конденсации между двумя моносахаридами. Иногда они используются в качестве запасных питательных веществ. Наиболее распространенными из них являются мальтоза (глюкоза + глюкоза), лактоза (глюкоза + галактоза) и сахароза (глюкоза + фруктоза). Лактоза содержится только в молоке. Сахароза (тростниковый сахар) наиболее распространена в растениях; это и есть тот самый «сахар», который мы обычно употребляем в пищу.
|
Рисунок 2.2. Мальтоза. |
|
Рисунок 2.3. Лактоза. |
|
Рисунок 2.4. Сахароза. |
Полисахариды состоят из моносахаридов. Большие размеры делают их молекулы практически нерастворимыми в воде; они не оказывают влияние на клетку и потому удобны в качестве запасных веществ. При необходимости они могут быть превращены обратно в сахара путём гидролиза.
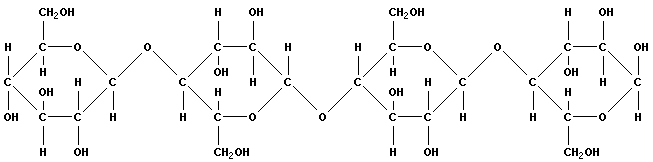
Крахмал (полимер глюкозы) запасается в клетках в виде так называемых крахмальных зерен. Эквивалентом крахмала в животном организме является гликоген (у позвоночных он содержится в печени и мышцах). Крахмал и гликоген играют роль резерва пищи и энергии.
2 |
|
|
Рисунок 2.5. Целлюлоза. |
|
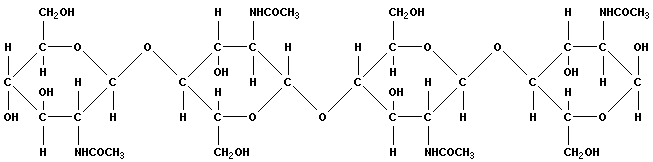
Рисунок 2.6. Хитин. |
Иногда простые сахара вступают в реакцию с сахарными спиртами и кислотами. Образующиеся при этом вещества близки к полисахаридам и носят название мукополисахаридов. Муреин играет роль структурного компонента в клетках прокариот. Хитин близок к целлюлозе; он встречается у некоторых форм грибов, а также как важный компонент наружного скелета некоторых животных. Гликопротеины и гликолипиды определяют антигенные свойства клеток. Гиалуроновая кислота и хондроитинсульфат – важные компоненты соединительной ткани позвоночных. Камеди и слизи имеют важную защитную функцию в организмах растений и животных.
|
|
|
|
|
|
|
Липидами обычно называют нерастворимые в воде органические вещества, являющиеся сложными эфирами жирных кислот и спиртов (например, глицерола). Жирные кислоты имеют общую формулу R?COOH, где R – атом водорода или радикал типа –CH3. В липидах радикал обычно представлен длинной углеводородной цепью; этот «хвост» гидрофобен, что и определяет плохую растворимость липидов в воде. Липиды, образующиеся из глицерола, называются глицеридами.
1 |
Фосфолипиды – группа глицеролов, включающая остатки жирных кислот и фосфорной кислоты. Благодаря наличию полярной фосфатной группы часть молекулы приобретает способность растворяться в воде, другая же часть молекулы остаётся нерастворимой. Из фосфолипидов строятся все плазматические мембраны живых клеток.
Воска – сложные эфиры жирных кислот и длинноцепочечных спиртов. Они используются животными и растениями в качестве водоотталкивающего покрытия (пчелиные соты, покрытие перьев птиц, эпидермис некоторых плодов и семян).
Стероиды и терпены построены из пятиатомных углеводородных строительных блоков C5H8. Из всех стероидов в организме человека в наибольшем количестве присутствует холестерол – ключевой промежуточный продукт синтеза стероидов. Стероидами также являются половые гормоны (эстроген, прогестерон, тестостерон), витамин D. К терпенам относятся ароматические вещества (ментол, камфора), натуральный каучук.
С кровью и лимфой липиды переносятся в виде липопротеинов – соединений липидов с белками.
|
|
|
|
В растениях и животных встречается свыше 170 различных аминокислот. В белках из них присутствует только 26. Растения синтезируют все необходимые им аминокислоты сами. Животные должны получать часть аминокислот – так называемые незаменимые аминокислоты (восемь аминокислот, в частности, валин, лизин, метионин, триптофан) – с пищей в готовом виде; синтезировать их из других органических соединений могут только растения и бактерии.
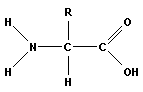
Все аминокислоты - бесцветные кристаллические вещества. Они растворимы в воде, многие имеют сладкий вкус. Важное свойство аминокислот - их амфотерность, то есть возможность проявлять как кислотные, так и основные свойства. Эта двойственность вещества связана с тем, что все аминокислоты содержат карбоксильную группу (-СООН) и аминогруппу (-NH2) (рис. 4, A). Карбоксильная группа придает аминокислоте кислотные свойства, а аминогруппа - основные.
|
Рисунок 3.1 Общая формула аминокислот. |
Общая формула аминокислот представлена на рисунке. Все они содержат карбоксильную группу –COOH и аминогруппу –NH2. В аминокислоте глицине роль R-группы играет атом водорода, в аланине – –CH3. Все аминокислоты могут существовать в двух конфигурациях: L-форме и D-форме. В природе встречается только L-форма.
Аминокислоты – бесцветные кристаллические вещества, обычно растворимые в воде. Благодаря пептидным связям аминокислоты объединяются друг с другом, образуя полипептиды (белки). Дисульфидными связями полипептиды могут соединяться как между собой, так и различными участками одной и той же цепи.
|
|
|
|
Как уже отмечалось выше, благодаря пептидным связям аминокислоты образуют белки. Часть белков образует комплексы с молекулами, содержащими серу, фосфор, железо, цинк и медь. Молекулярная масса белковых цепей колеблется от нескольких тысяч до нескольких миллионов (в вирусе табачной мозаики – около 40 000 000 молекул); в их состав входят сотни (иногда – сотни тысяч) аминокислотных остатков.
Потенциально многообразие белков очень велико – каждому белку соответствует своя особая последовательность аминокислот, контролируемая генетически. На долю белков приходится около половины сухой массы клетки.
1 |
|
По структуре белки делятся на фибриллярные (третичная структура почти не выражена, нерастворимы, представляют собой длинные полипептидные цепи), глобулярные (третичная структура хорошо выражена, растворимы) и промежуточные (фибриллярные, но растворимые). Первые входят в состав соединительных тканей, вторые играют роль ферментов, гормонов, антител.
Функционально белки могут быть структурными (компоненты соединительных тканей, слизистых секретов), транспортными (перенос крови, липидов), защитными (антитела, тромбообразование), сократительными (в мышечных тканях), запасными (молоко, белок), ферментами, гормонами, токсинами (змеиный яд).
Главная функция белков - каталитическая. Белки-катализаторы ускоряют химические реакции в клетке. Регуляторную функцию выполняют гормоны. Например, белок инсулин регулирует содержание сахара в крови. При недостатке инсулина у человека развивается болезнь - сахарный диабет.
Белки, как и углеводы, выполняют в клетке структурную функцию. Молекулы белков входят в состав всех клеточных мембран. Молекулы белка коллагена составляют основу хрящей и сухожилий. Из белка состоят волосы, шерсть, ногти, рога, копыта, чешуя, перья, паутина.
Двигательную функцию выполняют белки актин и миозин, способные вызывать сокращение мышечных волокон, а также белки, входящие в состав ресничек, жгутиков одноклеточных и специализированных клеток, например сперматозоидов многоклеточных организмов.
Специальные белки выполняют защитную функцию. Антитела, образующиеся у позвоночных,- это белки, которые обезвреживают проникающие в организм чужеродные вещества. Белок фибриноген участвует в свертывании крови.
Белки выполняют также транспортную функцию. Например, белок крови гемоглобин, который входит в состав эритроцитов, образует в легких непрочные соединения с кислородом и доставляет его ко всем клеткам организма.
Некоторые белки выполняют запасающую функцию, накапливаясь, например, в семенах растений.
При недостатке полисахаридов и липидов белки могут выполнять энергетическую функцию. При окислении молекул белков в клетке освобождается энергия примерно в таком же количестве, как и при окислении углеводов.
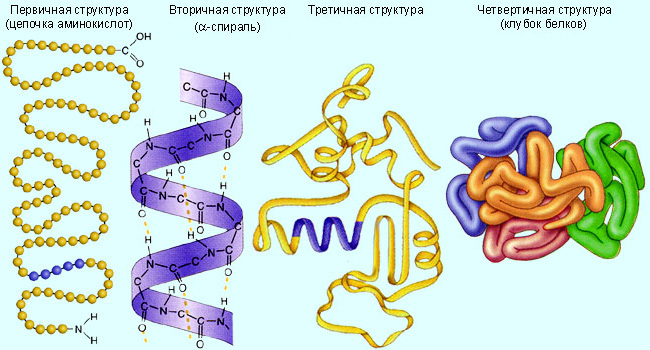
Каждому белку свойственна особая геометрическая структура. При описании пространственной структуры обычно описывают четыре разных уровня организации.
Под первичной структурой белка обычно понимают последовательность аминокислот. Первичная структура инсулина была открыта Ф. Сэнгером в 1944–54 годах; в настоящее время известна первичная структура нескольких сотен белков. Последовательность аминокислот определяет биологическую функцию белка, и замена одной единственной аминокислоты может резко изменить эту функцию.
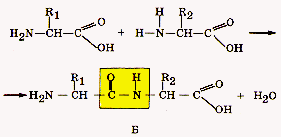
Остатки аминокислот соединяются между собой в молекулу белка посредством прочной ковалентной пептидной связи. Она возникает между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты. При этом отщепляется молекула воды (рис. 4, Б). Последовательное расположение в полипептидной цепи аминокислотных остатков, соединенных пептидными связями, определяет первичную структуру молекулы белка.
Обычно белковая молекула имеет форму спирали. Это так называемая вторичная структура, стабилизируемая водородными связями, возникающими между CO- и NH-группами. На один виток спирали приходится 3,6 аминокислотного остатка. Существуют и другие формы вторичной структуры, например, тройная спираль коллагена и складчатый слой фибрина.
Дисульфидные, ионные и водородные связи, а также гидрофобное взаимодействие заставляют большинство белковых цепей сворачиваться в компактную глобулу. Это так называемая третичная структура белка. Спираль благодаря наличию многочисленных и разнообразных связей между радикалами аминокислот (ковалентных, водородных и ионных) принимает более сложную конфигурацию, образуя клубки - третичную структуру белка.
Взаимное расположение в пространстве нескольких одинаковых или разных полипептидных клубков, составляющих одну белковую молекулу, образует четвертичную структуру. Наконец, многие белки с особо сложным строением состоят из нескольких полипептидных цепей – способ их упаковки называется четвертичной структурой.
Ряд причин (нагревание, воздействие каких-либо излучений, сильные кислоты и щелочи, тяжёлые металлы, органические растворители) могут вызвать денатурацию белка. Молекула временно или постоянно теряет свою третичную структуру и «сворачивается» или выпадает в осадок. Денатурация бывает частичной и полной. При частичной денатурации первичная структура белковой молекулы сохраняется. При устранении фактора, вызывающего частичную денатурацию, молекула белка вновь принимает естественную форму. При полной денатурации первичная структура разрушается и белковая молекула не может вернуться в исходное состояние.
Ферменты – глобулярные белки, синтезируемые живыми клетками. В каждой клетке имеются сотни ферментов. Они помогают осуществлять биохимические реакции, действуя как катализаторы. Без них реакции в клетке протекали бы слишком медленно и не могли бы поддерживать жизнь. Ферменты делятся на анаболические (реакции синтеза) и катаболические (реакции распада). Нередко в процессе превращения одного вещества в другое участвуют несколько ферментов; такая последовательность реакций называется метаболический путь.
Важнейшая функция белков - каталитическая. Белковые молекулы, увеличивающие на несколько порядков скорость химических реакций в клетке, называют ферментами. Ни один биохимический процесс в организме не происходит без участия ферментов.
*В настоящее время обнаружено свыше 2000 ферментов Их эффективность во много раз выше, чем эффективность неорганических катализаторов, используемых в производстве Так, 1 мг железа в составе фермента каталазы заменяет 10 т неорганического железа Каталаза увеличивает скорость разложения пероксида водорода (H2O2) в 1011 раз Фермент, катализирующий реакцию образования угольной кислоты (CO2 + H20 « Н2СО3), ускоряет реакцию в 107 раз.
Важным свойством ферментов является специфичность их действия. каждый фермент катализирует только одну или небольшую группу сходных реакций.
Вещество, на которое воздействует фермент, называют субстратом. Структуры молекулы фермента и субстрата должны точно соответствовать друг другу Этим объясняется специфичность действия ферментов. При соединении субстрата с ферментом пространственная структура фермента изменяется.
Последовательность взаимодействия фермента и субстрата можно изобразить схематично:
Субстрат + Фермент ® Фермент-субстратный комплекс ® Фермент + Продукт.
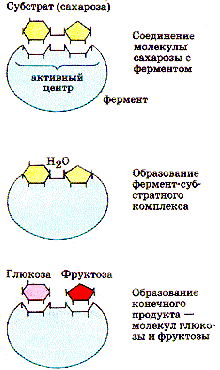
Из схемы видно, что субстрат соединяется с ферментом с образованием фермент-субстратного комплекса При этом субстрат превращается в новое вещество - продукт. На конечном этапе фермент освобождается от продукта и вновь вступает во взаимодействие с очередной молекулой субстрата.
Ферменты функционируют лишь при определенной температуре, концентрации веществ, кислотности среды. Изменение условий приводит к изменению третичной и четвертичной структуры белковой молекулы, а следовательно, и к подавлению активности фермента Как это происходит? Каталитической активностью обладает лишь определенный участок молекулы фермента, называемый активным центром. Активный центр содержит от 3 до 12 аминокислотных остатков и формируется в результате изгиба полипептидной цепи.
Под влиянием разных факторов изменяется структура молекулы фермента. При этом нарушается пространственная конфигурация активного центра и фермент теряет свою активность.
![]()
Ферменты - это белки, играющие роль биологических катализаторов. Благодаря ферментам на несколько порядков возрастает скорость химических реакций в клетках. Важное свойство ферментов - специфичность действия в определенных условиях.
Основные свойства ферментов:
увеличивают скорость реакции;
не расходуются в реакции;
их присутствие не влияет на свойства продуктов реакции;
активность ферментов зависит от pH, температуры, давления и концентрации;
ферменты изменяют энергию активации, при которой может произойти реакция;
ферменты не изменяют сколько-нибудь значительно температуру, при которой происходит реакция.
Высокая специфичность фермента объясняется особой формой его молекулы, точно соответствующей молекуле субстрата (вещества, атакуемого ферментом). Эту гипотезу называют гипотезой «ключа и замка». В середине XX века исследования показали, что субстрат может вызывать изменения в структуре фермента; фермент изменяет свою форму, что даёт ему возможность наиболее эффективно выполнять свою функцию.
Многим ферментам для эффективной работы требуются небелковые компоненты, называемые кофакторами. Такими веществами могут быть неорганические ионы, заставляющие ферменты принять форму, способствующую ферментативной реакции, простетические группы (флавинадениндинуклеотид (ФАД), гем), занимающие такое положение, при котором они могут эффективно содействовать реакции, и коферменты (НАД, НАДФ, АТФ).
Некоторые вещества могут вызывать замедление ферментативных реакций, действуя как ингибиторы. При этом они соединяются с субстратом сами, занимая место фермента и сводя на нет ферментативный эффект (конкурентное ингибирование), или вызывают денатурацию ферментативного белка (неконкурентное ингибирование).
Важнейшая функция белков - каталитическая. Белковые молекулы, увеличивающие на несколько порядков скорость химических реакций в клетке, называют ферментами. Ни один биохимический процесс в организме не происходит без участия ферментов.
*В настоящее время обнаружено свыше 2000 ферментов Их эффективность во много раз выше, чем эффективность неорганических катализаторов, используемых в производстве Так, 1 мг железа в составе фермента каталазы заменяет 10 т неорганического железа Каталаза увеличивает скорость разложения пероксида водорода (H2O2) в 1011 раз Фермент, катализирующий реакцию образования угольной кислоты (CO2 + H20 « Н2СО3), ускоряет реакцию в 107 раз.
Важным свойством ферментов является специфичность их действия. каждый фермент катализирует только одну или небольшую группу сходных реакций.
Вещество, на которое воздействует фермент, называют субстратом. Структуры молекулы фермента и субстрата должны точно соответствовать друг другу Этим объясняется специфичность действия ферментов. При соединении субстрата с ферментом пространственная структура фермента изменяется.
Последовательность взаимодействия фермента и субстрата можно изобразить схематично:
Субстрат + Фермент ® Фермент-субстратный комплекс ® Фермент + Продукт.
Из схемы видно, что субстрат соединяется с ферментом с образованием фермент-субстратного комплекса При этом субстрат превращается в новое вещество - продукт. На конечном этапе фермент освобождается от продукта и вновь вступает во взаимодействие с очередной молекулой субстрата (рис. 7).
Ферменты функционируют лишь при определенной температуре, концентрации веществ, кислотности среды. Изменение условий приводит к изменению третичной и четвертичной структуры белковой молекулы, а следовательно, и к подавлению активности фермента Как это происходит? Каталитической активностью обладает лишь определенный участок молекулы фермента, называемый активным центром. Активный центр содержит от 3 до 12 аминокислотных остатков и формируется в результате изгиба полипептидной цепи.
Под влиянием разных факторов изменяется структура молекулы фермента. При этом нарушается пространственная конфигурация активного центра и фермент теряет свою активность.
Ферменты - это белки, играющие роль биологических катализаторов. Благодаря ферментам на несколько порядков возрастает скорость химических реакций в клетках. Важное свойство ферментов - специфичность действия в определенных условиях.
|
|
|
|
|
|
|
Н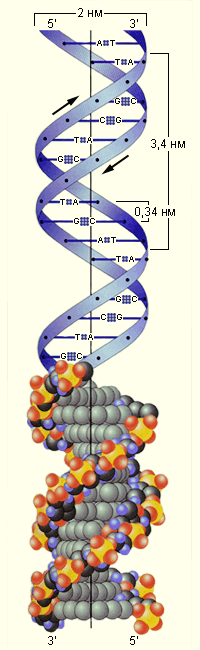 уклеиновые
кислоты содержат в себе генетический
материал всех живых организмов. Выяснение
их структуры открыло новую эру в наших
знаниях о природе.
уклеиновые
кислоты содержат в себе генетический
материал всех живых организмов. Выяснение
их структуры открыло новую эру в наших
знаниях о природе.
Составными частями нуклеиновых кислот являются нуклеотиды. Молекула нуклеотида состоит из пентозы, азотистого основания и фосфорной кислоты. В зависимости от типа сахара различают рибонуклеиновую кислоту (РНК; в её состав входит рибоза) и дезоксирибонуклеиновая кислота (ДНК; в её состав входит сахар дезоксирибоза, у которого на один атом кислорода меньше). В обоих типах нуклеиновых кислот содержатся четыре типа оснований: аденин (А), гуанин (Г), цитозин (Ц), тимин (Т; в РНК вместо него содержится урацил (У)). Первые два основания относятся к классу пуринов, остальные – к пиримидинам. Фосфорная кислота определяет кислотные свойства нуклеиновых кислот.
|
|
Выяснить структуру ДНК удалось в 1953 году английским ученым Д. Уотсону и Ф. Крику. Они показали, что ДНК состоит из двух полинуклеотидных цепей. Каждая цепь закручена в спираль вправо, и обе цепи свиты вместе, образуя двойную спираль. Шаг спирали составляет 3,4 нм (по 10 пар оснований в витке), а диаметр витка – 2 нм. Фосфатные группировки находятся снаружи спирали, а азотистые основания – внутри. ДНК – очень хрупкая молекула, простое перемешивание её раствора может привести к разрыву цепей на более мелкие куски.
Число адениновых оснований в любой ДНК равно числу тиминовых оснований, число гуаниновых оснований всегда равно числу цитозиновых оснований. Никаких ограничений относительно последовательности нуклеотидов в одной цепи не существует, но эта последовательность в одной цепи полностью определяет собой последовательность нуклеотидов в другой. Пары соединяются водородными связями между основаниями в строго определённом порядке (аденин с тимином, гуанин с цитозином). Таким образом, цепи двойной спирали комплементарны друг другу.
Для того, чтобы ДНК являлась генетическим материалом, она должна быть способна нести в себе закодированную информацию и точно воспроизводиться (реплицироваться). Последующие исследования доказали, что ДНК действительно содержит в себе генетическую информацию.
Молекула РНК в отличие от ДНК состоит, как правило, из одной цепи и имеет гораздо меньшие размеры. Существует три основных вида РНК: транспортная (т-РНК), информационная (и-РНК) и рибосомная (р-РНК). Информационная РНК (и-РНК) является матрицей, которую рибосомы используют при синтезе белка. Её нуклеотидная последовательность комплементарна сообщению, содержащемуся в определённом участке ДНК. Транспортные РНК переносит аминокислоты к месту синтеза. Несколько видов р-РНК являются основным компонентом рибосом. Нуклеотидные последовательности т-РНК и р-РНК также определяются определёнными участками ДНК.
ДНК находится, главным образом, в ядре клетки (у прокариот рассредоточена по клетке), являясь основным веществом хромосом. РНК сконцентрирована в ядрышке, цитоплазме и частично в хромосомах. Молекул РНК в клетке значительно больше (иногда их десятки тысяч), чем молекул ДНК.
Роль нуклеотидов заключается не только в синтезе нуклеиновых кислот. Некоторые нуклеотиды играют важную роль в жизнедеятельности организмов, являясь коферментами. Примером могут служить аденозинфосфорные кислоты, содержащие аденин, рибозу и несколько остатков фосфорной кислоты. Присоединение каждой новой фосфатной группы к кислоте сопровождается аккумуляцией энергии, а их отщепление – выделением. Превращение аденозинтрифосфорной кислоты (АТФ) в аденозиндифосфорную (АДФ) является основой энергетического обмена внутри клетки.
М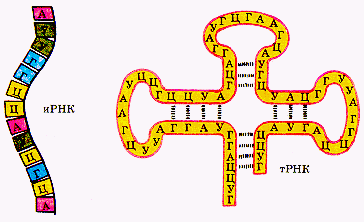 олекулы
РНК имеются и в ядре, и в цитоплазме.
олекулы
РНК имеются и в ядре, и в цитоплазме.
Содержание их в клетке зависит от стадии жизненного цикла клетки.
Известны три основных типа РНК: информационные, или матричные, - иРНК; рибосомные - рРНК, транспортные - тРНК, которые различаются по форме, размерам и функциям молекул. Их главная функция - участие в биосинтезе белка.
На рисунке показано строение молекул РНК. Вы видите, что молекула РНК, как и молекула ДНК, состоит из четырех типов нуклеотидов, три из которых содержат такие же азотистые основания, как и нуклеотиды ДНК (А, Г, Ц). Однако в состав РНК вместо азотистого основания тимина входит другое азотистое основание - урацил (У). Таким образом, в состав нуклеотидов молекулы РНК входят азотистые основания: А, Г, Ц, У. Кроме того, вместо углевода дезоксирибозы в состав РНК входит рибоза.
Молекула РНК, как правило, одиночная цепь, состоящая из четырех типов нуклеотидов - А, У, Г, Ц. Известны три основных вида РНК: иРНК, рРНК, тРНК. Содержание молекул РНК в клетке непостоянно, они участвуют в биосинтезе белка.
В клетках всех организмов имеются молекулы АТФ - аденозинтрифосфорной кислоты. АТФ - универсальное вещество клетки, молекула которого имеет богатые энергией связи. Молекула АТФ - это один своеобразный нуклеотид, который, как и другие нуклеотиды, состоит из трех компонентов: азотистого основания - аденина, углевода - рибозы, но вместо одного содержит три остатка молекул фосфорной кислоты. Связи, обозначенные на рисунке значком ~, богаты энергией и называются макроэргическими. Каждая молекула АТФ содержит две макроэргические связи.
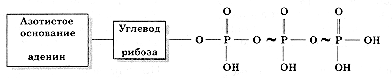
При разрыве макроэргической связи и отщеплении с помощью ферментов одной молекулы фосфорной кислоты освобождается 40 кДж/моль энергии, а АТФ при этом превращается в АДФ - аденозиндифосфорную кислоту. При отщеплении еще одной молекулы фосфорной кислоты освобождается еще 40 кДж/моль; образуется АМФ - аденозинмонофосфорная кислота. Эти реакции обратимы, то есть АМФ может превращаться в АДФ, АДФ - в АТФ.

Молекулы АТФ не только расщепляются, но и синтезируются, поэтому их содержание в клетке относительно постоянно. Значение АТФ в жизни клетки огромно. Эти молекулы играют ведущую роль в энергетическом обмене, необходимом для обеспечения жизнедеятельности клетки и организма в целом.
АТФ - универсальное энергетическое вещество клетки, в котором имеются богатые энергией связи. АТФ играет центральную роль в обмене энергии в клетке. РНК и АТФ содержатся как в ядре, так и в цитоплазме клетки.
Клетка в своей жизни проходит разные состояния: фазу роста и фазы подготовки к делению и деления. Клеточный цикл – переход от деления к синтезу веществ, составляющих клетку, а затем опять к делению – можно представить на схеме в виде цикла, в котором выделяют несколько фаз.
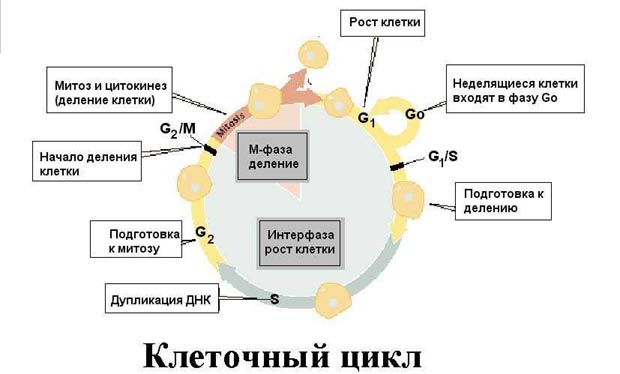
Клетки, сохранившие способность к митозу, имеют клеточный цикл, ограниченный последовательностью деления. Период между следующими друг за другом делениями (митозами) в таких клетках называют интерфазой. В интерфазе выделяют следующие периоды:
Пресинтетический период (G1). Клетка имеет полный диплоидный набор: 2n2c (гаплоидный – nc). В этот период происходят процессы биосинтеза белка, трансформации энергии и ее накопления в виде макроэргических соединений. Хромосомы в ядре деспирализованы. Клетка растет, увеличивается в размерах.
Синтетический период (S). Клетка готовится к предстоящему митозу. Происходит процесс репликации ДНК по принципу комплиментарности, то есть начинается процесс передачи наследственной информации. Генетическая характеристика клетки в конце синтетического периода 2n4c.
Постсинтетический период (G2). В этот период клетка морфологически содержит 2 молекулы ДНК. Начинается процесс надщепления хромосом на две хроматиды (дочерние хромосомы). Формируется сначала диада, а затем тетрада. Генетическая характеристика клетки 2n4c. Биохимический процесс надщепления изучен слабо. Предполагается, что на этой стадии происходит накопление высокоэнергетических соединений.
Жизнь клетки и переход от одной фазы клеточного цикла к другой регулируется изменением концентраций белков циклинов , как это показано на рисунке.
При подготовке к делению происходит репликация ДНК, на каждой хромосоме синтезируется ее копия. Пока эти хромосомы после удвоения не расходятся, каждая хромосома в этой паре называется хроматидой. После репликации ДНК конденсируется, хромосомы приобретают более компактную укладку, и в таком состоянии их можно увидеть в световом микроскопе. Между делениями эти хромосомы не столь конденсированы и в большей степени расплетены. Понятно, что в конденсированном состоянии им трудно функционировать. Хромосома имеет вид в виде буквы Х только во время одной из стадий митоза. Раньше считалось, что между делениями клетки хромосомная ДНК ( хроматин ) находится в полностью расплетенном состоянии, но сейчас выясняется, что структура хромосом достаточно сложная и степень деконденсации хроматина между делениями не очень велика.
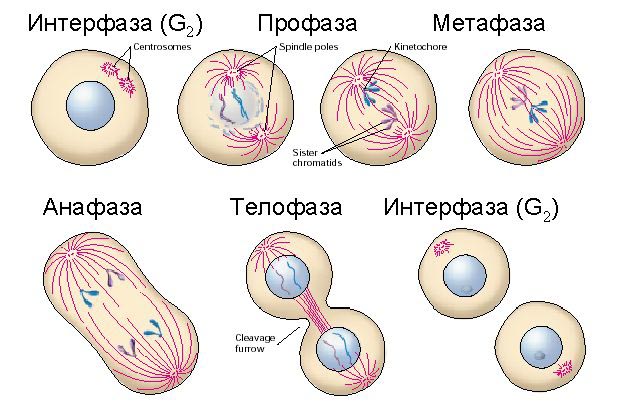
Митоз (кариокинез, непрямое деление клетки) – наиболее распространенный способ репродукции клеток. Митоз обеспечивает возможность образования генетически равноценных клеток и сохраняет преемственность хромосом в ряду клеточных поколений. Митоз – непрерывный единый процесс деления ядра, при котором обеспечивается идентичное расположение хромосом в дочерних клетках.
Собственно митотическое деление
Выделяют следующие стадии митоза:
Профаза. К началу профазы клетка обычно округляется, вязкость ее цитоплазмы нарастает. Морфологически хромосомы различимы вследствие спирализации. По мере протекания профазы хромосомы укорачиваются, утолщаются, наследственный материал плотно упаковывается по длине. Оболочка клетки утолщается. Ядерная оболочка растворяется, хромосомы перемещаются в центр клетки, образуя экваториальную пластинку. Центриоли клеточного центра расходятся к полюсам, между ними формируется веретено деления. Генетическая характеристика 2n4c.
Метафаза. Морфологически хромосомы упорядочено лежат в области экватора. В этот момент они хорошо различимы. Надщепление хромосом на хроматиды доходит до центромеры (центральная перетяжка хромосом). Кариотип организма изучают именно на предмете метафазной клетки. Генетическая характеристика 2n4c.
Анафаза. Это стадия полного разъединения сестринских хромосом и расхождения их к полюсам. Результатом является образование двух групп хромосом. В протекании анафазы важная роль принадлежит основным компонентам цитоскелета: микротрубочкам и микрофиламентам. Генетическая характеристика 4n4c (на полюсах по 2n2c).
Телофаза. На второй стадии происходят процессы цитокинеза. Хромосомы деспирализуются, вокруг них концентрируется ядерное вещество и формируется ядерная оболочка. Генетическая характеристика 4n4c. Цитотомия осуществляется путем образования внутриклеточной пластинки у растительных клеток или путем образования борозды деления у животных клеток. В результате последней фазы митоза образуются две клетки, каждая из которых имеет полный диплоидный набор: 2n2c.
Продолжительность митоза неодинакова в разных типах клеток. В животных клетках среднее время митоза составляет 30-60 минут, а в растительных может достигать 2-3 часов. В жизненном цикле клеток митоз занимает всего 5-10% времени клеточного цикла, все остальное время занимает интерфаза, причем пресинтетический период занимает 30-40%, синтетический 30-50%, постсинтетический – 10-20% времени клеточного цикла. Продолжительность митоза зависит также от размеров клеток, числа ядер, от условий окружающей среды, в частности от температуры.
Мейоз – форма ядерного деления, сопровождающаяся уменьшением числа хромосом от диплоидного (2n) до гаплоидного (n). При этом в родительской клетке происходит однократное удвоение хромосом (репликация ДНК, как при митозе), за которым следуют два цикла клеточных и ядерных делений (первое и второе деление мейоза). Таким образом, одна диплоидная клетка дает начало четырем гаплоидным клеткам.
Стадии мейоза Интерфаза I деления
Продолжительность ее различна у разных видов. В эту фазу происходит репликация ДНК, и клетка увеличивается в размерах. Начинается надщепление хромосом на пару хроматид, соединенных центромерой. Генетическая характеристика 2n4c.
Профаза I
Это наиболее продолжительная и сложная стадия мейоза. В ней различают 5 последовательных периодов:
Лептотена – стадия длинных, тонких, слабо спирализованных хромосом, на которых видны утолщения – хромомеры. В это время заканчивается репликация ДНК, которая была деспирализована перед мейозом.
Зиготена – стадия попарного соединения гомологичных хромосом, при котором хромомеры одной гомологичной хромосомы точно прикладываются к соответствующим хромомерам другой. Это явление называется конъюгацией.
Пахитена – стадия толстых нитей. Гомологичные хромосомы соединены в пары – биваленты. Число бивалентов соответствует гаплоидному набору хромосом. На этой стадии заканчивается расщепление хромосом на хроматиды, и каждая из них уже состоит из двух хроматид, поэтому каждый бивалент включает в себя четыре хроматиды. В это время конъюгирующие хромосомы переплетаются, и происходит обмен гомологичными участками хроматид – кроссинговер (crossing-over – перекрест).
Диплотена – период, когда гомологичные хромосомы начинают отталкиваться друг от друга, но в участках кроссинговера остаются соединенными.
Диакинез – период, в котором отталкивание гомологичных хромосом продолжается, но они еще соединены в биваленты своими концами, образуя характерные фигуры – кольца и кресты. Связь между хроматидами вследствие прошедшего кроссинговера называется хиазмой. В этот период хромосомы максимально спирализованы, укорочены и утолщены. Непосредственно после диакинеза ядерная оболочка разрушается.
В оогенезе выделяют еще один период профазы I мейоза (между диплонемой и диакинезом) – диктиотену. Хромосомы представляют собой деконденсированные нити и напоминают по внешнему виду «ламповые щетки». На этом периоде во время внутриутробного развития прерывается мейоз первичных половых клеток, синтезируется и-РНК. Мейоз возобновляется с началом созревания каждого конкретного фолликула в яичнике. Генетическая характеристика стадии – 2n4c.