- •5. Фазовые равновесия
- •5.1. Основные понятия, определения, законы
- •5.1.1. Условия фазового равновесия
- •5.1.2. Фазовые равновесия в однокомпонентной системе
- •5.1.3. Равновесие пар–жидкость в двухкомпонентной системе
- •5.1.4. Равновесие жидкость–твёрдое в двухкомпонентной системе. Уравнение Шрёдера
- •5.2. Лабораторные работы
- •5.2.1. Работа ф-1. Определение зависимости давления насыщенного пара от температуры в однокомпонентной системе и расчёт теплоты парообразования
- •5.2.2. Работа ф-2. Равновесие жидкость – пар в двухкомпонетных системах
- •5.2.3. Работа ф-3. Построение фазовой диаграммы плавкости двухкомпонентной системы kno3–NaNo3.
- •5.3. Контрольные вопросы к работам ф-1, ф-2 и ф-3
5.2.2. Работа ф-2. Равновесие жидкость – пар в двухкомпонетных системах
В лабораторной работе определяются температура кипения и равновесные составы жидкости и сосуществующего с ней пара при постоянном давлении. Как сказано выше, для точного определения температуры кипения веществ при постоянном давлении
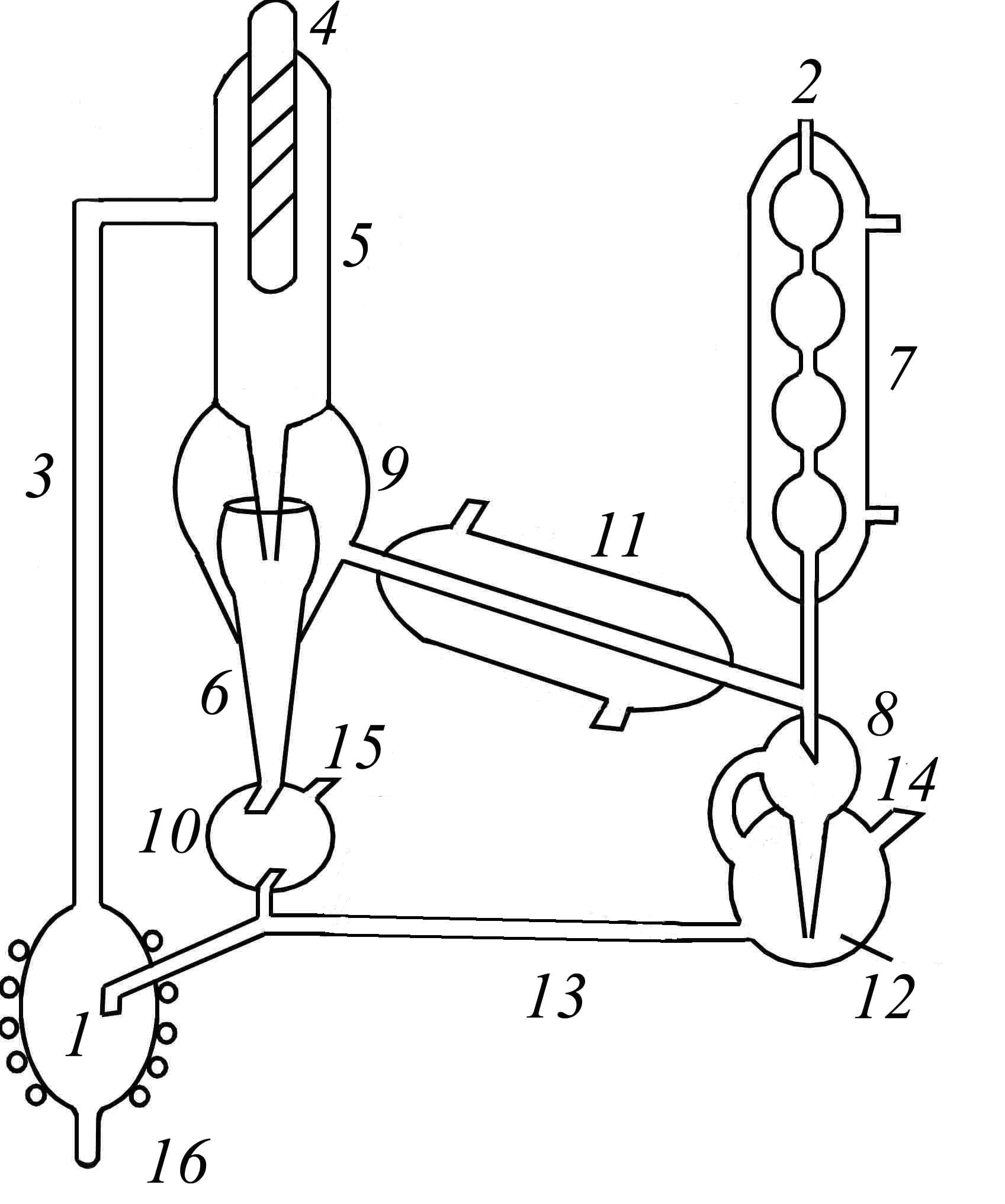
применяют эбулиометр Свентославского (см. задачу Ф-1). Эбулиометр является составной частью установки, используе-мой в данной задаче. На рис. 5.12 приведена схема прибора, который применяется в этой работе. Исследуемая жидкость заливается в куб 1 через отверстие 14, куб обогревается спиралью из нихрома, которая подключена к сети через ЛАТР, или водяным термостатом. Парожидкостная смесь поднимается по трубке 3 и орошает термометрический карман 4. Для разделения жидкости и |
Рис. 5.12. Схема прибора |
пара служит сепаратор 9. Жидкость по трубке 6 попадает в сборник жидкости 10, откуда избыток жидкости стекает в куб. Пар, проходя через прямой холодильник 11, конденсируется и через счётчик капель 8 попадает в резервуар 12, соединённый с кубом шлангом 13, по которому избыток дистиллята стекает обратно в куб. При этом дистиллят всё время обновляется. Через некоторое время состав дистиллята перестанет изменяться и будет строго соответствовать составу пара, равновесного с жидкостью, находящейся в приборе. Состав жидкости в резервуаре 10 может значительно отличаться от исходного, поэтому жидкость также должна анализироваться. Пробы дистиллята и жидкости отбираются для анализа через отростки 14 и 15. Жидкость из куба сливают через отросток 16. Прибор такой конструкции используют при изучении изобарических равновесий жидкость–пар. Чтобы получить давление, отличное от атмосферного, прибор может быть присоединён к маностату – устройству, обеспечивающему постоянство давлений. При выполнении лабораторной работы маностат не используется, так как небольшие колебания атмосферного давления сказываются на составах фаз незначительно.
Особенности методики и подготовка к выполнению работы
Для определения состава проб жидкости и пара, можно использовать различные методы анализа. В нашем практикуме для этой цели применяют измерение показателя преломления проб жидкости и сконденсированного пара или метод ГЖХ.
Если используется метод измерения показателя преломления, то точность измерения состава раствора тем выше, чем больше разница между показателями преломления компонентов смеси. Существенно, чтобы зависимость показателя преломления от концентрации компонентов была монотонной, т.е. зависимость не должна иметь экстремума.
Для выполнения лабораторной работы можно рекомендовать системы: толуол + изопропиловый спирт (анализ проб производится по показателю преломления); гексан + ацетон (для анализа применяется метод ГЖХ).
До начала основной части работы необходимо построить калибровочную кривую – зависимость показателя преломления nD от состава раствора. Для этого измеряют показатели преломления чистых веществ и девяти растворов известного состава. Растворы готовятся следующим образом: взвешивают бюкс с крышкой, после этого отбирают в бюкс определённый объём одного компонента и взвешивают его с закрытой крышкой. Затем добавляют определённый объём второго компонента и также взвешивают. Растворы удобно готовить с шагом 0,5 мл (0,5; 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,0; 4,5 мл одного компонента и, соответственно, 4,5; 4,0; 3,5; 3,0; 2,5; 2,0; 1,5; 1,0; 0,5 мл другого компонента). Состав растворов рассчитывается в мольных долях. Для определения состава исследуемой бинарной смеси достаточно измерить её показатель преломления и воспользоваться калибровочной кривой.
Если для определения состава проб используют метод ГЖХ, то до начала опытов также следует проделать калибровку хроматографа, т.е. определить относительную чувствительность детектора к компонентам раствора. Растворы для калибровки готовят как описано выше, затем записывают хроматограммы, рассчитывают коэффициент k = S1/(S1+S2), где S1 и S2 – площади пиков компонентов, и строят калибровочный график зависимости k от мольного содержания первого компонента в растворе.
Целью работы является построение фазовой Т–Х диаграммы и расчёт коэффициентов активности компонентов смеси.
Порядок выполнения работы
– В прибор заливают около 40 мл чистого компонента или приготовленного раствора. Для безопасного проведения опыта нужно заливать в куб компонент с меньшей температурой кипения, а в ходе работы добавлять компонент с большей температурой кипения.
– Подают воду в холодильники прибора и включают нагревание. С помощью ЛATPа устанавливают ток через нагреватель примерно 0,5 А. Через некоторое время жидкость в кубе закипает. Регулируют нагрев так, чтобы скорость прохождения капель через счётчик 8 была около 40 капель в минуту.
– После того, как установится значение температуры кипения, не изменяющееся в течение 10 мин, отдельными пипетками берут пробы жидкости и конденсата (~ 0,1 мл) через отростки 14 и 15. Сразу же после взятия наносят пробы на призму рефрактометра или вкалывают в испаритель газового хроматографа и определяют показатель преломления или площади пиков. Записывают значение температуры кипения раствора. Используя калибровочную кривую определяют составы проб.
– Чтобы проверить, установилось ли равновесие в приборе, через 5 минут повторяют процедуру. Если полученные значения nD жидкости и дистиллята, а также Ткип. отличаются от предыдущих, процедуру повторяют ещё раз. При установившемся равновесии составы фаз и Ткип. должны быть постоянными.
– Для того, чтобы изменить концентрацию раствора сливают часть жидкости через отросток 16 и добавляют в куб рассчитанное количество компонента с большей температурой кипения. Усиливают нагрев куба и после установления стационарного режима кипения вновь определяют составы фаз и Ткип.. В ходе эксперимента контролируют уровень жидкости в кубе 1.
– Повторяют процедуру так чтобы охватить весь диапазон составов исследуемой системы.
– В начале и в конце работы измеряют и записывают атмосферное давление, которое понадобится для последующих расчётов.
Экспериментальные данные сводят в табл. 5.2.
Таблица 5.2
Таблица для записи экспериментальных данных
Номер р-ра |
Tкип, 0С |
Ратм, мм рт. ст |
nD жидкости |
nD пара |
Состав жидкости |
Состав пара |
|
|
|
|
|
|
|
Обработка полученных данных
Строят фазовую диаграмму Т–Х. По характеру кривых жидкости и пара судят о наличии или отсутствии азеотропа. При наличии азеотропа определяют его состав.
Рассчитывают коэффициенты активности компонентов смеси, используя данные о температурной зависимости давления насыщенного пара чистых жидкостей из справочника.
Строят график зависимости коэффициентов активности обоих компонентов от состава, проверяют их на термодинамическую совместимость.
Интерпретируют наблюдаемую зависимость от состава с молекулярной точки зрения (дать общую характеристику межмолекулярных взаимодействий в системе).