
УДК 553.973(542.943+662.744)
ИССЛЕДОВАНИЕ ПРОЦЕССОВ ОКИСЛЕНИЯ И ТЕРМОРАСТВОРЕНИЯ ОЗЕРНОГО САПРОПЕЛЯ
© Б.Н.Кузнецов, В.Е.Тарабанько, М.Ю.Черняк, Н.Г.Береговцова, В.И.Шарыпов, Т.П.Милошенко, Г.В.Плаксин
Институт химии и химической технологии СО РАН, Академгородок, Красноярск, 660036 (Россия) e-mail: inm@icct.ru
Институт проблем переработки углеводородов СО РАН, Нефтезаводская, 54, Омск, 644040 (Россия) e-mail: plaksin@incat.okno.ru
Показана возможность полного перевода органического вещества сапропеля в растворимое состояние при окислении его пероксидом водорода в водно-аммиачной среде при комнатной температуре в течение 15-20 мин.
При каталитическом окислении сапропеля молекулярным кислородом при 170оС в присутствии Сu(OH)2 зарегистрировано образование ароматических альдегидов, среди которых преобладает сиреневый альдегид. При терморастворении сапропеля в нефтяном остатке степень конверсии органической массы сапропеля составляет 70% при 370оС, а выход жидких углеводородов достигает 73% масс.
Введение
Сапропели представляют собой типичные органоминеральные донные отложения пресноводных озёр. Процессы их накопления протекают постоянно, причём для многих водоёмов они приобретают прогрессирующий характер [1]. По данным ПГО Новосибирскгеология, разведанные сапропелевые ресурсы Новосибирской и Омской областей включают 92 крупных месторождения с общими учётными запасами более 93 млн м3 [2, 3].
Непосредственным источником органического вещества (ОВ) в сапропелевых осадках озёр служат нерастворимые остатки планктона и других организмов. Некоторая доля отложившегося ОВ подвергается минерализации, а остальная часть консервируется и в дальнейшем подвергается геохимическим превращениям в анаэробных условиях. Границей между минеральными осадками озёр и сапропелями принято считать 15 % содержание ОВ. Осадки с большим количеством ОВ приобретают ряд характерных для сапропелей особенностей: студнеобразную консистенцию, тёмный цвет, коллоидную структуру. Содержание ОВ в сапропелях разных типов варьируется в широких пределах и может достигать 94% на сухую массу (СВ).
Химический состав ОВ сапропелей определяется условиями их формирования, а также разнообразием растительного и животного мира озёр. По сравнению с торфами и углями органическая масса сапропелей менее богата углеродом и отличается более высоким содержанием легкогидролизуемых веществ, включающих гемицеллюлозу, азотсодержащие соединения. Средний элементный состав сухой органической массы сапропеля (% масс): С-62; Н-8,6; N-2,7 [4].
Широкое распространение получило применение сапропелей в сельском хозяйстве в качестве органоминеральных удобрений и кормовых добавок рациону животным, а также в медицине (целебные грязи и вытяжки биологически активных веществ). Анализ литературных источников показывает, что малозольные сапропели с высоким выходом смолы или повышенным содержанием битумов могут служить сырьём для получения разнообразных химических продуктов [4-7].
Изучение термического разложения некоторых сапропелей Латвии [4] показало, что в процессе полукоксовании можно получить до 25-30% смолы на СВ. При термическом растворении сапропеля общий выход жидких продуктов в 1,5-2 раза, а фенолов и пиридиновых оснований в 304 раза выше, причём примерно половина продуктов выкипает до 300оС. Таким образом, термическое растворение является перспективным методом переработки сапропеля для получения жидкого топлива, фенолов, пиридиновых оснований и ряда других продуктов.
Представляет интерес переработка органической массы сапропелей окислительными методами. Известно, что окислением лигнинов получают ароматические альдегиды – пара-гидроксибензальдегид и его метоксилированные производные - ванилин и сиреневый альдегид. В процессе превращения растительных остатков в сапропель лигниновые компоненты оказываются относительно устойчивыми и накапливаются в сапропеле. Поскольку даже из сапропелитовых углей путём их окисления нитробензолом получают до 7-8% ванилина [8], менее метаморфизованное сырьё – сапропель – может дать ещё больший выход ароматических альдегидов.
Цель настоящей работы заключалась в оценке возможностей переработки сапропелей в ценные химические продукты методами окисления и терморастворения.
Экспериментальная часть
В работе использовали воздушно - сухой сапропель озёр Омской области. Зольность данного образца составляла 52% масс. Элементный состав органической массы сапропеля (обеззоленной): Сdaf – 54,1; Нdaf – 6,5; Ndaf – 1,6; Odaf – 33,1%.
Для окисления пероксидом водорода навеску сапропеля обрабатывали 25% водным раствором аммиака в массовом соотношении 1 : 0.6, выдерживали в течение 7 мин. И добавляли 4 масс. Части в расчёте на сапропель 35% раствора пероксида водорода. По окончании процесса нерастворимый остаток отфильтровывали и по разности массы исходного сапропеля и твёрдого остатка рассчитывали выход солей гуминовых кислот.
Эксперименты по каталитическому окислению молекулярным кислородом проводили в качающемся реакторе из нержавеющей стали объёмом 0,1 литра при температуре 170оС и парциальном давлении кислорода 0,3 МПа [9]. В реактор загружали 3 г. сапропеля, 60 мл. раствора 10% NaOH и 1,58 г. CuSO4 · 5H2O. Через определённые промежутки времени (5, 10, 15 и далее мин.) всю реакционную массу под давлением эвакуировали из редактора. Пробу реакционной массы подкисляли 10% H2SO4 до pH 3÷4 и исчерпывающие экстрагировали этилацетатом. Концентрацию альдегидов определяли методом ГЖХ[9].
Для термического растворения сапропеля использовали остаток дистилляции западно – сибирской нефти с началом кипения 350оС и следующими характеристиками, масс.%: Сdaf – 85,4; Hdaf – 12,5; Ndaf – 0,2; Sdt – 0,9; Odif – 1,0.
Терморастворение сапропеля проводили в нагреваемом вращающемся автоклаве ёмкостью 0,25 л. В атмосфере аргона [10]. Загрузка сапропеля и нефтяного остатка – по 10 г., продолжительность эксперимента при рабочей температуре – 60 мин., рабочее давление – 0,7 – 1,0 МПа в зависимости от температуры процесса. По окончании эксперимента определяли объём газообразных продуктов. Состав газов анализировали на хроматографе с использованием детектора по теплопроводности и колонок с цеолитом (для анализа CH4 и CO) и порапаком PQ (для анализа CO2 и углеводородов). Легкокипящую часть жидких продуктов, выкипающую до 200оС, собирали непосредственно из автоклава вымораживанием жидким азотом в ловушке под вакуумом. Содержимое автоклава экстрагировали бензолом, по количеству нерастворимого остатка определяли степень конверсии сапропеля в жидкие и газообразные продукты.
Обсуждение результатов
Кипячение сапропеля в течение 30 мин. В 10% водном растворе щелочи приводит к растворению более 90% его органической массы. Окисление сапропеля пероксидом водорода в водно – аммиачной среде при комнатной температуре, позволяющее быстро и практически нацело перевести органическое вещество сапропеля в растворимое состояние, протекает ещё быстрее – в течение 15 – 20мин. Получаемые этим способом продукты из бурых углей и других органических субстратов используются в качестве стимуляторов роста сельскохозяйственных культур [11].
На рисунке представлена динамика накопления сиреневого альдегида в процессе каталитического окисления сапропеля молекулярным кислородом в условиях, характерных для получения ароматических альдегидов из лигнинсодержащего сырья [10, 12]. При температуре 170оС процесс окисления протекает достаточно быстро, и максимальный выход сиреневого альдегида достигается за 10 – 15 мин. В таблице 1 представлены результаты, позволяющие сопоставить выходы ароматических альдегидов (ванилин, сиреневый альдегид, пара-гидроксибензальдегид) в процессах окисления сапропеля и других лигнинсодержащих субстратов – соломы, берёзовой о сосновой гнили и древесины, а также лигносульфонатов Сяського ЦБК[12].
Окисление сапропеля протекает с весьма высокой селективностью по сиреневому альдегиду. Ванилин и пара-гидроксибензальдегид содержатся в реакционной смеси в количестве до 10% по отношению к сиреневому альдегиду. Такое соотношение является нехарактерным для продуктов окисления природных лигнинов. Разрушение древесины грибами бурой гнили не оказывает значительного влияния на отношение выходов ароматических альдегидов: соотношение сиреневый альдегид/ванилин составляет 3,04 и 2,3 для берёзовой древесины и берёзовой гнили соответственно (табл. 1 [12]). Проведённое сопоставление полученных результатов и литературных данных указывает на различие механизмов анаэробного (сапропель) и аэробного (бурые гнили) ферментативного разрушения лигнинов. По суммарному выходу альдегидов в расчёте на субстрат сапропель (составляет 2,3 вес.% сиреневого альдегида) близок к соломе (составляет 2,0 вес.%) и значительно уступает лигносульфонатам (составляет 6,1%), используемым в промышленности для производства ванилина, а также сосновой гнили (составляет 13 вес.% ванилина).
В таблице 2 представлены результаты терморастворения сапропеля в нефтяном остатке. Степень конверсии органической массы сапропеля в газообразные и жидкие продукты мало зависит от вариации температуры в интервале 370 – 430оС (изменяется от 68 до 72%). Однако увеличение температуры приводит к возрастанию выхода воды, газов и легкокипящих углеводородных продуктов. Газообразные продукты (табл. 3) более чем на 50% масс. состоят из оксидов углерода. При увеличении температуры процесса наблюдается возрастание выхода газообразных углеводородов.
Полученные результаты показывают, что в условиях термического растворения органическое вещество сапропеля подвергается интенсивной деструкции. Значительную роль в этом процессе играет термический крекинг кислородосодержащих функциональных групп, сопровождающийся образованием оксидов углерода и воды. Увеличение температуры интенсифицирует процессы вторичного превращения образовавшихся высококипящих жидких продуктов в углеводороды с меньшей молекулярной массой.
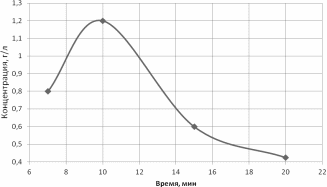
Рисунок 1.2 – Зависимость выхода сиреневого альдегида от продолжительности окисления сапропеля при 170оС, 0,3 МПа кислорода (состав реакционной смеси 3 г сапропеля, 10 г/л гидроксида меди, 60 мл 10%-ного раствора NaOH)
Таблица 2.1 – Каталитическое окисление сапропеля и других субстратов в ароматические альдегиды молекулярным кислородом при 170оС (катализатор Cu(OH)2, парциальное давление кислорода 0,3 МПа)
Субстрат |
Суммарный выход альдегидов, вес.% на субстрат |
Концентрация альдегидов в реакционной массе, г/л |
||
сиреневый альдегид |
ванилин |
n-гидроксибензальдегид |
||
Сапропель |
2,3/5** |
1,2 |
0,1 |
0,05 |
Берёзовая бурая гниль* |
11,2 |
7,0 |
2,3 |
- |
Берёзовая древесина |
8,6 |
3,0 |
1,3 |
- |
Сосновая гниль |
13 |
- |
11,8 |
- |
Солома |
2,0 |
2,4 |
3,3 |
0,8 |
Лигносульфонаты |
6,1 |
1,0 |
11,9 |
- |
*Катализатор отсутствует
**В знаменателе – в расчёте на органическую массу сапропеля
Таблица 2.3 – Влияние температуры терморастворения сапропеля в нефтяном остатке (кипит выше 350оС) на основные показатели процесса
Температура, оС |
Степень конверсии сапропеля в жидкие и газообразные продукты, % масс. |
Выход, % масс на ОМП*. |
|||
газ |
водная фаза |
углеводородная фракция жидких продуктов |
|||
н.к. – 200оС |
>200оС |
||||
370 |
70 |
8 |
4 |
11 |
62 |
400 |
72 |
9 |
6 |
15 |
56 |
430 |
68 |
11 |
6 |
21 |
46 |
*Выход приведён в расчёте на суммарную органическую массу сапропеля и нефтяного остатка.
Таблица 2.4 – Состав газообразных продуктов термического растворения сапропеля в нефтяном остатке
Содержание, % масс. |
Температура процесса, оС |
||
370 |
400 |
430 |
|
СО |
4,1 |
4,8 |
6,1 |
СО2 |
67,5 |
59,1 |
45,3 |
СН4 |
8,5 |
10,0 |
14,8 |
ƩС2 |
9,4 |
12,0 |
17,5 |
ƩС3 |
5,9 |
7,7 |
10,2 |
ƩС4 |
4,6 |
6,4 |
6,1 |
Сопоставление показателей процесса термического растворения сапропеля и бурого угля Канско – Ачинсокого бассейна [10] показывает, что степень конверсии и выход легкокипящих жидких продуктов из сапропеля превышает полученные в сопоставимых условиях значения для бурого угля более чем в 2 раза. Повышенная реакционная способностью сапропеля при терморастворении объясняется отсутствием ароматических структур в его органической массе [10,11] и высоким содержанием в нём термически менее стабильных кислородсодержащих соединений.
