
- •Предисловие
- •Лекция №1 Предмет и задачи курса “История и методология химии”
- •Предмет и задачи курса “История и методология химии”
- •2. Историческое и логическое в обучении химии
- •3. Роль фактического материала в структуре химии, истории и методологии химии, теории и методики обучения химии
- •4. Понятие о концептуальных системах в химии
- •5. Периодизация исторического развития химии
- •Методологические уроки исторического развития химии
- •Структура элементарного и концептуального уровней химии
- •Методология обобщения знаний
- •Взаимосвязь понятий
- •Лекция № 3 Химия в древности и средние века
- •Возникновение химического искусства
- •Натурфилософские учения о первопричинах образования веществ
- •Алхимический период
- •Эпоха возрождения и ее влияние на развитие химии
- •Лекция №4 Химия как самостоятельная область научного знания (вторая половина XVII века – первая половина XVIII века)
- •Развитие химических знаний во второй половине XVII века
- •Возникновение научной химии
- •Химические воззрения Георга Эрнеста Шталя (1659 - 1734)
- •Химия в России в XVIII веке. Вклад м.В.Ломоносова в развитие химии
- •Лекция № 5 Химия на рубеже XVIII и XIX веков (период развития химии как науки об атомах и молекулах)
- •1.Работы а.Л.Лавуазье (1743 – 1794). Новый взгляд на теорию горения
- •2.Работы Клода Луи Бертолле (1748 – 1822г.)
- •Джон Дальтон (1766 - 1844) и его атомное учение
- •Дальнейшее развитие химической атомистики. Работы Гей-Люссака (1778 - 1850) и Авогадро (1776 - 1856)
- •Лекция №6 Возникновение и развитие органической химии
- •1. Возникновение органической химии
- •2. Причины выделения органической химии в самостоятельную науку
- •3. Теоретические представления в органической химии до появления структурной теории строения (доструктурные теории)
- •Теория химического строения органических соединений а.М.Бутлерова
- •Лекция № 7 История открытия периодического закона. Основные этапы развития учения о периодичности
- •1. Попытки классификации химических элементов до д.И.Менделеева
- •2.Предпосылки открытия периодического закона и создания периодической системы д.И.Менделеева
- •3. Открытие д.И.Менделеевым периодического закона и периодической системы
- •4. Триумф периодического закона
- •Лекция № 8 Период развития химии как науки о веществах и их превращениях (вторая половина XIX века)
- •1. Основные направления в развитии органической химии на базе теории химического строения
- •2. Успехи неорганической химии в конце XIX столетия
- •Лекция № 9 Основные направления развития химии в XX веке
- •1. Характерные черты химии хх века.
- •2.Основные направления развития химии хх века
- •Краткие биографии некоторых известных ученых-химиков
3. Теоретические представления в органической химии до появления структурной теории строения (доструктурные теории)
Первые теоретические представления в органической химии берут свое начало от Лавуазье. Согласно его учению, органические вещества можно рассматривать как состоящие из двух частей: кислорода и радикала.
Еще в XVIII веке ученые заметили, что существует сочетание атомов, как бы переходящих в неизменном виде из одного вещества в другое (например, группа – CN-,анион [Fе(CN)6]-3- – и др).
В 30-х годах XIX века Либих и Вёлер установили, что из масла горького миндаля можно получить ряд веществ, в составе которых находиться бензоил (C7H6О – бензальдегид, хлористый бензоил и др.).
В первой половине XIX века господствовала теория радикалов, основоположником которой считали Берцелиуса. Ее называли еще дуалистической, т.к. она рассматривала органические вещества как комбинации двух частей: радикала и простого неорганического остатка, который Берцелиус считал электроотрицательной частью, проводя, таким образом, аналогию с неорганическими веществами.
Органическую химию он определял, как “химию сложных радикалов”, считая их подлинными элементами органической химии.
Он правильно предполагал, что силы, связывающие атомы в веществе, носят электрический характер, но модель этого взаимодействия была неверной: он считал, что атомы имеют два полюса. Частицы из 2-х атомов, в свою очередь, тоже обладают двумя полюсами и могут идти дальнейшие усложнения. Самый электроотрицательный элемент – O, поэтому он не может входить в радикалы.
Теория радикалов помогла правильно подметить существование устойчивых группировок атомов – радикалов. Неверно то, что радикалы абсолютно неизменны. Не укладывались в схему Берцелиуса реакции замещения, в которых Cl- замещался на H+, входящего в состав радикала.
В 1832 году Либих и Вёлер показали, что бензоил соединяется как с положительными, так и с отрицательными частицами.
В конце 40-х годов XIX в. представления Берцелиуса были опровергнуты.
Еще в 20-е годы было открыто несколько соединений одинакового состава, но различных по свойствам. Берцелиус назвал это явление изомерией, которое опровергло положение Лавуазье, что свойства определяются элементарным составом соединений. Французские химики выдвинули предположение, что свойства молекул определяются их пространственным строением: появилась теория механических типов Дюма и Лорана.
В основе ее была ошибочная модель (аналогия с кирпичным зданием). Однако веществ открывалось все больше, и их надо было классифицировать.
Принцип классификации с использованием как идеи типов, так и идеи радикалов был предложен в 50-х годах Д.Жераром. Он рассматривал органические вещества как производные простых неорганических соединений .Выделялись типы водорода, хлороводорода, воды, аммиака. Путем замещения в них водорода на радикалы можно было составить формулы различных классов органических веществ:
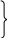
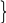
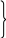 H
H
H
Н
H
H
H
Н
Н Cl О Н N
Н Н
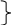
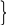
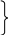 CH3
CH3
СН3
CH3
CH3
СН3
H Cl O
Н
Однако теорию типов Жерара трудно было применить для объяснения реакций присоединения и отщепления, для изображения состава веществ с несколькими функциональными группами: например этаноламин выводили из двух типов:

Н
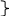 О
О
Н Н О
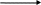 С2Н4
С2Н4
Н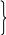
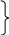 H
H
Н N N
Н Н
Возникла теория многоатомных радикалов и веществ, относящихся к различным типам.
Важным этапом в развитии химии явилось введение понятия «валентность». Эта заслуга принадлежит Франкланду (1852 год). Свои выводы о валентности он сделал при изучении металлоорганических соединений (цинкдиметила, триэтилсурьмы).
Развивая учение о валентности, Кекуле в 1858 г. четко разработал представление о 4-х валентности углерода.
В том же году Купер обратил внимание на то, что атомы углерода в органических веществах могут затрачивать свою валентность не только на связь с другими элементами, но и друг с другом. Он указал на способности углерода образовывать цепи, а также первый стал использовать «-», для обозначения валентности. Его формулы уже напоминают чем-то современные:
С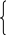 Н3
СН3
СН3
Н3
СН3
СН3
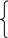 |
Н2
| |
О
|
Н2
| |
О
С СН2 С
ОН | Н2 ОН
С уксусная кислота
этанол ОН
пропанол
Однако, по вопросу о значении формул они оставались на позициях теории типов.
Перечисленные теории не следовали друг за другом, а существовали одновременно, причем наряду с основными теориями было немало еще и разновидностей этих теорий.
