
- •200___ – 200___ Учебный год
- •Аттестационный лист студента Защита модулей
- •Накопительная ведомость
- •Основы количественного анализа. Способы выражения концентрации раствора.
- •Задания для самостоятельной работы
- •Основы количественного анализа.
- •Кислотно – основное титрование.
- •Дата_________ Лабораторная работа № ______
- •Определение массы гидроксида натрия в растворе
- •Расчеты:
- •Задания для самостоятельной работы
- •Химическая термодинамика. Энергетика химических реакций.
- •I начало термодинамики. Энтальпия. Закон Гесса. Дата_________ Лабораторная работа № ______ Определение стандартной энтальпии реакции нейтрализации.
- •Расчеты
- •Энтропия. Химическое равновесие. Задания для самостоятельной работы
- •Химическая кинетика. Дата_________ Лабораторная работа №________ Определение кинетических характеристик реакции окисления иодид-ионов пероксидом водорода.
- •Экспериментальные данные
- •Расчеты Вывод
- •Задания для самостоятельной работы
- •Расчеты Вывод
- •Свойства растворов Дата_________ Лабораторная работа № ________ Криометрическое определение молярной массы неэлектролита
- •Экспериментальные данные
- •Расчеты:
- •Задания для самостоятельной работы
- •Теоретическое и экспериментальное определение рН. Дата_________ Лабораторная работа
- •Экспериментальные данные
- •Свойства буферных растворов. Дата_________ Лабораторная работа Свойства буферных растворов.
- •Экспериментальные данные
- •Расчет рН
- •Экспериментальные данные
- •Гетерогенные процессы. Дата_________ Лабораторная работа Гетерогенные равновесия в растворах электролитов
- •Расчет пс:
- •Расчет пс:
- •Дата_________ Лабораторная работа № _________ Построение изотермы адсорбции уксусной кислоты на угле.
- •Получение и устойчивость дисперсных систем. Дата_________ Лабораторная работа № ______
- •Адсорбция на подвижной и неподвижной границах раздела фаз. Получение и устойчивость дисперсных систем. Задания для самостоятельной работы
- •Ход работы:
- •Задания для самостоятельной работы
- •Дата_________ Лабораторная работа № _________
- •Задания для самостоятельной работы
- •Защита модуля 4 Механизмы реакций в органической химии
- •Биологически важные органические соединения неполимерного характера Дата_________ Лабораторная работа № _________ Свойства гетерофункциональных соединений.
- •Задания для самостоятельной работы
- •Выводы Задания для самостоятельной работы
- •Задания для самостоятельной работы
- •Строение и свойства аминокислот, пептидов и белков. Дата_________ Лабораторная работа № ________
- •Ход работы:
- •Занятие 29
- •Свойства растворов биополимеров
- •Дата_________ Лабораторная работа
- •Свойства растворов вмс. Определение изоэлектрической точки белка по степени набухания.
- •Дата_________ Лабораторная работа № _______ Строение и свойства углеводов
- •Дата_________ Лабораторная работа Нуклеиновые кислоты и их структурные компоненты
- •Дата_________ Лабораторная работа Изучение свойств липидов и их структурных компонентов
Расчеты Вывод
Занятие 8. Защита модуля 1 Химическая термодинамика и химическая кинетика
Дата _________
Ф.И.О. _______________________ группа _______ Билет № ________
Занятие 9
Свойства растворов Дата_________ Лабораторная работа № ________ Криометрическое определение молярной массы неэлектролита
Цель работы: Научиться криометрически определять молярную массу вещества
Приборы, оборудование и реактивы: криометр, термометр Бэкмена, термометр химический, лёд колотый, хлорид натрия, исследуемые растворы сахарозы, мочевины, 0,9% раствор хлорида натрия.
Сущность работы:
Молярная масса неэлектролита определяется по измеренному относительному понижению температуры замерзания раствора по сравнению с чистым растворителем.
Проводится охлаждение заданных растворов до начала образования кристаллов льда. Измерение проводится с помощью термометра Бэкмана. По полученным данным вычисляется понижение температуры замерзания раствора:
DТз=Тз (Н2О) – Тз(р-р),
где Тз – точка замерзания при данной настройке термометра. Рассчитывают молярную массу неэлектролита по формуле:
Ход работы:
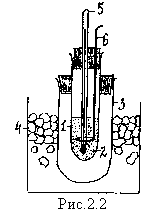
1. Внутренний сосуд криометра 1 (см. рис ) ополаскивают, заполняют дистиллированной водой приблизительно на 1/3 высоты, чтобы обеспечить полное погружение резервуара термометра.
2. Внешний сосуд криометра заполняют толченым льдом, добавляют 40-50 г технической соли, доливают воду до всплывания льда и перемешивают. Температура смеси должна быть около –5° ¾ -6° С. Сосуд с дистиллированной водой помещают в криометр и некоторое время охлаждают, но не до замерзания.
3. Устанавливают заранее настроенный термометр Бэкмана; он не должен касаться стенок сосуда. Непрерывно перемешивают жидкость мешалкой и наблюдают за показаниями термометра. Столбик термометра постепенно опускается, после чего следует резкое повышение температуры, которое достигает максимального значения и стабилизируется (точка замерзания чистого растворителя), или снова понижается (точка замерзания раствора).
4. Записывают соответствующее максимальное показание термометра. Сосуд осторожно приподнимают и слегка нагревают до исчезновения льда. Повторяют определение температуры замерзания воды 2-3 раза.
5. Аналогично проводят определение температуры замерзания исследуемого раствора. При работе с раствором особенно важно интенсивное непрерывное перемешивание, препятствующее сильному переохлаждению жидкости. Наиболее точный результат получается при минимальном количестве образующегося льда.
Экспериментальные данные
Измерения |
Температура замерзания (по шкале термометра Бэкмана) |
|
|
Вода |
Анализируемый раствор |
1 |
|
|
2 |
|
|
3 |
|
|
Среднее значение |
|
|
Справочные величины ___________________________________
Обработка результатов эксперимента
1. Вычисляют значение DТз .
2. Рассчитывают осмоляльность, которая в данном случае (одно растворенное вещество) равна моляльной концентрации.
bосм = b(X) = ΔТз /К(Н2О)
3. Рассчитывают молярную массу неэлектролита по формуле:
1000ω
М(Х) = --------------------------
b(x)(100-ω)
4. Вычисляют относительную ошибку опыта:
