
ЛЕКЦІЯ № 5
ОКИСНО-ВІДНОВНІ ПРОЦЕСИ
ПЛАН
1. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ
2. ОКИСНИКИ
3. ВІДНОВНИКИ
4. МЕТОД ЕЛЕКТРОННОГО БАЛАНСУ
Л І Т Е Р А Т У Р А:
1. Ахметов Н.С. “Общая и неорганическая химия.: Учебник для ВУЗов. – М.: В.школа. – 1981 – 679 с.
2. Басов В.П., Родіонов В.М., Юрченко О.Г. Хімія. Навчальний посібник для самопідготовки до іспитів. К.: Каравела, Львів,: Новий світ – 2000, 2002 – 280с.
3. Глинка Н.Л. Общая химия. Изд. 17,1975, с. 728
4.Рейтер Л.Г., Степаненко О.М., Басов В.П. Теоретичні розділи загальної хімії.: Навчальний посібник.: -К.: Каравела, 2003 - 344 с.
5. Романова Н.В. Загальна та неорганічна хімія. Підручний для студентів вищих навчальних закладів. – К.: Ірпінь. ВТФ “Перун”, 2002 – 480 с.
6. Сегеда А.С. Загальна й неорганічна хімія в тестах, задачах, вправах. Київ: ЦУП, Фітосоціоцентр, 2003 – 592 с.
7. Хомченко И.Г., Сборник задач и упражнений по химии: Учебное пособие для нехимических техникумов.: - М.: В.школа, 1989 – 256 с.
Література: Л.1.(с.214-219), Л.3.(с.261-299), Л.4.(с.234-283), Л.5.(с.182-198), Л.6.(с.242-257), Л.7.(с.50-54), конспект лекції №8.
1. Окисно-відновні реакції
За зміною ступеня окиснення елементів, які входять до складу вихідних речовин та продуктів реакції, хімічні реакції можна поділити на дві групи.
До першої групи належать реакції, що відбуваються без зміни ступенів окиснення елементів. Це реакції подвійного обміну, або витіснення, комплексоутворення, деякі реакції розкладу, реакції ізомеризації, полімеризації, асоціації тощо:
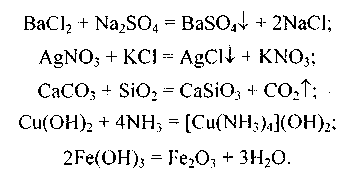
До другої групи належать реакції, що відбуваються із зміною ступенів окиснення елементів реагуючих речовин та продуктів реакції. Такі реакції називаються окисно-відновними, наприклад:
![]()
У процесі цієї реакції ступінь окиснення Цинку змінюється від 0 до +2, а Гідрогену — від +1 до 0. Отже, це окисно-відновна реакція.
Окисно-відновні реакції — одне з найважливіших теоретичних питань, знання якого необхідне для вивчення основних розділів загальної, неорганічної, органічної, аналітичної та фізколоїдної хімії.
Окисно-відновні реакції мають величезне значення, особливо для підтримування життєдіяльності біологічних систем. Процеси фотосинтезу, дихання, травлення — все це ланцюги окисно-відновних реакцій.
Теорія окисно-відновних реакцій вперше була запропонована російськими та українськими вченими С. О. Даїном, Л. В. Писаржевським, Я. І. Михайленком, М. О. Шиловим.
Під час складання рівнянь окисно-відновних реакцій потрібно визначити, скільки електронів приєднує окисник і скільки їх віддає відновник.
Умовно прийнято вважати, що під час окиснення відновник віддає електрони, а під час відновлення — окисник їх приєднує, тобто до уваги не береться будова частинок, природа хімічного зв'язку і механізм процесу. Для спрощення запису ступені окиснення зазначають лише для тих атомів, у яких вони змінюються.
Хоч поняття про ступінь окиснення є формальним і не завжди характеризує стан атомів у сполуках, ним зручно користуватися під час розгляду окисно-відновних реакцій та під час класифікації різних речовин.
Щоб скласти рівняння окисно-відновної реакції, потрібно знати хімічні формули вихідних речовин і продуктів реакції. Продукти реакції визначають експериментальне; іноді їх можна передбачити, врахувавши властивості вихідних речовин. Якщо реакція відбувається в розчині, то в ній може брати участь вода.
Найпоширеніші два методи складання рівнянь окисно-відновних реакцій: метод електронного балансу та йонно-електронний метод. Обидва методи ґрунтуються на положенні, що в окисно-відновних процесах загальне число електронів, які віддає відновник, дорівнює загальному числу електронів, які приєднує окисник.
2. Окисники
Р![]() ечовини,
до складу молекул яких входять атоми,
здатні приєднувати електрони,
тобто знижувати свій ступінь окиснення,
називаються окисниками.
До
окисників належать кисень, вільні
галогени, сірка, оскільки вони мають
велику
електронегативність. Окисниками є також
різні сполуки галогенів
ечовини,
до складу молекул яких входять атоми,
здатні приєднувати електрони,
тобто знижувати свій ступінь окиснення,
називаються окисниками.
До
окисників належать кисень, вільні
галогени, сірка, оскільки вони мають
велику
електронегативність. Окисниками є також
різні сполуки галогенів
з![]() позитивними
ступенями окиснення:
позитивними
ступенями окиснення:
До
активних окисників належать також
нітратна кислота, концентрована сульфатна
кислота, солі металів із вищими ступенями
окиснення![]()
![]() пероксиди
(N3^02, КО2),
оксиди металів
пероксиди
(N3^02, КО2),
оксиди металів
з
вищими ступенями окиснення![]()
