
задачи колды
.pdf1.Рассчитайте удельную поверхность адсорбента по изотерме адсорбции азота, используя уравнение БЭТ. Площадь, занимаемая молекулой азота в плотном монослое, составляет 16·10-20
м2. |
3 |
2.В таблице приведены данные по адсорбции паров воды макропористым адсорбентом при комнатой температуре. Пользуясь уравнением Ленгмюра определите емкость адсорбционного
монослоя: |
3 |
3.Рассчитайте время половинной коагуляции аэрозоля с дисперсностью частиц 2,5·108 м-1 и концентрацией 1,2 г/м3, если константа быстрой коагуляции Смолуховского равна 2·10-19 м3/с.
Плотность частиц аэрозоля примите равной 2200 кг/м3. |
4 |
4.По результатам измерения адсорбции на активированном угле рассчитайте удельную поверхность адсорбента (величина адсорбции указана в расчете на азот при нормальных условиях): 4
5.Используя уравнение Эйнштейна, рассчитайте вязкость золя AgCl, имеющего концентрацию 10% массовых и содержащего сферические частицы. Плотность AgCl: 5,56·103 кг/м3; вязкость и плотность дисперсионной среды составляют 1·10-3 Па·с и 1000 кг/м3 соответственно. 5
6.Для отрицательно заряженного гидрозоля Al2S3, порог коагуляции при добавленном КСl равен 49 ммоль/л. Используя закон Дерягина, рассчитайте пороги коагуляции для таких электролитов как
Na2SO4, MgCl2 и AlCl3. |
5 |
7.Электрофорез дисперсии бентонитовой глины происходит при следующих условиях: расстояние между электродами 32 см, напряжение 120 В, за 15 минут частицы переместились на 11 мм к
аноду. Рассчитайте ζ-потенциал, учитывая, что ε = 78,2, а η = 10-3 Па·с. |
6 |
8.Используя гипсометрический закон, рассчитайте для золя SiO2 высоту, на которой концентрация частиц уменьшится в е раз. Принять, что форма частиц сферическая, удельная поверхность дисперсной фазы 108 м-1, плотность SiO2 2,2 г/cм3, плотность дисперсионной среды 1 г/cм3,
|
температура 20 ºС. |
6 |
9. |
Определите поверхностную и полную (внутреннюю) энергию 15 г водяного тумана, имеющего |
|
|
частицы с удельньной поверхностью 100 м2 |
/г; t = 20ºC, σ = 72 мДж/м2; dσ/dT = - 0,16 мДж/ |
|
(м2·К); ρ = 1000 кг/м3. |
7 |
10. |
Определите диаметр капилляра, если хлороформ поднялся в нем на выосту 12,3 см. σ = 27 мДж/ |
|
|
м2; Δρ = 1490 кг/м3, Θ = 0 ºC. |
7 |
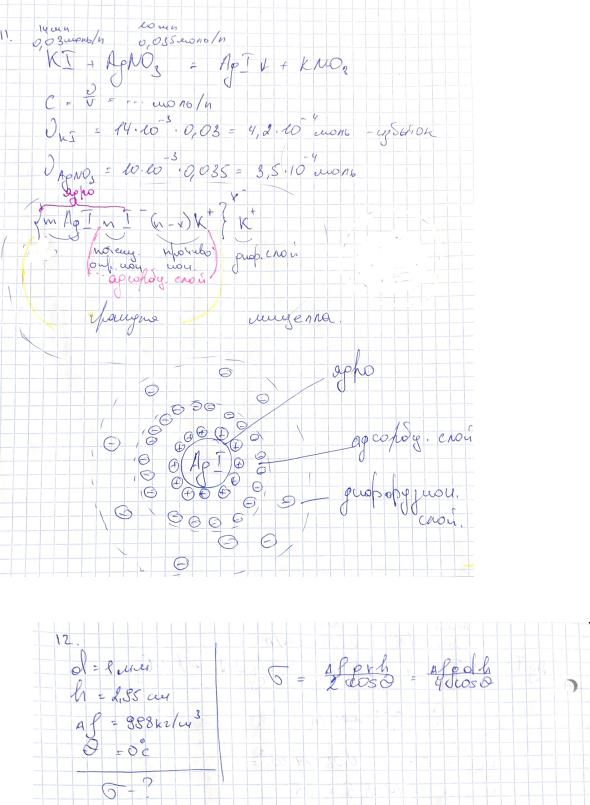
11.Гидрозоль AgI получен добавлением 14 мл КI с концентрацией 0,03 моль/л к 10 мл раствора AgNO3 с концентрацией 0,035 моль/л. Напишите формулу мицеллы образовавшегося золя и
объясните строение ДЭС. |
8 |
12. Рассчитайте поверхностное натяжение воды, если известно, тго в капилляре диаметром 1 мм она
поднимается на высоту 2,95 см. Δρ = 998 кг/м3, Θ = 0 ºС. |
8 |
13.Растворенное в воде ПАВ адсорбируется на поверхности раздела вода-ртуть и соответствии с уравнением Ленгмюра. При этом, при концентрация ПАВ 0,2 моль/л, степень заполнения поверхности равна 0,5. Рассчитайте значение межфазного поверхностного натяжения на границе ртуть-раствор при 25 ºС и СПАВ = 0,1 моль/л, учитывая, что в отсутствие ПАВ поверхностное натяжение составляет 0,375 Дж/м2, а площадь, занимаемая молекулой ПАВ в монослое равна
20·10-20 м2. |
9 |
14.Определите удельную поверхность (м2/г) монодисперсного порошка оксида алюминия, если известно, что его частицы сферической формы оседают в водной среде с высоты 20 см за 1600 секунд. Плотность оксида алюминия равна 4 г/см3, плотность и вязкость воды составляют 1 г/см3
и 10-3 Па·с, соотвстственно. |
9 |
15.Рассчитайте концентрацию частиц гидрозоля золота через 300 с от начала быстрой коагуляции, если начальная концентрация составляла 2·1015 частиц/м3; вязкость дисперсионной среды 10-3
Па·с при 25 ºС. |
10 |
16. Используя уравнение Гуи-Чепмена, рассчитайте значение потенциала на расстоянии 10 и 30 нм от
поверхности (пренебрегая толщиной слоя Гельмгольца). Дисперсионная среда - водный раствор ZnCl2 с концентрацией 10-4 моль/л (индифферентный электролит), t = 20 ºС, ε = 80,1; потенциал
диффузного слоя 45 мВ. |
10 |
17.Рассчитайте ζ-потенциал по данным электроосмоса через корундовую (Аl2О3) мембрану: при силе тока 0,015 A за 70 секунд перенесено 1,5 мл раствора, удельная электропроводимость которого χV = 0,013 См·м-1, поверхностная проводимость χS = 0,006 См·м-1, η = 10-3 Па·с, ε =
81, ε0 = 8,85·10-12 Ф/м. |
11 |
18.Рассчитайте толщину диффузной части ДЭС частиц гидрозоля AgI при 25 ºС. Дисперсионная среда золя (ε = 77) содержит Ва(NО3)2 (М = 261) с концентрацией 50 г/м3. Во сколько раз изменится толщина диффузной части, если концентрацию Ba(NO3)2 повысить в 4 раза? 11
19.Используя данные по адсорбции этана на поверхности однородной графитированной сажи при
постоянной степени заполнения, рассчитайте изостерическую теплоту адсорбции: |
12 |
20.Рассчитайте разность уровней воды в двух сообщающихся капиллярах диаметрами 0,1 и 0,3 мм при 20 ºС. Поверхностное натяжение и плотность воды составляют соответственно 72,75 мДж/м2
и 0,998 г/см3. |
13 |
21.Рассчитайте избыточное давление внутри капель воды и равновесное давление пара при 20 ºС для аэрозоля с удельной поверхностью 108 м-1. Поверхностное натяжение воды 73 мДж/м2,
плотность 1 г/см3, PS = 2306 Па. |
13 |
22.Рассчитайте численную концентрацию золя Al2O3, если известно, что его массовая концентрация равна 0,3 кг/м3. Коэффициент диффузии частиц 2·10-6 м2/сутки, плотность Al2O3 4 г/см3,
|
вязкость среды 10-3 Па·с, температура 25ºС. |
14 |
23. |
Рассчитайте работу адгезии и коэффициент растекания для системы вода-графит, если известно, |
|
|
что краевой угол равен 90 º, а поверхностное наятжение воды 72 мДж/м2. |
14 |
24. |
Найдите графически время половинной коагуляции и начальную концентрацию частиц по |
|
|
изменению общей концентрации частиц лиофобной дисперсной системы: |
15 |
25.Рассчитайте межфазное натяжение в системе CaF2-вода, если известно, что растворимость частиц CaF2 диаметром 0,3 мкм превышает нормальную растворимость на 18% при 20ºС. Плотность
частиц CaF2 составляет 2500 кг/м3, а молярная масса – 78 г/моль. |
15 |
26.Какую долю составляет давление паров воды в капиллярах радиусом 0,1 и 0,01 мкм от нормального давления насыщенного пара при 25 ºС? При расчетах примите, что краевой угол равен нулю; поверхностное натяжение воды 71,96 мДж/м2, плотность воды 998 кг/м3. 16
27.Используя уравнение Дубинина-Радушкевича, рассчитайте объем микропор 1кг сажи на основе
данных об адсорбции паров бензола (мольный объем бензола 88,8 см3/моль): |
17 |
28.Для гидрозоля, содержащего положительно заряженные частицы гидроксиде алюминия порог быстрой коагуляции при добавлении равен 41 ммоль/л. Используя закон Дерягина, рассчитайте
порог коагуляции для электролитов |
17 |
29.Коэффициент диффузии частиц золя серебра в воде при 25ᵒС равен м2/сутки. Рассчитайте дисперность частиц золя и их среднеквадратичный сдвиг за 10 с. Вязкость воды при 25ᵒС равна
Па с. |
18 |
30.Удельная поверхность непористой сажи составляет 80,5 м2/г. Используя уравнение Ленгмюра, определите площадь, занимаемую молекулой бензола в плотном мономлое, исходя из данных об
адсорбции паров бензола на этом адсорбенте при 20ᵒС: |
18 |
31. Используя уравнение Гуи-Чепмена, рассчитайте значение потенциала на расстоянии 20 и 40 нм от поверхности (пренебрегая толщиной слоя Гельмгольца). Дисперсионная среда - водный раствор ZnCl2 с концентрацией 0,3 ммоль/л (индифферентный электролит), t = 20 ºС, ε = 80,1; потенциал
диффузного слоя 28 мВ |
19 |
32.Для гидрозоля, содержащего отрицательно заряженные частицы порог быстрой коагуляции при добавлении равен 31 ммоль/л. Используя закон Дерягина, рассчитайте порог коагуляции для
электролитов |
19 |

1.Рассчитайте удельную поверхность адсорбента по изотерме адсорбции азота, используя уравнение БЭТ. Площадь, занимаемая молекулой азота в плотном монослое, составляет 16·10-20 м2.
p/ps |
0,0286 |
0,136 |
0,200 |
|
|
|
|
A, моль/кг |
2,16 |
3,02 |
3,33 |
|
|
|
|
2.В таблице приведены данные по адсорбции паров воды макропористым адсорбентом при комнатой температуре. Пользуясь уравнением Ленгмюра
определите емкость адсорбционного монослоя:
P·10-3, Па |
А, моль/кг |
|
|
4,68 |
6,28 |
|
|
7,72 |
9,22 |
|
|
17,77 |
14,89 |
|
|
!

3.Рассчитайте время половинной коагуляции аэрозоля с дисперсностью частиц 2,5·108 м-1 и концентрацией 1,2 г/м3, если константа быстрой коагуляции Смолуховского равна 2·10-19 м3/с. Плотность частиц аэрозоля примите равной 2200 кг/м3.
!
4.По результатам измерения адсорбции на активированном угле рассчитайте удельную поверхность адсорбента (величина адсорбции указана в расчете на азот
при нормальных условиях):
P·10-2, Па |
А·103, м3/кг |
|
|
1,85 |
5,06 |
|
|
4,01 |
9,90 |
|
|
68,80 |
40,83 |
|
|
!

5.Используя уравнение Эйнштейна, рассчитайте вязкость золя AgCl, имеющего концентрацию 10% массовых и содержащего сферические частицы. Плотность AgCl: 5,56·103 кг/м3; вязкость и плотность дисперсионной среды составляют 1·10-3 Па·с и 1000 кг/м3 соответственно.
!
6.Для отрицательно заряженного гидрозоля Al2S3, порог коагуляции при добавленном КСl равен 49 ммоль/л. Используя закон Дерягина, рассчитайте пороги коагуляции для таких электролитов как Na2SO4, MgCl2 и AlCl3.

7.Электрофорез дисперсии бентонитовой глины происходит при следующих условиях: расстояние между электродами 32 см, напряжение 120 В, за 15 минут частицы переместились на 11 мм к аноду. Рассчитайте ζ-потенциал, учитывая, что
ε = 78,2, а η = 10-3 Па·с.
!
8.Используя гипсометрический закон, рассчитайте для золя SiO2 высоту, на которой концентрация частиц уменьшится в е раз. Принять, что форма частиц сферическая, удельная поверхность дисперсной фазы 108 м-1, плотность SiO2 2,2 г/ cм3, плотность дисперсионной среды 1 г/cм3, температура 20 ºС.
!

9.Определите поверхностную и полную (внутреннюю) энергию 15 г водяного тумана, имеющего частицы с удельньной поверхностью 100 м2 /г; t = 20ºC, σ = 72 мДж/м2; dσ/dT = - 0,16 мДж/(м2·К); ρ = 1000 кг/м3.
!
10.Определите диаметр капилляра, если хлороформ поднялся в нем на выосту 12,3 см.
σ = 27 мДж/м2; Δρ = 1490 кг/м3, Θ = 0 ºC.
!
11.Гидрозоль AgI получен добавлением 14 мл КI с концентрацией 0,03 моль/л к 10 мл раствора AgNO3 с концентрацией 0,035 моль/л. Напишите формулу мицеллы образовавшегося золя и объясните строение ДЭС.
12.Рассчитайте поверхностное натяжение воды, если известно, тго в капилляре диаметром 1 мм она поднимается на высоту 2,95 см. Δρ = 998 кг/м3, Θ = 0 ºС.
!

13.Растворенное в воде ПАВ адсорбируется на поверхности раздела вода-ртуть и соответствии с уравнением Ленгмюра. При этом, при концентрация ПАВ 0,2 моль/ л, степень заполнения поверхности равна 0,5. Рассчитайте значение межфазного поверхностного натяжения на границе ртуть-раствор при 25 ºС и СПАВ = 0,1 моль/л, учитывая, что в отсутствие ПАВ поверхностное натяжение составляет 0,375 Дж/м2, а площадь, занимаемая молекулой ПАВ в монослое равна 20·10-20 м2.
!
14.Определите удельную поверхность (м2/г) монодисперсного порошка оксида алюминия, если известно, что его частицы сферической формы оседают в водной среде с высоты 20 см за 1600 секунд. Плотность оксида алюминия равна 4 г/см3, плотность и вязкость воды составляют 1 г/см3 и 10-3 Па·с, соотвстственно.

15.Рассчитайте концентрацию частиц гидрозоля золота через 300 с от начала быстрой коагуляции, если начальная концентрация составляла 2·1015 частиц/м3; вязкость дисперсионной среды 10-3 Па·с при 25 ºС.
!
16.Используя уравнение Гуи-Чепмена, рассчитайте значение потенциала на расстоянии 10 и 30 нм от поверхности (пренебрегая толщиной слоя Гельмгольца). Дисперсионная среда - водный раствор ZnCl2 с концентрацией 10-4 моль/л (индифферентный электролит), t = 20 ºС, ε = 80,1; потенциал диффузного слоя 45 мВ.
