
- •Вопросы к занятию
- •Вопросы к занятию
- •Пути поступления токсических веществ в организм.
- •Вопросы к занятию
- •Ход занятия
- •Ход занятия
- •Ход занятия
- •Ход занятия
- •Ход занятия
- •Ход занятия
- •Составление заключения эксперта
- •Вопросы к коллоквиуму
- •Ход занятия
- •Ход занятия
- •Методика фотометрического определения папаверина (аминазина) в биожидкостях
- •Методика количественного определения хинина в биожидкостях
- •Методика спектрофотометрического определения производных барбитуровой кислоты в биожидкостях
- •Вопросы к занятию
- •Занятие №16. Экзамен по практическим навыкам.
- •Литература
Ход занятия
Контроль исходного уровня знаний
Правила работы на спектрофотометре, фотоэлектроколориметре и флуориметре.
Основные требования, предъявляемые к методам количественного определения токсических веществ в биологических жидкостях.
Применение физико-химических методов в химико-токсикологическом анализе.
Лабораторная работа
Методика фотометрического определения папаверина (аминазина) в биожидкостях
В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл воды очищенной, перемешивают. Фильтруют в мерную колбу вместимостью 25 мл, прибавляют 1 мл 0,1% раствора поливинилового спирта (ПВС), 1 мл 0,07% раствора эозина, 2 мл 0,01 М раствора серной кислоты и доводят водой до метки. Параллельно готовят раствор сравнения, содержащий все реактивы за исключением определяемых соединений.
Для приготовления раствора стандартного образца в мерную колбу вместимостью 25 мл помещают 2 мл стандартного раствора папаверина (аминазина) - 10 мкг/мл, прибавляют вышеуказанные реактивы и доводят водой до метки. Измеряют оптическую плотность раствора на ФЭКе при длине волны 540 нм, в кювете с толщиной слоя 2 см относительно раствора сравнения. Концентрацию папаверина (аминазина) в мкг/мл рассчитывают по формуле:
![]()
где АХ – оптическая плотность анализируемого раствора;
где АСТ – оптическая плотность стандартного раствора.
Методика количественного определения хинина в биожидкостях
В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл 0,01 М раствора серной кислоты, встряхивают 5 минут и фильтруют в пенициллиновый флакон. В качестве стандарта используют раствор хинина с концентрацией 1 мкг/мл. Измеряют интенсивность флуоресценции анализируемого и стандартного растворов. Концентрацию хинина в мкг/мл в анализируемой биожидкости рассчитывают по формуле:
![]()
где IХ – интенсивность флуоресценции анализируемого раствора;
где IСТ - интенсивность флуоресценции стандартного раствора.
Методика спектрофотометрического определения производных барбитуровой кислоты в биожидкостях
В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл воды очищенной. Встряхивают 5 минут. Фильтруют в пенициллиновый флакон. В кювету спектрофотометра с толщиной слоя 1 см помещают фильтрат и добавляют 3 капли 0,2 М раствора серной кислоты. Перемешивают. Измеряют оптическую плотность раствора при 240 нм. В качестве раствора сравнения используют воду очищенную. Затем в кювету с анализируемым раствором прибавляют 3 капли 30% спиртового раствора NaOH, перемешивают и измеряют оптическую плотность. В качестве раствора сравнения используют воду очищенную. Аналогично измеряют оптическую плотность стандартного раствора барбитала с концентрацией 10 мкг/мл. Концентрацию барбитуратов (мкг/мл) в анализируемой биологической жидкости рассчитывают по формуле:
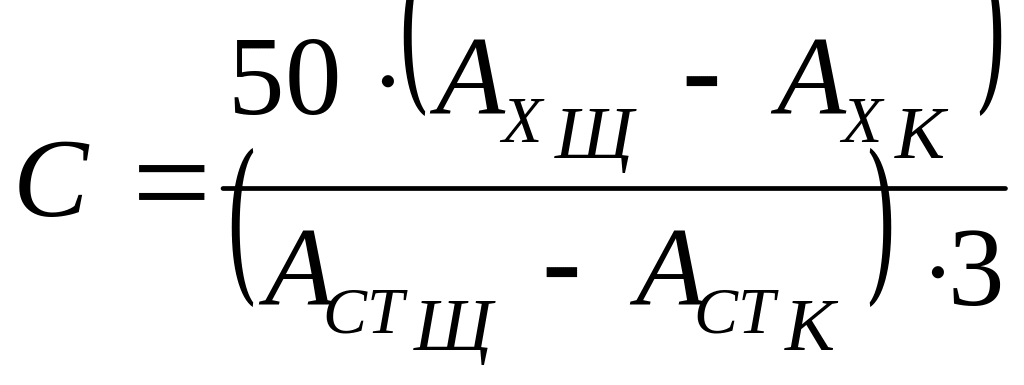
где
![]() и
и
![]() -
оптические плотности анализируемого
раствора в щелочной и кислой средах;
-
оптические плотности анализируемого
раствора в щелочной и кислой средах;
где
![]() и
и
![]() -
оптические плотности стандартного
раствора в щелочной и кислой средах;
-
оптические плотности стандартного
раствора в щелочной и кислой средах;
ЗАНЯТИЕ №14. Изолирование, обнаружение, количественное определение и метаболизм пестицидов
Цель занятия: изучить методы химико-токсикологического анализа и основные пути метаболизма некоторых ядохимикатов.
