
- •Конспект лекций по физике
- •Раздел 2 Молекулярная физика и термодинамика
- •Основы молекулярно-кинетической теории. Термодинамика
- •Основы молекулярно-кинетической теории. Основные положения молекулярно-кинетической теории. Сила и энергия взаимодействия молекул. Шкалы измерения температуры
- •Сила и энергия взаимодействия молекул
- •Контрольные вопросы:
- •Идеальный газ. Давление газа. Основное уравнение молекулярно-кинетической теории идеального газа
- •Контрольные вопросы:
- •Зависимость давления газа от температуры при постоянном объеме. Температура как мера средней кинетической энергии движения молекул
- •Связь между абсолютной температурой и кинетической энергией поступательного движения молекул
- •Контрольные вопросы:
- •Уравнение Клапейрона - Менделеева. Закон Дальтона
- •Количество молекул в 1 моле любого вещества одинаково и называется числом Авогадро:
- •2. 1 Моль любого газа при нормальных условиях занимает объём 22,4 дм3. (закон Авогадро).
- •Контрольные вопросы:
- •Изопроцессы и их графики
- •Контрольные вопросы:
- •Выберете правильный ответ на поставленный вопрос
- •Закон Максвелла о распределении молекул идеального газа по скорости и энергии теплового движения
- •Контрольные вопросы:
- •Барометрическая формула. Распределение Больцмана
- •Контрольные вопросы:
- •Реальные газы. Уравнение Ван-дер-Ваальса
- •Изотермы Ван-дер-Ваальса и их анализ. Критическое состояние вещества
- •Контрольные вопросы:
- •Среднее число столкновений и средняя длина свободного пробега молекул
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленный вопрос
- •Основы термодинамики Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы
- •Изменение внутренней энергии тела в процессе теплообмена и совершения работы. Уравнение теплового баланса
- •Уравнение теплового баланса
- •Контрольные вопросы:
- •Первое начало термодинамики. Адиабатный процесс
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленный вопрос
- •Работа газа. Круговой процесс. Кпд кругового процесса Работа газа при изменении объема
- •Контрольные вопросы:
- •Принцип действия тепловой машины. Цикл Карно
- •Кпд тепловой машины
- •Контрольные вопросы:
- •Необратимые процессы. Понятие о втором начале термодинамики
- •Контрольные вопросы:
- •Явления переноса в термодинамически неравновесных системах
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленные вопросы:
- •Агрегатные состояния вещества и фазовые переходы
- •Свойства паров. Влажность воздуха. Способы определения влажности воздуха. Парообразование
- •Влажность воздуха. Точка росы. Способы определения влажности
- •Приборы для определения влажности воздуха
- •Контрольные вопросы:
- •Кипение.
- •Контрольные вопросы:
- •Характеристика жидкого состояния вещества.
- •Молекулярное давление поверхностного слоя жидкости
- •Энергия поверхностного слоя жидкости.
- •Поверхностное натяжение
- •Смачивание
- •Капиллярность
- •Контрольные вопросы:
- •Кристаллическое состояние вещества. Типы связей в кристаллах, виды кристаллических структур
- •Полиморфизм
- •Применение кристаллов
- •Жидкие кристаллы
- •Контрольные вопросы:
- •Механические свойства твердых тел
- •Закон Гука. Модуль упругости
- •Диаграмма растяжения твердого тела
- •Контрольные вопросы:
- •Тепловое расширение твердых тел.
- •Плавление и кристаллизация. Диаграмма фазовых состояний
- •Контрольные вопросы:
Сила и энергия взаимодействия молекул
При рассмотрении реальных газов
следует учитывать силы межмолекулярного
взаимодействия. Они появляются на
расстоянии, меньшем, чем 10-9м. Между
молекулами вещества одновременно
действует силы притяжения
![]() и силы отталкивания
и силы отталкивания
![]() (см. рисунок 1а). Силы отталкивания
положительные,
а силы притяжения
–
отрицательные. Результирующая сила
(см. рисунок 1а). Силы отталкивания
положительные,
а силы притяжения
–
отрицательные. Результирующая сила
![]() этих двух сил является силой отталкивания
на участке от 0 до
этих двух сил является силой отталкивания
на участке от 0 до
![]() и силой притяжения при 10-9м>
и силой притяжения при 10-9м>
![]() >
.
При расстоянии
=
равнодействующая сила
>
.
При расстоянии
=
равнодействующая сила
![]() =0.
Таким образом, расстояние
соответствует устойчивому состоянию
молекулы. На этом расстоянии и находились
бы молекулы в отсутствие теплового
движения. На расстоянии
>10-9м
межмолекулярные силы также практически
отсутствуют.
=0.
Таким образом, расстояние
соответствует устойчивому состоянию
молекулы. На этом расстоянии и находились
бы молекулы в отсутствие теплового
движения. На расстоянии
>10-9м
межмолекулярные силы также практически
отсутствуют.
Элементарная работа
![]() силы
при увеличении расстояния между
молекулами на
силы
при увеличении расстояния между
молекулами на
![]() совершается за счет уменьшения взаимной
потенциальной энергии молекул:
совершается за счет уменьшения взаимной
потенциальной энергии молекул: ![]() .
.
При >10-9м силы отсутствуют и потенциальная энергия равна 0. взаимодействия молекул (см. рисунок 1б).
П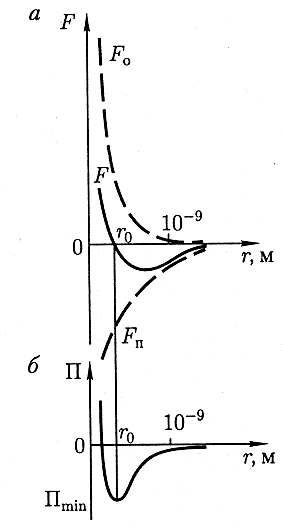 ри
сближении молекул на расстояние меньшее
чем 10-9м, появляется сила притяжения
(
<0),
которая совершает положительную работу
(
ри
сближении молекул на расстояние меньшее
чем 10-9м, появляется сила притяжения
(
<0),
которая совершает положительную работу
(![]() >0).
Поэтому потенциальная энергия уменьшается,
достигая минимума
>0).
Поэтому потенциальная энергия уменьшается,
достигая минимума
![]() при расстоянии
=
.
при расстоянии
=
.
![]() определяет работу, которую нужно
совершить против сил притяжения чтобы
разъединить молекулы.
определяет работу, которую нужно
совершить против сил притяжения чтобы
разъединить молекулы.
При расстоянии < действуют силы отталкивания и совершаемая против них работа отрицательна ( <0). Потенциальная энергия начинает резко возрастать. Таким образом, система из двух молекул в состоянии устойчивого равновесия
Рисунок 1. Силы и энергия взаимодействия молекул
(при = ) обладает минимальной потенциальной энергией (потенциальной ямой).
Критерием различных агрегатных
состояний вещества является соотношение
и произведением
![]() ,
где коэффициент
,
где коэффициент
![]() – постоянная Больцмана (
=1,38
– постоянная Больцмана (
=1,38![]() ),
),
![]() - абсолютная температура.
- абсолютная температура.
Произведение определяет удвоенную среднюю энергию, приходящуюся на одну степень свободы теплового движения молекулы.
Если << , то вещество находится в газообразном состоянии.
Если >> , то вещество находится в твердом состоянии.
Если » , то вещество находится в жидком состоянии, т.к. в результате теплового движения молекулы перемещаются в пространстве, обмениваясь местами, но, не расходясь на расстояние, превышающее r0.
Внутренняя энергия тела
является суммой
кинетической энергии всех его молекул
![]() и потенциальной энергии их взаимодействия.
и потенциальной энергии их взаимодействия.
Контрольные вопросы:
Изложите основные положения молекулярно-кинетической теории.
Что такое температура, и какие температурные шкалы Вам известны?
Что такое диффузия? Приведите примеры диффузии в газах, жидкостях и твердых телах.
Расскажите о силе взаимодействия молекул.
Расскажите о кинетической и потенциальной энергии молекул.
Идеальный газ. Давление газа. Основное уравнение молекулярно-кинетической теории идеального газа
Для упрощения рассмотрения процессов в газах можно пренебречь взаимодействием молекул газа, т.к. оно не оказывает существенного влияния на поведение молекул. Немецкий физик Клаузиус ввел понятие идеального газа, в котором:
Объемом всех молекул газа можно пренебречь по сравнению с объемом сосуда, в котором этот газ находится.
Время столкновения молекул друг с другом пренебрежимо мало по сравнению со временем между двумя столкновениями (т.е. со временем свободного пробега молекул).
Молекулы взаимодействуют между собой только при непосредственном соприкосновении, при этом они отталкиваются.
Силы притяжения между молекулами идеального газа ничтожно малы, и ими можно пренебречь.
Реальный газ при нормальном давлении очень близок по свойствам к идеальному газу. Значительное повышение давления газа приводит к существенному уменьшению среднего расстояния между молекулами и поэтому реальный газ уже нельзя считать идеальным. Так при давлении 500 МПа объем молекул составит половину занимаемого газом объема.
Давление газа.
Молекулы газа, ударяясь о поверхность
тела (например, о стенку сосуда), оказывают
на нее давление. Давление
![]() ,
где
,
где
![]() – сила давления,
– сила давления,
![]() – площадь поверхности тела.
– площадь поверхности тела.
Единица измерения давления в системе СИ:
![]()
Существуют и другие единицы измерения давления. Наиболее распространенными из них являются атмосфера и миллиметр ртутного столба.
Техническая атмосфера
- давление, оказываемое силой 1 кгс на
площадь 1
![]() .
1
.
1![]() .
.
Миллиметр ртутного столба
(![]() )
– это давление, оказываемое столбом
ртути высотой 1мм. на горизонтальную
поверхность. Давление внутри жидкости
на глубине h:
)
– это давление, оказываемое столбом
ртути высотой 1мм. на горизонтальную
поверхность. Давление внутри жидкости
на глубине h:
![]() .
1мм.рт.ст. =
.
1мм.рт.ст. =
![]() =133
Па
=133
Па
Прибор для измерения давления
называется манометром.
![]()
О
Рисунок 2. Движение
молекулы массой
![]() со скоростью
со скоростью
![]()
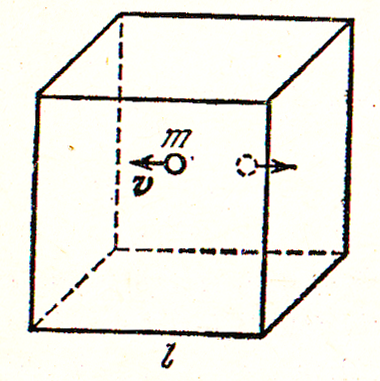
![]() (рисунок 2). В каждой единице объема куба
содержится
(рисунок 2). В каждой единице объема куба
содержится
![]() одинаковых молекул
газа. Общее число молекул в кубе
одинаковых молекул
газа. Общее число молекул в кубе
![]() .
Будем считать удары молекул о стенки
сосудов абсолютно упругими. Каждая
молекула обладает количеством движения
(импульсом) p=
.
Будем считать удары молекул о стенки
сосудов абсолютно упругими. Каждая
молекула обладает количеством движения
(импульсом) p=![]() ,
где
,
где
![]() - масса молекулы, а
- масса молекулы, а
![]() - скорость её движения. В процессе удара
импульс меняется на величину
- скорость её движения. В процессе удара
импульс меняется на величину
![]() 2
2![]() ,
и, следовательно, стенка получает импульс
силы
,
и, следовательно, стенка получает импульс
силы
![]() =2
.
=2
.
Средняя сила воздействия одной
молекулы на стенку равна:
![]() ,
где
,
где
![]() - время движения молекулы от одной стенки
к другой и обратно.
- время движения молекулы от одной стенки
к другой и обратно.
![]() .
.
Отсюда:
![]() .
.
Сила давления газа на стенку куба равна
сумме сил ударов
![]() отдельных молекул об эту стенку:
отдельных молекул об эту стенку:
![]() .
.
Величина
![]() - называется среднеквадратической
скоростью
- называется среднеквадратической
скоростью![]() .
.
Отсюда:
=![]() и
и
![]()
![]() где:
где:
— число молекул, летающих между двумя
противоположными стенками куба. Поскольку
в кубе три пары таких стенок, то в одном
из трех взаимно перпендикулярных
направлений движется
![]() общего
числа молекул.
общего
числа молекул.
Отсюда:
![]() и тогда:
и тогда:
![]()
Поскольку: ![]() ,
а средняя кинетическая энергия
поступательного движения молекулы
,
а средняя кинетическая энергия
поступательного движения молекулы
![]()
![]() ,
отсюда: - - основное
уравнение молекулярно-кинетической
теории газов: давление
газа прямо пропорционально средней
кинетической энергии поступательного
движения его молекул и числу молекул в
единице объема.
,
отсюда: - - основное
уравнение молекулярно-кинетической
теории газов: давление
газа прямо пропорционально средней
кинетической энергии поступательного
движения его молекул и числу молекул в
единице объема.
Поскольку
![]() - плотность газа, то
- плотность газа, то
![]() - уравнение Клаузиуса.
- уравнение Клаузиуса.
