
- •Предисловие
- •Введение
- •Литература
- •Тема: основы химической термодинамики, термохимии. Определение теплоты растворения вещества
- •Учебно-целевые вопросы
- •Краткая теоретическая часть Основные понятия, определения, законы
- •Классификация термодинамических систем
- •I закон термодинамики
- •Стандартные условия (с.У.):
- •Э нтальпия реакции равна разности алгебраической суммы энтальпий сгорания исходных веществ и суммы энтальпий сгорания продуктов реакции с учетом их стехиометрических коэффициентов.
- •Нормальные величины суточной потребности в энергии для городского населения в зависимости от рода деятельности (данные Института питания амн ссср)
- •II закон термодинамики
- •Математическая форма второго начала термодинамики для изолированных систем:
- •Изменение знака g при изменении знаков н и s
- •В заимосвязь термодинамических величин
- •Особенности термодинамики биохимических процессов
- •Принцип энергетического сопряжения биохимических реакций
- •Многостадийность, обратимость
- •Гомеостаз
- •Обучающие тесты с решением
- •Обучающие задачи с решением
- •Учебно-исследовательская лабораторная работа « Определение теплового эффекта процесса растворения безводной соли»
- •Контрольные вопросы для защиты экспериментальной работы
- •Учебно-исследовательская лабораторная работа «Определение энтальпии нейтрализации»
- •Контрольные вопросы для защиты экспериментальной работы.
- •Краткая теоретическая часть Основные понятия, определения, формулы
- •Природа реагирующих веществ
- •Концентрация реагентов
- •Давление
- •Влияние величины поверхности соприкосновения реагирующих веществ
- •Влияние катализатора
- •Общие принципы катализа
- •Механизм действия катализатора
- •Суть механизма гомогенного катализа
- •Особенности механизма гетерогенного катализа
- •Ферментативный катализ
- •Особенности ферментативного катализа
- •Обучающие тесты с решением
- •Обучающие задачи с решением
- •« Химическая кинетика. Катализ»
- •Контрольные вопросы для защиты экспериментальной работы
- •Тема: химическое равновесие
- •Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Смещение химического равновесия
- •Способы смещения равновесия
- •Обучающие тесты с решением
- •Обучающие задачи с решением
- •« Химическое равновесие»
- •Контрольные вопросы для защиты экспериментальной работы
- •Задачи для самостоятельного решения
- •Тематика рефератов
- •Приложение
- •Основные термодинамические и кинетические величины
- •Термодинамические свойства некоторых веществ, применяемых в медицине
- •3. Теплоты сгорания (н , кДж/моль) некоторых веществ
- •4. Средняя удельная теплота полного окисления основных компонентов пищевых продуктов
- •5. Периоды полураспада некоторых радионуклидов, применяемых в медицине
- •Калорийность продуктов питания
- •Содержание
Смещение химического равновесия
Каждое химическое равновесие устанавливается при определенном значении трех параметров, которые его характеризуют:
1) концентрация реагирующих веществ,
2) температура,
3) давление для газов.
Изменение одного их этих параметров определяет характер внешнего воздействия на систему и приводит к нарушению равновесия (рис. 16). Установившееся новое равновесие оказывается смещенным по отношению к исходному вправо или влево в зависимости от того, равновесные концентрации каких веществ стали больше - продуктов реакции или исходных веществ.
Направление смещения равновесия определяется принципом Ле Шателье:
Е сли
на систему, находящуюся в состоянии
химического равновесия, оказывать
воздействия путем изменения концентрации
реагентов, давления, температуры, то
равновесие смещается в направлении той
реакции, протекание которой ослабляет
это воздействие.
сли
на систему, находящуюся в состоянии
химического равновесия, оказывать
воздействия путем изменения концентрации
реагентов, давления, температуры, то
равновесие смещается в направлении той
реакции, протекание которой ослабляет
это воздействие.
Это означает, что до установления нового равновесия получает большую скорость та реакция, которая уменьшат внешнее воздействие, и таким образом равновесие смещается в сторону образования продуктов этой реакции.
Аналогично принципу Ле Шателье в природе существует принцип адаптивных перестроек:
Л юбая
живая система при воздействии на нее
перестраивается так, чтобы уменьшить
это воздействие.
юбая
живая система при воздействии на нее
перестраивается так, чтобы уменьшить
это воздействие.
А нри-Луи Ле-Шателье родился 8 октября 1850 года в Париже. После окончания Политехнической школы в 1869 году он поступил в Высшую Национальную горную школу. Будущий открыватель знаменитого принципа был широко образованным и эрудированным человеком. Его интересовали и техника, и естественные науки, и общественная жизнь. Много времени он посвятил изучению религии и древних языков. В возрасте 27 лет Ле-Шателье стал уже профессором Высшей горной школы, а тридцать лет спустя - Парижского университета. Тогда же он был избран в действительные члены Парижской Академии наук. Наиболее важный вклад французского ученого в науку был связан с изучением химического равновесия, исследованием смещения равновесия под действием температуры и давления. Студенты Сорбонны, слушавшие лекции Ле-Шателье в 1907-1908 годах, так записывали в своих конспектах: "Изменение любого фактора, могущего влиять на состояние химического равновесия системы веществ, вызывает в ней реакцию, стремящуюся противодействовать производимому изменению. Повышение температуры вызывает реакцию, стремящуюся понизить температуру, то есть идущую с поглощением тепла. Увеличение давления вызывает реакцию, стремящуюся вызвать уменьшение давления, то есть сопровождающуюся уменьшением объема...".
К сожалению, Ле-Шателье не был удостоен Нобелевской премии. Причина заключалась в том, что эта премия присуждалась только авторам работ, выполненных или получивших признание в год получения премии. Важнейшие работы Ле Шателье были выполнены задолго до 1901 года, когда состоялось первое присуждение Нобелевских премий.
Способы смещения равновесия
1. Увеличение давления (для газов) смещает равновесие в сторону реакции, ведущей к уменьшению объема (т.е. к образованию меньшего числа молекул).
|
1 |
|
|
A |
((;(( 2 |
С(г); |
увеличение давления приводит к возрастанию скорости прямой реакции (1 > 2), |
2 моль |
|
1моль |
равновесие смещается вправо.
|
2. Увеличение температуры смещает положение равновесия в сторону эндотермической реакции (т.е. в сторону реакции, протекающей с поглощением теплоты):
|
1 |
|
|
A + В |
((;(( |
С + Q, |
увеличение температуры приводит к |
|
2 |
|
возрастанию скорости обратной (эндотермической) реакции (2 > 1), равновесие смещается влево. |
|
1 |
|
|
A + В |
((;(( |
С – Q, |
увеличение температуры приводит к |
|
2 |
|
возрастанию скорости прямой (эндотермической) реакции (1 > 2), равновесие смещается вправо. |
3. Увеличение концентрации исходных веществ А и В и удаление продуктов из сферы реакции смещает равновесие вправо, так как увеличивается скорость прямой реакции. Уменьшение концентраций исходных веществ A или В приводит к возрастанию скорости обратной реакции (2 > 1), равновесие смещается влево.
4. Катализаторы не влияют на положение равновесия, так как катализатор ускоряет как прямую, так и обратную реакции.
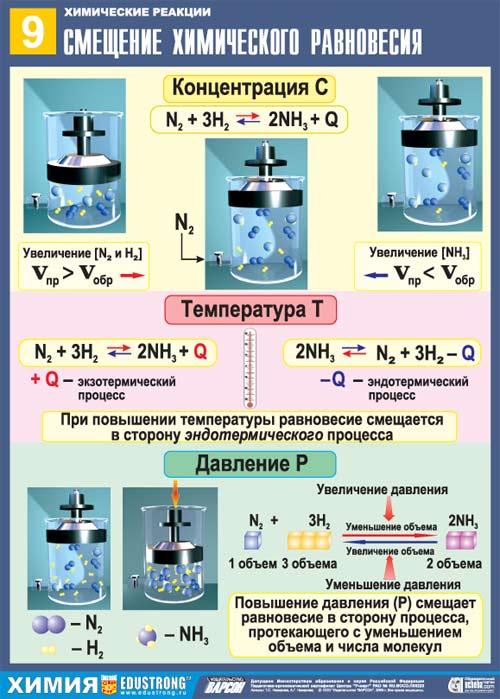
Рис. 16. Влияние концентрации, давления, температуры на равновесие

 (г)
+В(г)
(г)
+В(г)