
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
Нітробензол.
Нітробензол С6Н5NO2. Рідина жовтоватого кольору, з запахом гірького миндалю. Погано розчиняється у воді та добре в багатьох органічних розчинниках. Вихідний продукт у виробництві аніліну, широко використовується у анілінофарбовій, парфумерній, фармацевтичній промисловостях.
За хімічними властивостями нітробензол взаємодіє:
а) з сірнистим амінієм:
С6Н5NO2 + 3(NН4)2S С6Н5NН2 + 6NН3 +3S+ 2Н2O;
б) з залізом у нейтральному середовищі:
4С6Н5NO2 + 9Fe + 4Н2O 4С6Н5NН2 + 3Fe3О4;
в) з оловом у кислому середовищі:
С6Н5NO2 + 3Sn + 7НСІ 4С6Н5NН2НСІ + 3SnСІ2+ 2Н2O;
г) з гідразіном у присутності каталізатору – скелетного нікелю:
2С6Н5NO2
+ 3Н2N
- NН2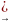 2С6Н5NН2+
3N2+
4Н2O;
2С6Н5NН2+
3N2+
4Н2O;
Азо- і діазосполуки, їх властивості.
У діазосполуках АrN2Х атоми азоту пов’язані з ароматичним радикалом та неорганічним залишком Х (СІ-, Br-,NO2-, НSО4-, BF4-, ОН-).
Азосполуки містять групіровку – N = N– (азогрупа), яка пов’язана з двома радикалами. В залежносты выд характеру радикалу діазо- та азосполуки можуть бути аліфатичного, ароматичного або гетероциклічного ряду. Найбільшу цікавість визиває ароматичний діазо- та азосполуки завдяки різноманітності використання у виробничих синтезах.
Діазосполуки існують у декількох формах:
[Ar – N+ ≡N]Cl- [Ar – N+ ≡N]ОН- Ar – N=N– ОН Ar – N =N– ОМе
солі діазонію гідроксиди діазонію діазогідрати діазотати
У кислому середовищі діазосполуки існують у виді солей діазонію, у лугах – у виді дізотатів, а в середовищі, близькому до нейтрального – у виді ізомерних гідроксидів діазонію та діазогідратів.
Основний спосіб добування солей діазонію – реакція діазотирування: дія нітратної кислоти на сіль первинного ароматичного аміну у кислому середовищі. Азотисту кислоту отримують безпосередньо у процесі діазотирування, дією соляної кислоти на нітріт натрію. Весь процес відбувається при охолодженні, використовуючи надлишок соляної кислоти:
С6Н5NН2 + НСІ С6Н5NН2НСІ
анілін солянокислий анілін
NаNO2 + НСІ НNO2 + NаСІ
С6Н5NН2НСІ + НNO2 [С6Н5N ≡ N]+СІ-+ 2Н2О
фенілдіазонійхлорид
Солі діазонію у сухому стані легко вибухають, тому використовують звичайні їх розчини, які отримали у результаті реакції діазотирування.
Р
 еакція
з виділенням азоту
(обмін діазогрупи на інші групіровки).
Добування
фенолів:
еакція
з виділенням азоту
(обмін діазогрупи на інші групіровки).
Добування
фенолів:
ArN + X- + Н2О Ar – ОН + N2 + НХ
⃦ фенол
N
Заміщення діазогрупи на хлор, бром та СN-групу. Реакція Зайдмейера (каталізатори – відповідні солі одновалентної міді):
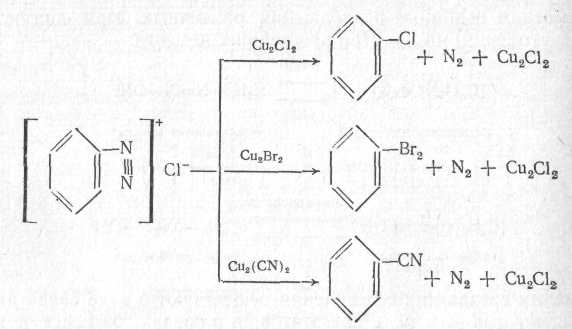
Заміщення
діазогрупи на йод:
[ArN≡N]+Cl-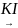 ArІ
+N2+КCl
ArІ
+N2+КCl
Обмін діазогрупи на фтор:
[С6Н5N
≡ N]+СІ-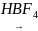 [С6Н5N
≡ N]+BF4-
[С6Н5N
≡ N]+BF4-
фенілдіазонійборфторид
[С6Н5N
≡ N]+BF4-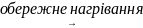 С6Н5F
+ N2
+ ВF3
С6Н5F
+ N2
+ ВF3
Утворення металорганічних сполук (реакція Несмеянова).
[С6Н5N ≡ N]+СІ-+ НgCl2 + 2CuС6Н5Нg – Cl+ N2 + Cu2Cl2
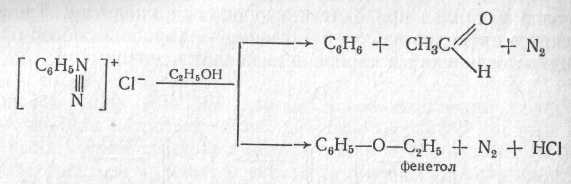
Взаємодія солей діазонію зі спиртами. Реакція йде у двох напрямках: спирт окиснююється у альдегід, сіль діазонію відновлюється до вуглеводню, а діазогрупа обмінюється на алкоксігрупу та утворюється простий ефір фенолу:
Р
 еакції,
які йдуть без виділення азоту.
До таких реакцій відносяться відновлення
діазосполук та азопоє’днання.
Відновлення
солей діазонію.
еакції,
які йдуть без виділення азоту.
До таких реакцій відносяться відновлення
діазосполук та азопоє’днання.
Відновлення
солей діазонію.
С6Н5 – N + СІ- С6Н5 – NН – NН2 + НСІ
⃦ фенілгідразін
N
фенілдіазонийхлорид
Реакція азопоє’днання. Це основний спосіб добування азопоє’днання. Солі арилдіазонієв (слабкі електрофіли) вступають до взаємодії з похідними бензолу, які мають сильні електроно-донорні групіровки, такі, як феноли та аміни. Первинний ароматичний амін, з якого була добута відповідна сіль діазонію, називають діазоскладеним (діазокомпонентом) реакції азопоє’днання. Амін або фенол, який поє’днується з сілью діазонію, називають азоскладаючим реакції азопоє’днання.
Первинні та вторинні ароматичні аміни поє’днуючись з солями діазонію у нейтральних або слабокислих середовищах по атому азоту, утворюючи діазоаміносполуки, які при підкисленні перегрупіруються у аміноазосполуки.
Третинні ароматичні аміни поє’днуючись з солями діазонію у кислому середовищі.
Активність азоскладаючих у реакціях азопоє’днання збільшується зі збільшенням електронної густини бензольного ядра. Азосполуки відіграють велике значення у виробництві барвників, багато яких є їх похідними.
