
- •Часть I
- •Введение
- •1. Внеаудиторная подготовка
- •1.1. Аминокислоты
- •1.1.1. Строение, классификация, номенклатура
- •1.1.2. Биологические функции аминокислот
- •1.1.3. Физико-химические свойства аминокислот
- •Физические свойства l-аминокислот
- •Кислотно-основные свойства протеиногенных аминокислот
- •1.1.4. Химические свойства аминокислот
- •1.1.4.1. Реакции с участием карбоксильной группы
- •1.1.4.2. Реакции с участием аминогруппы
- •1.1.4.3. Реакции с одновременным участием карбоксильной и аминогрупп
- •1.1.4.4. Специфические реакции аминокислот
- •Специфические реакции, используемые для идентификации и количественного анализа α-аминокислот и белков
- •1.2. Полипептиды
- •1.2.1. Природа пептидной связи
- •1.2.2. Классификация полипептидов, отдельные представили и их биологическая роль
- •1.2.2.1. Малые линейные пептиды
- •Пептидные гормоны
- •1.2.2.2. Циклопептиды
- •1.2.2.3. Белки
- •1.2.2.3.1. Уровни структурной организации белков
- •1.2.2.3.2. Классификация белков
- •1.2.2.3.3. Физико-химические свойства белков
- •1.2.2.3.4. Выделение белков
- •Контрольные вопросы, задачи и упражнения
- •2. Лабораторный практикум
- •2.1. Идентификация аминокислот и белков
- •2.1.1. Общие качественные реакции аминокислот
- •2.1.2. Специфические качественные реакции аминокислот
- •2.1.3. Хроматографические методы разделения и идентификации аминокислот и белков
- •Rf для аминокислот при разделении методом хроматографии на бумаге
- •Практическая контрольная работа по идентификации аминокислот и белков химическими и хроматографическими методами
- •2.2. Количественный анализ аминокислот и белков
- •2.2.1. Титриметрические методы анализа аминокислот
- •2.2.2. Спектральные методы количественного определения белка
- •Множители ƒ для вычисления концентрации белка
- •Практическая контрольная работа по количественному анализу аминокислот и белков
- •Библиографический список
- •Оглавление
- •Часть I 0
- •Аминокислоты и полипептиды
- •443100. Г. Самара, ул. Молодогвардейская, 244. Главный корпус
- •443100. Г. Самара, ул. Молодогвардейская, 244. Корпус №8
Специфические реакции, используемые для идентификации и количественного анализа α-аминокислот и белков
Реактивы |
Определяемые аминокислоты |
Наблюдаемое проявление |
Ксантопротеиновая реакция Концентрированная азотная кислота |
Тирозин Фенилаланин Триптофан |
Желтая окраска |
Реакция Миллона Нитрат ртути (I) + азотная кислота |
Тирозин |
Красный осадок |
Реакция Гопкинса – Кола Глиоксиловая + концентрированная серная кислоты |
Триптофан |
Сине-фиолетовая окраска |
Реакция Эрлиха n-Диметиламинобензальдегид + концентрированная хлористоводородная кислота |
Триптофан |
Пурпурно-синяя окраска |
Реакция Сакагучи α-Нафтол + гипобромит натрия |
Аргинин |
Красная окраска |
Нитропруссидная реакция Нитропруссид натрия + разбавленный водный аммиак |
Цистеин |
Красно-фиолетовая окраска |
Реакция Фоля Ацетат свинца + едкий натр |
Цистеин Метионин |
Черный осадок |
Фармакопейная реакция 1. Резорцин + концентрированная серная кислота 2. Раствор аммиака |
Глутаминовая кислота Глутамин |
Красно-фиолетовая окраска |
Реакция Паули Диазореактив из сульфаниловой кислоты + + едкий натр |
Гистидин Тирозин |
Красная окраска |
Реакция Фолина-Чиокалтеу Фосфомолибдовольфрамовая кислота |
Тирозин |
Синяя |
Как видно из сущности ксантопротеиновой реакции, определению тирозина, триптофана и фенилаланина мешают ароматические соединения, и прежде всего фенолы и ароматические амины.
Реакция Миллона. Этот метод определения тирозина основан на том, что, во-первых, тирозин в отличие от триптофана и фенилаланина нитруется даже разбавленной азотной кислотой, а во-вторых, образующийся нитротирозин дает красную, нерастворимую в кислой среде аци-нитросоль с ионом [Hg2]2+:
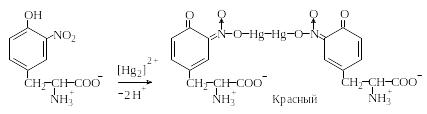
При низкой концентрации тирозина возникает красное окрашивание, при высокой – выпадает красный осадок.
Эта реакция положительна также для фенольных соединений.
Нитропруссид натрия – Na2[Fe(CN)5NO] дает с меркаптанами в щелочной среде характерную красную или красно-фиолетовую окраску вследствие образования комплексных соединений следующего типа:
N![]() a2[Fe(CN)5NO
+ 2 HS-R + 2 NH3
Na2(NH4)2[Fe(CN)5NO(S-R)2]
a2[Fe(CN)5NO
+ 2 HS-R + 2 NH3
Na2(NH4)2[Fe(CN)5NO(S-R)2]
Цистеин дает положительную реакцию в разбавленном растворе аммиака, а цистин и метионин – отрицательную. Аммиак, а не щелочь, как обычно, используется потому, чтобы исключить возможность образования меркаптанов из цистина и метионина, меркаптаны дают положительную реакцию с нитропруссидом натрия.
Реакция Фоля. Метод Фоля позволяет определять наличие серы в меркаптанах и сульфидах. Метод заключается в кипячении раствора препарата с щелочным раствором плюмбита натрия; при этом образуется черный осадок сульфида свинца. Положительную реакцию Фоля дают не только цистеин, цистин и метионин, но и пептиды и белки, содержащие эти аминокислоты:
![]()
Определению серосодержащих аминокислот мешают соединения, содержащие в своей молекуле сульфидную или меркаптановую функциональные группы, например антибиотик пенициллин.
Реакция Сакагучи. Аргинин легко конденсируется с α-дикетонами с образованием имидазольного цикла, что используется в пептидном синтезе для защиты гуанидиновой группы аргинина. В реакции Сакагучи происходит аналогичная конденсация с 1,2-нафтохиноном, который образуется при окислении α-нафтола гипобромитом или гипохлоритом натрия.
Реакция Сакагучи является общей для любых производных гуанидина. Так, например, антибиотик стрептомицин также дает положительную реакцию Сакагучи, поскольку содержит в своей молекуле гуанидиновый остаток ((H2N)HN=C-NH-):
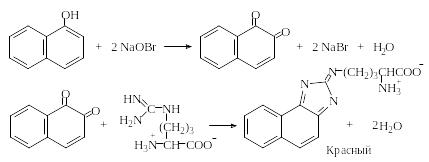
Открытие глутаминовой кислоты и глутамина. При нагревании глутаминовой кислоты или глутамина они циклизуются с отщеплением воды и образованием пирролидонкарбоновой кислоты (пироглутаминовая кислота) или ее амида соответственно:
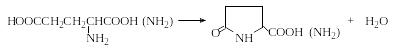
Пироглутаминовая кислота при нагревании с резорцином в присутствии концентрированной серной кислоты образует краситель, приобретающий в щелочной среде красно-фиолетовый цвет:
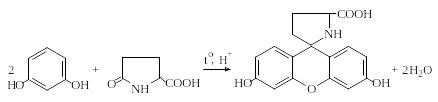
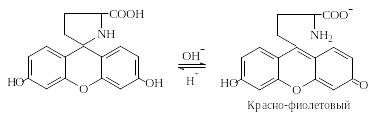
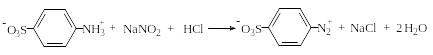
Реакция Паули. Эта реакция основана на азосочетании активированных ароматических соединений с солями диазония, в результате которой образуются азокрасители. Соль диазония готовят из сульфаниловой кислоты:
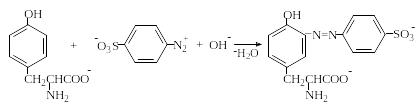
Реакция Фолина-Чиокалтеу. Среди протеиногенных аминокислот тирозин является самым сильным восстановителем. На использовании этого свойства и основана реакция Фолина-Чиокалтеу. Из всех протеиногенных аминокислот реактив Фолина-Чиокалтеу, представляющий собой фосфомолибдовольфрамовую кислоту, окисляет лишь тирозин по схеме
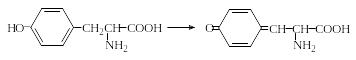
При этом фосфомолибдовольфрамовая кислота восстанавливается до фосфомолибдовольфрамовой гетерополисини – вещества непостоянного состава синего цвета.
