
Лабораторна робота
Тема. Полуменево-фотометричне визначення натрію в розчинах.
Мета роботи. Ознайомитися із принципами фотометрії полум'я, використання методу для якісної ідентифікації елементів і кількісного аналізу. Визначити вміст натрію у водній витяжці ґрунту Донецької області, питній воді.
Прилади й реактиви. Полуменевий фотометр; терези лабораторні й аналітичні; натрій хлорид кваліфікації х.ч.; посуд мірний лабораторний; піпетки й бюретки; вода дистильована за ДЕСТ.
Принцип методу
Метод фотометрії полум'я є різновидом атомно-емісійного спектрального аналізу й заснований на вимірюванні довжини хвилі й інтенсивності світла, що випромінюється атомами в газоподібному стані. Випромінення світла атомами відбувається за рахунок зміни енергії атомів. Атоми можуть мати строго певні дискретні запаси внутрішньої енергії Ео, Е1, Е2 і т.д. У незбудженому, тобто в нормальному стані атоми мають мінімальну енергію Ео. При отриманні енергії атоми збуджуються, тобто переходять на більш високий енергетичний рівень Е1, Е2 і т.д. Через дуже короткий час (~ 10-8 с) атом мимовільно вертається в нормальний стан або якийсь більш низький збуджений стан. Вивільнювана при цьому енергія ΔЕ випромінюється у вигляді світлового кванта hν:
ΔЕ= hν
Інтенсивність аналітичного сигналу (спектральної лінії) визначається вираженням
Ii0 = Ni·Ai0·h·νi0
де Ni – число атомів у збудженому стані i;
Ai0 – імовірність переходу зі збудженого стану i у більш низький стан 0;
νi0 – частота, відповідна до цього переходу;
h – постійна Планка.
Підставляючи в попереднє вираження розподілу атомів по ступенях збудження для термічно рівноважної плазми, одержуємо:
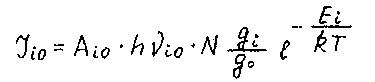
де N – число атомів у плазмі;
Ei – енергія збудження iгго рівня;
qi і q0 – статистичні терези збудженого й нормального стану;
Т – температура.
При сталості температури й інших умов збудження одержимо
Ii0 = α·N
Якщо режим роботи джерела збудження досить стабільний і швидкість подачі речовини в плазму постійна, наступає деякий стаціонарний стан, у якому число атомів елемента в плазмі виявляється пропорційним концентрації цього елемента в пробі:
N = α'’·C
де С – концентрація речовини в пробі;
α,, – коефіцієнт пропорційності.
Остаточно одержуємо:
Ii0 = a·C
З урахуванням самопоглинання одержуємо формулу Ломакина, яка добре описує концентраційну залежність інтенсивності спектральної лінії:
I = a·Cb
де а – коефіцієнт, що залежить від джерела збудження, його стабільності, температури і т.д.;
b – коефіцієнт самопоглинання, що враховує поглинання квантів світла незбудженими атомами.
Полум'я може використовуватися як джерело збудження емісійних спектрів елементів. У роботі використовується полуменевий фотометр або атомно-абсорбційний спектрометр у режимі «ЕМІСІЯ».
У цьому режимі відключена або виведена з робочого положення лампа з порожнистим катодом або безелектродна лампа. Напівпрозоре дзеркало для збільшення кількості світла повинне бути виведене з робочого положення (ручка «ПОЛУПРОЗ. ДЗЕРКАЛО ВІДКЛ.»). Проба подається в пальник, де відбувається процес збудження атомів елемента, який визначають, що супроводжується випромінюванням з характерної для даного елемента довжиною хвилі ( аналітичною лінією). Під дією випромінювання полум'я у вимірювальному обладнанні виникає сигнал, що залежить від концентрації елемента, який визначають.
Натрій визначають по лініях жовтого дублету 589,0 – 589,6 нм. При роботі із приладами малої роздільної сили визначенню натрію може заважати літій, а також кальцій і стронцій. Присутність у розчинах великих кількостей алюмінію знижує інтенсивність випромінювання натрію.
