
- •14. Реакции конденсации
- •14.1. Реакции конденсации, не приводящие к образованию новых циклов
- •Реакции электрофильного замещения
- •14.1.1.1. Алкилирование ароматических соединений
- •14.1.1.2. Конденсация ароматических соединений с альдегидами и кетонами.
- •14.1.1.3. Реакции хлор- и бромметилирования
- •14.1.1.4. Реакция аминометилирования
- •14.1.1.5. Формилирование ароматических соединений
14. Реакции конденсации
Реакции конденсации представляют собой наиболее обширную группу процессов в технологии органического синтеза. Эти реакции обязательно сопровождаются усложнением структуры исходных соединений: образованием новых связей, увеличением числа атомов углерода, образованием циклических систем. В соответствии с общепринятой терминологией реакциями конденсации называются химические реакции, приводящие к образованию новой углерод-углеродной связи или циклической системы. Однако, очень часто к процессам конденсации относят также реакции, приводящие к образованию новой связи между атомом углерода и гетероатомом, обычно атомом азота.
Реакции конденсации можно разделить на две большие группы:
реакции, не приводящие к образованию новых циклов
реакции с образованием новых циклов.
14.1. Реакции конденсации, не приводящие к образованию новых циклов
В результате реакций конденсации, не приводящих к образованию новых циклов, происходит усложнение исходной молекулы субстрата в результате образования новой связи углерод-углерод. Эти процессы также можно разделить на несколько групп, которые будут рассмотрены ниже.
Реакции электрофильного замещения
Реакции конденсации ароматических углеводородов, протекающих по механизму электрофильного замещения, представляют собой важнейшую группу процессов, позволяющих получать замещенные ароматические соединения.
14.1.1.1. Алкилирование ароматических соединений
Для алкилирования ароматических соединений могут быть использованы алкилгалогениды, олефины (алкены) и спирты.
Алкилирование по Фриделю-Крафтсу
А![]() лкилирование
по Фриделю-Крафтсу представляет собой
взаимодействие ароматического
углеводорода с алкилгалогенидом в
присутствии хлористого алюминия.
Стехиометрическое уравнение этой
реакции выглядит следующим образом:
лкилирование
по Фриделю-Крафтсу представляет собой
взаимодействие ароматического
углеводорода с алкилгалогенидом в
присутствии хлористого алюминия.
Стехиометрическое уравнение этой
реакции выглядит следующим образом:
Механизм данного процесса предполагает первоначальное образование комплекса алкилгалогенида с хлористым алюминием:
![]()
Склонность алкилгалогенидов к комплексообразованию в силу стерических причин изменяется в ряду:
RF > RCl > RBr > RJ
Поэтому на практике используют алкилхлориды и алкилбромиды. Алкилгалогенид и алкилируемое соединение используют в эквимолекулярных количествах, а количество хлористого алюминия составляет 10-20% от количества субстрата.
Алкилирование по Фриделю-Крафтсу сопровождается рядом побочных процессов, включающих изомеризацию промежуточного карбокатиона, -комплекса и конечного продукта. Как указывалось выше, при взаимодействии алкилгалогенидов с хлористым алюминием в качестве первой промежуточной частицы образуется карбокатион R+. Известно, что устойчивость карбокатионов изменяется в ряду третичный > вторичный > первичный. Поэтому при использовании первичных алкилгалогенидов возможна перегруппировка первичного карбокатиона во вторичный или третичный. В связи с этим реакция протекает однозначно только в случае метил- и этилгалогенидов. При использовании же н-пропилхлорида или н-пропилбромида и высших н-алкилгалогенидов основным продуктом реакции является соответствующий изоалкилбензол:
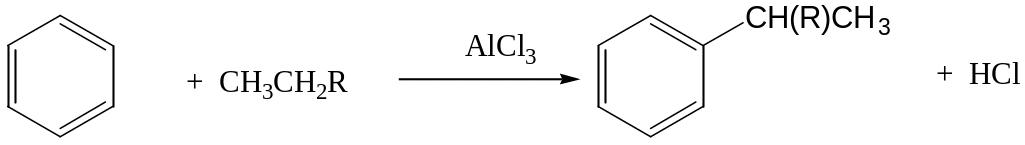
Вторым процессом, приводящим к изомерным продуктам, является изомеризация промежуточного -комплекса. Так, при метилировании толуола метилхлоридом наряду с орто- и пара-ксилолом образуется и значительное количество мета-ксилола. Образование мета-ксилола наблюдается также при нагревании п-ксилола с хлористым алюминием.
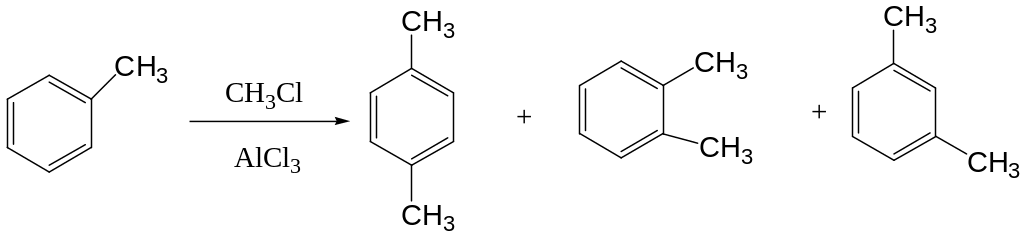
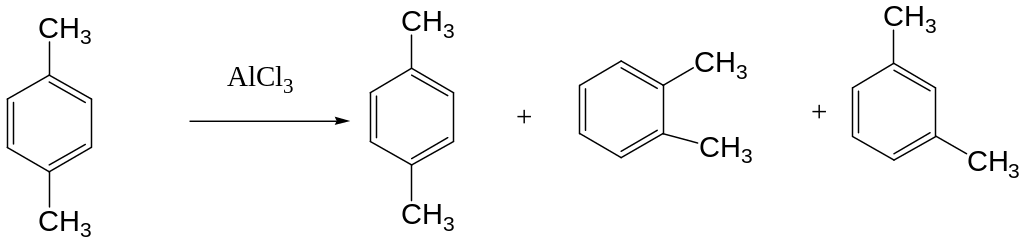
Практически алкилирование по Фриделю-Крафтсу проводят с использованием в качестве растворителя избытка алкилируемого соединения в том случае, если последнее представляет собой жидкость. Возможно также применение таких растворителей как нитробензол, сероуглерод и другие, индифферентные к хлористому алюминию. Реакция является экзотермической, и в начальный момент необходимо строго поддерживать требуемую температуру, чтобы избежать осмоления реакционной массы. В конце процесса обычно требуется нагревания. По окончании реакции реакционную массу охлаждают, хлористый алюминий разлагают путем добавления воды, превращая его в основные соли.
Алкилирование олефинами
Алкилирование бензола -алкенами (-олефинами) имеет важное значение с точки зрения получения этилбензола, изопропилбензола и длинноцепочечных вторичных алкилбензолов, используемых в производстве алкилбензолсульфонатов. В качестве катализатора используют хлористый алюминий и хлороводород, образующийся из хлористого алюминия при добавлении небольшого количества (~2%) воды. Процесс проводят непрерывным способом либо в каскаде емкостных аппаратов, либо в колонных аппаратах.

этилбензол
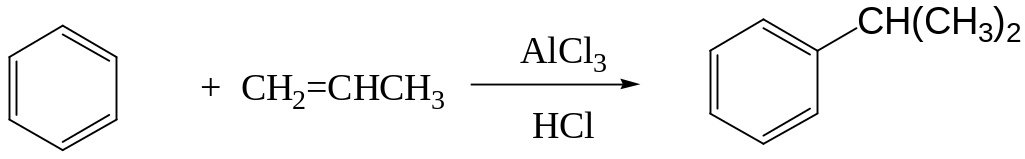
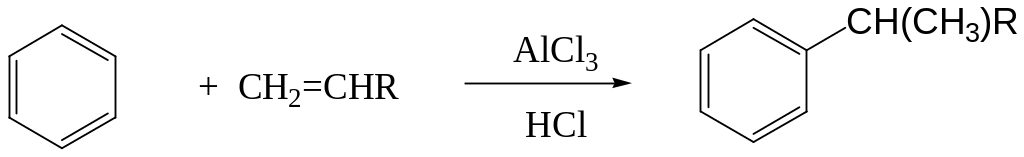 изопропилбензол
(кумол)
изопропилбензол
(кумол)
Этилбензол используется для получения стирола:
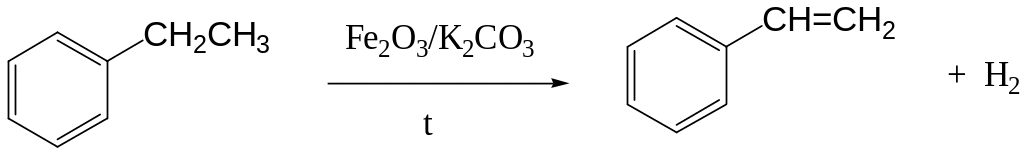
Изопропилбензол используют в производстве фенола и -метилстирола.
Другим важным процессом алкилирования с использованием олефинов является С-алкилирование фенолов. Процесс ведут при 80-120оС в присутствии кислых катализаторов (H2SO4, катионообменная смола КУ-2). Практический интерес представляет получение соединений, содержащих третичный атом углерода, связанный с бензольным ядром.
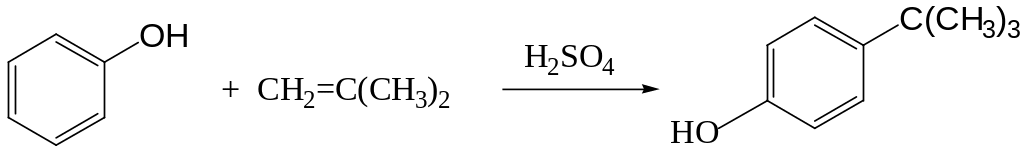
изобутилен 4-трет-бутилфенол
4-трет-Бутилфенол используется в лакокрасочной промышленности.

I
Соединение (I) в результате оксиэтилирования превращается в соединения (II, n = 4-20), представляющие собой неионогенные ПАВ (препараты ОП)
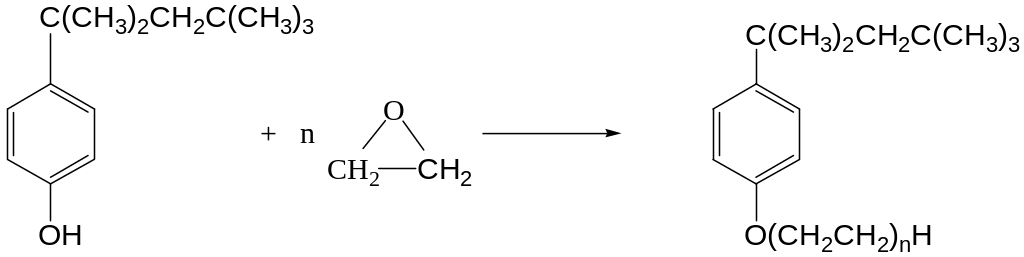
II
При алкилировании фенола изобутиленом в присутствии Al(OC6H5)3 получают важный антиоксидант – 2,6-ди(трет-бутил)фенол:
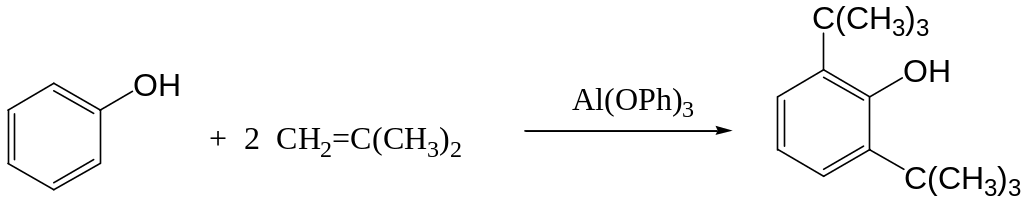
Алкилирование спиртами
В качестве алкилирующих агентов могут использоваться и спирты. Катализаторами в данных реакциях являются соединения кислотного характера: H2SO4, H3PO4, ZnCl2, Al2O3. В зависимости от природы субстрата и спирта, процесс можно вести либо в жидкой, либо в паровой фазе.
![]()
К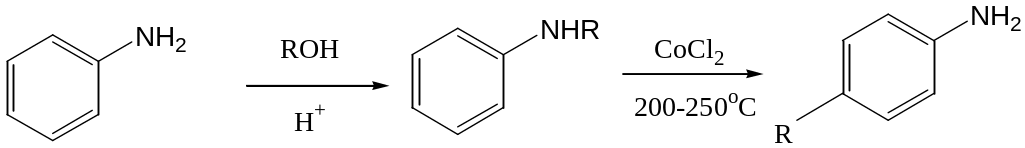 онденсация
со спиртами представляет собой интерес
при алкилировании ароматических аминов.
В случае первичных ароматических аминов
первоначально образуются N-алкилзамещенные
соединения, которые при нагревании при
температуре 200-250оС в присутствии
хлоридов кобальта или цинка
перегруппировываются в соответствующие
пара-алкиланилины.
онденсация
со спиртами представляет собой интерес
при алкилировании ароматических аминов.
В случае первичных ароматических аминов
первоначально образуются N-алкилзамещенные
соединения, которые при нагревании при
температуре 200-250оС в присутствии
хлоридов кобальта или цинка
перегруппировываются в соответствующие
пара-алкиланилины.
Реакция оксиэтилирования
Р еакция
оксиэтилирования представляет собой
взаимодействие ароматического соединения
с окисью этилена в присутствии кислотного
катализатора (минеральная кислота,
Al2O3,
AlCl3). На примере
бензола этот процесс выглядит следующим
образом:
еакция
оксиэтилирования представляет собой
взаимодействие ароматического соединения
с окисью этилена в присутствии кислотного
катализатора (минеральная кислота,
Al2O3,
AlCl3). На примере
бензола этот процесс выглядит следующим
образом:
Целевым продуктом в данном случае является β-фенилэтиловый спирт, который получают также гидрированием окиси стпирола.
β-Фенилэтиловый спирт, т.пл. – 27оС, т.кип. 220-222оС, d204 = 1.021-1.025. Применяется в пищевой и парфюмерной промышленности в качестве душистого вещества (запах розы); является исходным сырьем для получения ряда других душистых веществ.
