- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
4.3.4. Правила ориентации в бензольном кольце
Введение нового заместителя в бензольное кольцо, уже содержащее заместители, происходит в определенные положения.
Реакционная способность того или иного атома углерода в бензольном кольце определяется следующими факторами:
1) положением и природой уже имеющихся заместителей,
2) природой действующего реагента,
3) условиями проведения реакции.
Решающее влияние имеют два первых фактора.
Заместители в бензольном кольце можно разделить на две группы. Заместители первого рода – это группировки атомов, способные отдавать электроны (электронодонорные). К ним относятся:
-OH, -OR, -OCOR, -SH, -SR, NH2, -NHR, -NR2, -NHCOR, -N=N-, -CH3, -CH2R, -CR3, -F, -Cl, -Br, -J.
Заместители второго рода – это атомные группировки, способные оттягивать электроны от бензольного ядра (электроноакцепторные). К ним относятся:
-SO3H, -COR, -COOH, -COOR, -CN, -CCl3, -NH3+, -NR3+ и т.д.
Действующие на бензол реагенты также можно разделить на две группы: электрофильные и нуклеофильные. Наиболее характерны для ароматических соединений процессы галогенирования, сульфирования и нитрования. Эти процессы идут при взаимодействии бензольного кольца с электрофильными реагентами.
Известны и реакции с нуклеофильными реагентами (NaOH, NaNH2). Сюда относятся, например, реакции гидроксилирования, аминирования.
Заместители первого рода облегчают реакции с электрофильными реагентами (кроме галогенов), причем они ориентируют новый заместитель в орто- и пара- положения.
Заместители второго рода затрудняют реакции с электрофильными реагентами, причем они ориентируют новый заместитель в мета-положение. В то же время эти заместители облегчают реакции с нуклеофильными реагентами направляя в орто- и пара положения.
Примеры.
1. Заместитель 1 рода, реагент электрофильный. Облегчающее действие заместителя, о-, п-ориентация:
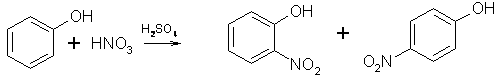
2. Заместитель II рода, реагент электрофильный. Затрудняющее действие заместителя; мета-ориентация:

3. Заместитель I рода, реагент нуклеофильный; мета-ориентация. Затрудняющее действие заместителя. Примеры таких реакций с бесспорным механизмом неизвестны.
4. Заместитель II рода, реагент нуклеофильный, о-, п — ориентация:
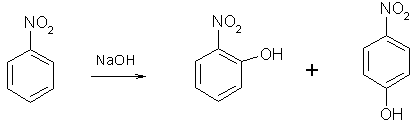
Главнейшие заместители по силе ориентирующего действия в реакциях электрофильного замещения можно расположить в следующий ряд:
OH > NH2 > Cl > J > Br > CH3
COOH > SO3H > NO2
Описанное правило не носит характера закона. Речь почти всегда идет только о главном направлении реакции.
4.2.5. Механизм ориентирующего влияния заместителей
В молекуле бензола электронная плотность распределена совершенно равномерно. Присутствие заместителя нарушает эту равномерность. Появляется чередующаяся полярность углеродных атомов, неугасающая по всему кольцу.
Заместитель может влиять на бензольное ядро двумя способами, т.е. могут иметь место два эффекта:
1) индукционный;
2) сопряжения.
В случае проявления индукционного эффекта изменение электронной плотности в ядре связано с поляризацией σ-связи между заместителем и ядром:

–J +J
Второй эффект связан с возникновением сопряжения между р-элек-тронами заместителя и кольца. При этом электроны могут смещаться в сторону кольца или в сторону заместителя:
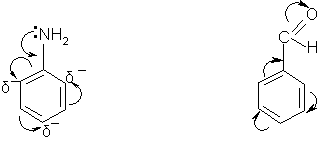
( +Е ) ( –Е )
положительный отрицательный
мезомерный мезомерный
эффект эффект
анилин бензойный альдегид
В случае анилина увеличивается реакционная способность бензольного кольца по отношению к электрофильным реагентам, в случае бензойного альдегида по отношению к нуклеофильным реагентам.
Оба эффекта индукционный и сопряжения могут проявляется одновременно в одной молекуле, усиливая или ослабляя друг друга.

Таким образом, в случае заместителей первого рода наиболее сильно изменяют свой заряд орто- и пара- углеродные атомы: они обогащаются электронной плотностью и становятся весьма реакционноспособными по отношению к электрофильным реагентам.
Заместители второго рода вызывают обеднение кольца электронной плотностью. Поэтому реакции электрофильного замещения идут в этом случае значительно труднее. Наиболее обедняются электронной плотностью орто- и пара-положения. Поэтому по отношению к электрофильным реагентам эти положения становятся наименее реакционноспособными.
При наличии в бензольном ядре двух заместителей ориентирующее влияние обоих заместителей может быть согласованным и несогласованным. При согласованной ориентации новый продукт получается с наилучшим выходом.
Задачи для самопроверки
1.
Бензол получают из гексана при нагревании
в присутствии катализатора. Какой объем
бензола (ρ![]() =0,86
г/см3)
можно получить из 16 г гексана, если его
выход составляет 60 % от теоретического.
=0,86
г/см3)
можно получить из 16 г гексана, если его
выход составляет 60 % от теоретического.
2. Какова масса бензола (г), который может быть получен из 22 дм3 ацетилена (н. у.) с 80 % выходом.
3. Рассчитайте массу хлорбензола, который может быть получен при пропускании 30 дм3 хлора (н. у.) в избыток бензола в присутствии хлорида железа (+3), если выход хлорбензола составляет 50%.
4. В круглодонной колбе, снабженной шариковым холодильником, прокипятили на песчаной бане в течение 4 часов смесь, состоящую из 10 мл толуола (ρ = 0,86 г/см3), воды и перманганата калия. После завершения реакции окисления и удаления диоксида марганца фильтрат был упарен и подкислен соляной кислотой. Выделившаяся бензойная кислота промыта небольшим количеством холодной воды и высушена. Получено 8 г целевого продукта. Определить выход бензойной кислоты в % от теоретического.
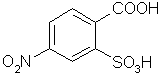
5. В какой последовательности и при каких условиях необходимо обработать бензол для получения с наилучшим выходом (условия согласованной ориентации) следующего соединения:
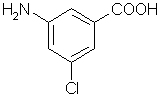
6. Назовите соединение по международной номенклатуре: