
- •1. Фазы в сталях. Общие понятия. Типы фаз. Возможные фазы в нелегированных и легированных сталях.
- •2. Диаграммы фазовых равновесий. Типы для разных сплавов. Расчет количества фазовых и структурных составляющих.
- •3. Фазовые и структурные превращения. Понятия. Возможные механизмы. Термодинамика и кинетика.
- •4. Полиморфизм железа и стали.
- •5. Диаграмма железо - цементит.
- •6.Фазовые и структурные превращения при нагреве стали. Образование аустенита. Структурная наследственность.
- •7. Превращения при охлаждении стали. Изотермические и термокинетические диаграммы распада переохлажденного аустенита.
- •Термокинетические диаграммы превращения переохлажденного аустенита: а) эвтектоидная сталь; б) доэвтектоидная легированная сталь
- •8. Перлитное превращение, структура и свойства перлита.
- •9. Мартенситное превращение в стали. Структура. Свойства стали с мартенситной структурой.
- •10. Бейнитное превращение, влияние легирующих элементов, структура и свойства бейнита.
- •11. Виды отжига. Назначение, режимы. 12. Отжиг сталей. Дефекты отжига.
- •13. Нормализация сталей. Назначение. Режимы.
- •14. Закалка без полиморфного превращения. Назначение. Режимы. 15. Закалка на мартенсит. Структура стали после закалки.
- •16. Старение и отпуск закаленных сталей.
- •17. Механические свойства. Методы испытаний. Уровень свойств.
- •19. Методы повышения конструкционной прочности.
- •20. Химико-термическая обработка
1. Фазы в сталях. Общие понятия. Типы фаз. Возможные фазы в нелегированных и легированных сталях.
Фазой называется однородная часть системы, отделенная от других частей системы (фаз) поверхностью раздела, при переходе через которую химический состав или структура вещества изменяется скачком. Фазой называется объем металла или сплава отделенная от остального сплава границей и характеризующая определенными однородными свойствами. Твердые растворы. Твердыми растворами называют фазы, в которых один из компонентов сплава сохраняет свою кристаллическую решетку, а атомы другого или других компонентов располагаются в решетке первого компонента (растворителя), изменяя ее размеры (периоды). Различают твердые растворы замещения и твердые растворы внедрения. При образовании твердого раствора замещения атомы растворенного компонента замещают часть атомов растворителя в узлах его кристаллической решетки. При образовании твердого раствора внедрения атомы растворенного компонента располагаются в междоузлиях (пустотах) кристаллической решетки растворителя. Переходные металлы образуют с элементами, имеющими малый атомный радиус, соединения. Они имеют общность строения и свойств и называются фазами внедрения. Фазы Лавеса – фазы с определенной концентрацией элементов в сплаве. Интермиталиды – соединения различных металлов, являются промежуточными фазами.
Однородная жидкость является однофазной системой, а механическая смесь двух видов кристаллов – двухфазной. В такой системе каждый кристалл отличается от другого по составу или по строению и они отделены один от другого поверхностью раздела. Компонентами называются вещества, образующие систему. Следовательно, чистый металл представляет собой однокомпонентную систему, сплав двух металлов - двухкомпонентную. Типы фаз:
- металл;
- твердый раствор;
- химическое соединение.
В сталях выделяют фазы:
- α-железо;
- γ-железо;
- карбид железа Fe3C;
- карбиды легирующих элементов. В нелегированных сталях: Доэфтектоидные, эфтектоидные стали, заэфтектоидные стали: α + Fe3C. Техническое железо: α, α + Fe3C.
2. Диаграммы фазовых равновесий. Типы для разных сплавов. Расчет количества фазовых и структурных составляющих.
Д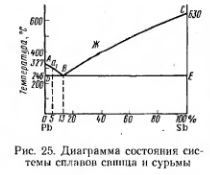 иаграмма
состояния сплавов, образующих механические
смеси из чистых компонентов.
иаграмма
состояния сплавов, образующих механические
смеси из чистых компонентов.
Диаграмма состояния сплавов Pb-Sb представляет собой систему, в которой компоненты нерастворимы в твердом состоянии, а образуют механическую смесь двух видов кристаллитов, одновременно кристаллизующихся из жидкости. На оси ординат отложена температура, а на оси абсцисс - концентрация. С левой стороны диаграммы откладывается 100% компонента Pb, а с правой стороны - 100% компонента Sb. Окончание затвердеваиия характеризуется температурой 2460С для всей данной системы сплавов и что сплав, содержащий 13% Sb и 87% Рb, имеет одну критическую точку В, в которой он полностью затвердевает. Линия СВА, соединяющая точки начала затвердевания сплавов, называется линией ликвидуса, а линия DBE, ниже которой все сплавы находятся в твердом состоянии, называется линией солидуса. В точке В при содержании 13% Sb и 87% Рb происходит одновременно кристаллизация Рb и Sb с образованием механической смеси этих кристаллов - эвтектическим. Сплавы, содержащие менее 13% Sb, называются доэвтектическими, а содержащие более 13% - заэвтектическими. Сплав, содержащий 5% Sb, до линии Аа1 находится в жидком состоянии, а ниже этой линии из жидкого расплава кристализуется компонент Рb. По мере охлаждения количество жидкого расплава уменьшается, а твердого свинца увеличивается. При дальнейшем охлаждении концентрация сурьмы в жидком расплаве становится равной 13% и жидкий расплав кристаллизуется, образуя механическую смесь (эвтектику), состоящую из Рb и Sb. Так как до кристаллизации эвтектики выделялись кристаллы свинца, структура данного сплава после окончательного затвердевания будет: свинец+эвтектика (свинец+сурьма).Сплав, содержащий 40% Sb – заэфтектический сплав, выше линии ВС находится в жидком состоянии. При охлаждении ниже линии ВС из жидкого раствора выпадает Sb и при 2460С происходит кристаллизация всего оставшегося жидкого расплава эвтектического состава. Так как до кристаллизации эвтектики выделялись кристаллы сурьмы, структура после окончательного затвердевания будет: сурьма + эвтектика (свинец+сурьма).
Д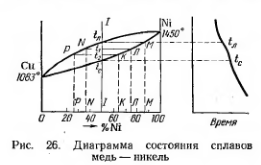 иаграмма
состояния сплавов с неограниченной
растворимостью компонентов.
иаграмма
состояния сплавов с неограниченной
растворимостью компонентов.
На диаграмме верхняя линия - это линия ликвидуса, а нижняя - линия солидуса. Сплава 1-1 состава 50% Cu+50% Ni. При температуре tл начинается кристаллизация. На диаграмме состояния состав твердой части сплава (состав кристаллов, которые могут находиться в равновесии с жидкостью) при данной температуре показывает линия солидуса. Следовательно, первые образовавшиеся кристаллы будут иметь состав точки М. Этот процесс происходит за счет диффузии атомов меди в уже имеющиеся кристаллы. При достаточной выдержке или медленном охлаждении при t1 установится равновесие кристаллов состава точки Л и жидкого сплава. Но в кристаллах состава точки Л никеля больше, чем в сплаве, следовательно, жидкая часть сплава должна быть беднее никелем. При этой температуре состав жидкой части сплава определяется линией ликвидуса, т. е. точкой N. При дальнейшем охлаждении, когда сплав достигнет температуры t2 и установится равновесие, сплав будет состоять из кристаллов состава точки К и жидкой части сплава состава точки Р. Чем ниже температура, тем больше кристаллов твердого раствора и они по составу ближе к исходному. Наконец, при достижении температуры tc сплав полностью затвердеет и будет состоять из однородных кристаллов твердого раствора.
 Диаграмма состояния сплавов с
ограниченной растворимостью компонентов.
Характерной особенностью таких диаграмм
является наличие при температурах ниже
линии солидуса линии ограниченной
растворимости.
Диаграмма состояния сплавов с
ограниченной растворимостью компонентов.
Характерной особенностью таких диаграмм
является наличие при температурах ниже
линии солидуса линии ограниченной
растворимости.
Линия KCD - линия ликвидуса; линия KECF - линия солидуса. Линия SE показывает изменение растворимости компонента В в компоненте А в твердом состоянии. До температуры точки 1 сплав 1-1 жидкий. При температуре точки 1 начинается кристаллизация и образуются кристаллы твердого раствора В в А. Образование кристаллов происходит до температуры точки 2. В точке 2 сплав имеет структуру кристаллов α. При температуре точки 3 линия сплава пересекает линию SE и при этой температуре из кристаллов твердого раствора а начинают выделяться кристаллы компонента В, называемые вторичными (ВII). С понижением температуры от точки 3 до точки 4 растворимость компонента В в компоненте А становится все меньше и меньше и из твердого раствора α выделяется все большее количество кристаллов компонента В. Таким образом, после полного охлаждения сплав будет иметь структуру твердого раствора α и вторичных кристаллов компонента В (ВII).
В сплавах, лежащих по составу правее точки Е, т. е. на линии ECF, образуется эвтектика, но она представляет смесь не кристаллов А и В, а кристаллов твердого раствора а и кристаллов компонента В.
Диаграмма состояния с перетектическим превращением
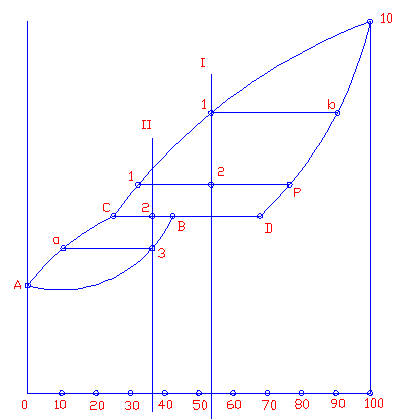
Жидкость реагирует с ранее выпавшими кристаллами и образует новый вид кристаллов L + β → α. Такая реакция называется перитектической. На диаграмме показаны три однофазные области: жидкость L и ограниченные твердые растворы α и β. Линия ABC является линией ликвидус, линия APDB - линией солидус. Кристаллизация сплава I. Кристаллизация начинается в точке 1, когда из жидкости выпадают кристаллы β-раствора состава точки b. Затем по мере снижения температуры жидкость меняет свою концентрацию по линии ликвидус от точки 1 до точки С, а кристаллы β по линии солидус от точки b до точки D. По достижении перитектической горизонтали CPD состав жидкости будет отвечать точке С, а состав кристаллов точке D. В результате образуется фаза α. Перитектическая реакция тогда имеет вид: LС + βD → αP. Точки D и Р показывают предельную концентрацию твердых растворов β и α. В данном сплаве имеется избыток β-фазы по сравнению с тем количеством, которое необходимо для образования α-кристаллов. Поэтому по окончании реакции в избытке остаются β-кристаллы. Следовательно, в структуре будут продукты перитектической реакции и оставшиеся избыточные первичные β-кристаллы. Чем ближе точка 2 лежит к точке Р, тем меньше в реакции остается избыточных β-кристаллов. Для сплава, отвечающего по концентрации точке Р, соотношение реагирующих при перитектическом превращении жидкости и β-кристаллов таково, что оно как раз достаточно для образования α-кри-сталлов предельной концентрации. Кристаллизация сплава II. Отличие кристаллизации этого сплава от кристаллизации сплава I состоит в том, что при перитектической температуре имеется избыток жидкой фазы по сравнению с тем количеством, которое необходимо для образования α-кристаллов концентрации Р. Поэтому перитектическое превращение заканчивается исчерпанием β-твердого раствора, и оставшаяся жидкость в интервале между точками 2'-3 кристаллизуется в α-фазу. При этом концентрация жидкости изменяется по кривой С-а, а концентрация образующихся α-кристаллов по Р-3.
