
8.2. Уравнение для энергии.
Уравнение для энергии в методе ММ является суммой сумм, например
![]() ,
(8.1)
,
(8.1)
вкладов для растяжения связей, изменения углов, торсионных и Ван-дер-ваальсовых взаимодействий. В сумму могут добавляться и иные члены. Рассмотрим вклады в выражение (8.1) по отдельности.
8.3.1. Растяжение химических связей. Пусть потенциальная энергия молекулы равна нулю для равновесного значения длины химической связи, соответствующего дну потенциальной ямы. Тогда энергия химической связи в неравновесном состоянии равна
![]() ,
(8.2)
,
(8.2)
где r0 – равновесная длина связи, r - реальная длина связи, kstretch – силовая постоянная связи. r0 и kstretch являются эмпирическими параметрами.
8.3.2. Изменение углов. Изменение углов учитывается так же, как изменение длин химических связей.
![]() .
(8.3)
.
(8.3)
Здесь θ0 – равновесное (стандартное) значение валентного угла, θ – реальное значение валентного угла, kbend – «силовая постоянная» для угла.
Квадратичное приближение для изменения валентного угла является более хорошим приближением, чем для изменений длин химических связей, причем в большинстве случаев оно хорошо работает для значений валентных углов, которые на ±30º отличаются от равновесного значения. Как и в случае химических связей величины рассчитываемых методом ММ валентных углов несколько отличаются от равновесных (стандартных) значений, поскольку их значения являются компромиссом действия различных сил. Это приводит к ненулевому вкладу Vbend(θ) в стерическую энергию равновесной геометрии молекулы.
8.3.3. Торсионный вклад. Торсионная деформация изолированной равновесной структуры означает вращение, т.е. изменение двухгранного угла при связи, соединяющей два атома. Соответствующий вклад является периодической функцией угла.
![]() .
(8.4)
.
(8.4)
Здесь ω – значение двухгранного угла, Vn и n – эмпирические параметры.
8.3.4. Вклад энергии Ван-дер-Ваальса. В ММ считается, что атомы дают вклад в энергию Ван-дер-Ваальса тогда, когда они не связаны химической связью. Для описания Ван-дер-Ваальсовых взаимодействий используются два потенциала. Одним из них является 6-12 потенциал Леннард-Джоунса или его модификация
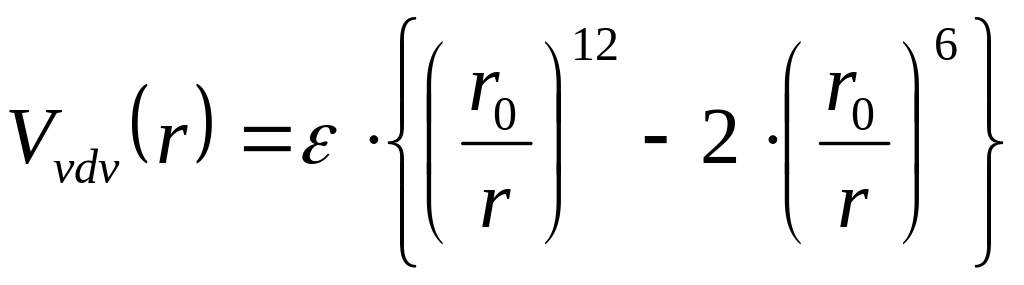 ,
(8.5)
,
(8.5)
где является подгоночным параметром, соответствующим по физическому смыслу глубине минимума на кривой потенциальной энергии для Ван-дер-Ваальсовых взаимодействий двух конкретных атомов. Другим потенциалом этого типа является потенциал Бакингэма
![]() ,
(8.6)
,
(8.6)
причем A, B и C являются подгоночными параметрами.
8.3.5. Кулоновский вклад. Энергия кулоновского взаимодействия появляется благодаря наличию в молекуле постоянных диполей, например, избыточных положительных и отрицательных зарядов на атомах. Вклад от такого взаиодействия определяется по уравнению
![]() ,
(8.7)
,
(8.7)
где 0 – диэлектрическая постоянная вакуума. В варианте MM3, этот член имеет другой вид
![]() .
(8.8)
.
(8.8)
Углы , β и χ определяются, как показано на приведенном ниже рисунке.
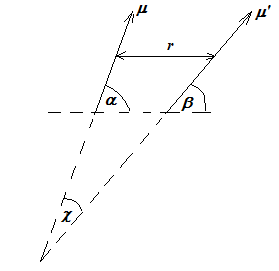
Здесь r - расстояние между центрами связей.
Величиной, принимаемой по умолчанию, является 1.0 для диэлектрической постоянной среды, что соответствует вычислениям, производимым для изолированных молекул в вакууме, но величина по умолчанию должна быть увеличена до 1.5 для учета внутримолекулярных взаимодействий дипольных моментов. В присутствии растворителя для этой константы берется величина, отличная от 1.5.
8.3.6. Вклад от образования внутримолекулярной водородной связи. Если такая водородная связь присутствует в молекулярной системе, то она моделируется при помощи модифицированного потенциала Бакингэма, умноженного на cos θ (L/L0) для учета угла θ между реальной водородной связью в изучаемой молекуле и идеального угла для образования водородной связи вдоль химической связи с равновесной длиной L ковалентной связи атома водорода по сравнению со стандартной длиной связи L0.
8.3.7. Перекрестные члены. Они характеризуют вклады от взаимного влияния различных вкладов в стерическую энергию. Ниже приведены типичные формулы для их вычисления.
![]() ,
(8.9)
,
(8.9)
![]() ,
(8.10)
,
(8.10)
![]() ,
(8.11)
,
(8.11)
![]() ,
(8.12)
,
(8.12)
, (8.13)
. (8.14)
