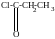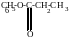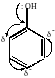- •Теории химического строения
- •Основные положения теории бутлерова:
- •2. Положение о зависимости свойств от химического строения.
- •3. Положение о взаимном влиянии атомов.
- •6. Классификация органических реакций по механизму
- •Пространственное строение предельных углеводородов
- •Способы получения предельных углеводородов
- •Лабораторные способы получения алканов
- •Физические свойства предельных углеводородов
- •I. Замещение
- •II. Окисление
- •IV. Изомеризация предельных углеводородов
- •Номенклатура
- •Способы получения
- •Химические свойства олефинов
- •1. Реакции присоединения
- •2. Реакции окисления
- •3. Реакции полимеризации
- •4. Реакции аллильного замещения
- •Физические свойства
- •Особенности электронного строения диенов с сопряженными связями
- •1. Реакции присоединения
- •Классификация
- •Способы получения
- •Физические свойства
- •Химические свойства
- •I.Реакции нуклеофильного замещения
- •Реакции отщепления галогена
- •III. Реакции отщепления галогеноводорода
- •Карбонильные соединения
- •Способы получения
- •Отличие химических свойств альдегидов и кетонов
- •Химические свойства
- •III. Реакции окисления и восстановления
- •Реакции восстановления
- •Карбоновые кислоты
- •Номенклатура
- •Способы получения
- •4) Дегидратация кислот
- •Определение
- •Классификация
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Основные признаки ароматичности
- •Ароматические соединения
- •Гомологический ряд, изомерия и номенклатура ароматических углеводородов
- •Названия ароматических радикалов
- •Способы получения ароматических углеводородов
- •Б. Синтетические способы получения ароматических углеводородов
- •Химические свойства
- •Механизм электрофильного замещения
- •Нитрование гомологов бензола
- •Реакции присоединения (нетипичны)
- •Галоидпроизводные ароматических углеводородов Классификация, изомерия, номенклатура
- •Получение
- •Физические свойства галогенопроизводных ароматических углеводородов
- •Химические свойства
- •Нитросоединения ароматического ряда
- •1.Нитросоединения с нитрогруппой в ядре
- •Физические свойства
- •Химические свойства
- •II. Реакции в ядре
- •II. Нитросоединения с группой no2 в боковой цепи
- •Способы получения
- •Химические свойства ароматических нитросоединений с группой no2 в боковой цепи
- •Ароматические сульфокислоты
- •Физические свойства
- •Химические свойства
- •I тип реакций. Реакции, характерные для органических кислот.
- •II тип реакции. Восстановление сульфогруппы
- •III тип реакций. Реакции нуклеофильного замещения сульфогруппы
- •IV тип реакций. Реакции электрофильного замещения в ядре идут в соответствии с правилами замещения
- •27. Ариламины. Ароматические амины Классификация
- •I. По положению аминогруппы относительно ароматического ядра.
- •II. По количеству радикалов, связанных с азотом
- •III. По количеству аминогрупп
- •Получение
- •Физические свойства
- •Химические свойства
- •II. Реакции замещения водорода в аминогруппе
- •IV. Окисление
- •V. Реакции замещения в ароматическом ядре
- •VI. Реакции конденсации ароматических аминов с другими органическими и неорганическими соединениями
- •Диазо- и азосоединения
- •Ароматические диазосоединения
- •1. Реакция диазотирования - -получение солей диазония.
- •Химические свойства солей диазония
- •I. Реакции с выделением азота
- •II. Реакции диазосоединений без выделения азота
- •Азокрасители
- •Связь строения с цветностью
- •Ароматические оксисоединения
- •Классификация
- •Физические свойства фенолов
- •Химически свойства фенолов
- •I. Реакции подвижного водорода в группе он
- •II. Реакции электрофильного замещения в ядре
- •III. Окислительно-восстановительные реакции
- •IV. Конденсация фенолов с другими органическими соединениями
- •Ароматические альдегиды и кетоны
- •Способы получения
- •II. Частные способы получения альдегидов и кетонов
- •Физические свойства
- •Химические свойства
- •Ароматические кислоты
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Полициклические ароматические углеводороды и их производные
- •Ароматические углеводороды с изолированными ядрами
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Наиболее важные группы многоядерных соединений. Группа дифенила
- •Группа трифеиилметана
- •Полициклические ароматические углеводороды с конденсированными ядрами
- •Получение
- •Физические свойства
- •Особенности химических свойств
- •Ароматические моноциклические пятичленные гетероциклы
- •Номенклатура гетероциклических соединений
- •Способы получения
- •Физические свойства
- •34. Шестичленные гетероциклы с одним гетероатомом
- •Получение
I. Реакции подвижного водорода в группе он
1) Фенолы, в отличие от спиртов, проявляют вполне выраженные кислотные свойства.
а) образуют солеобразные соединения – феноляты со щелочью;
|
+ NaOH -HOH |
|
||
|
|
|
||
|
|
|
||
2) о-алкилирование фенолов приводит к образованию простых эфиров фенолов. Осуществляется чаще всего действием галоидных алкилов на феноляты.
C6H5Ona + ICH3 C6H5OCH3 + NaI
метилфениловый эфир
3) о-ацилирование фенолов приводит к образованию сложных эфиров фенолов. Осуществляется обычным образом – действием хлорангидридов или ангидридов кислот на фенолы.
С6H5ONa + |
|
|
|
+ NaCl |
фенолят натрия |
хлорангидрид пропионовой кислоты
|
|
фенилпропианат |
|
II. Реакции электрофильного замещения в ядре
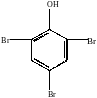
1) Бромирование
Под действием бромной воды идет замещение всех трех атомов водорода в о- и п-положении.
|
+ 3 Br2 3 HBr + |
|
|
|
2,4,6-трибромфенол (белый осадок) |
При избытке брома бромирование может идти дальше, но с перестройкой бензольного кольца на хиноидное, что сопровождается изменением окраски.
2) Нитрование
Реакция нитрования протекает уже при комнатной температуре под действием разбавленной азотной кислоты.
При нитровании избытком HNO3 образуется тринитрофенол.
|
+ 3 HONO2 3 H2O + |
|
(это сильное взрывчатое вещество – пикриновая кислота).
Обладает сильными кислотными свойствами благодаря сильному оттягиванию электронов тремя электроноакцепторными группами NO2.
Сульфирование.
-
комн.
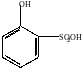
+ HOSO2OH
конц.
-H2O
o-феносульфокислота
нагр.

п-фенолсульфокислота
III. Окислительно-восстановительные реакции
1) Окисление фенолов протекает очень легко даже под действием кислорода воздуха при комнатной температуре (этим объясняется появление окраски). Различными окислителями фенолы окисляются до разных состояний.
|
|
|
|
O H2O + |
|
|
+ O |
|
пирокатехин |
|
о-бензохинон |
|
|
|
|
O H2O + |
|
гидрохинон п-бензохинон
Восстановление фенолов.
Протекает трудно.
а) При перегонке в присутствии Zn-пыли фенол восстанавливается до углеводорода.
C6H5OH + Zn ZnO + C6H6
б) действие водорода в присутствии катализатора группу ОН не затрагивает (гидрируется ядро), т.е.
|
Ni + 3 H2 |
|
|
|
циклогексанол |