
- •1.Предмет изучения и основное содержание биофизики.
- •2. Общие принципы описания кинетического поведения биологических систем, принцип узкого места, понятие фазовой траектории.
- •3. Качественное исследование простейших моделей биопроцессов. Поведение переменных на фазовой плоскости вблизи состояния равновесия.
- •4. Биологические триггеры. Фазовый портрет тригерной системы. Способы переключения стационарных состояний тригерной системы.
- •5. Колебательные процессы в биологии. Фазовый портрет автоколебательной системы.
- •6. Термодинамика систем вблизи равновесия. Первый и второй закон термодинамики. Живые системы.
- •Термодинамика живых систем
- •7. Второй закон термодинамики в открытых системах. Поддержание неравновесных состояний в бисистемах.
- •8. Теорема Пригожина
- •9. Термодинамика систем вдали от равновесия.
- •10. Энтропия, информация и биологическая упорядоченность.
- •11.Пространственная организация макромолекул.
- •Слабые невалентные взаимодействия в биологических системах.
- •13. Электронно-конформационные взаимодействия в макромолекулах
- •14. Спин электрона.
- •18. Механизмы переноса электрона и миграции энергии в биоструктурах.
- •19. Механизмы ферментативного катализа. Конформационные перестройки и высота барьера активации реакции
- •20. Молекулярная организация биологических мембран. Жидкомазаичная модель мембраны. Межмолекулярные взаимодействия в мембранах.
- •21. Механические и конформационные свойства мембран. Фазовые переходы биомембран.
13. Электронно-конформационные взаимодействия в макромолекулах
В основе функционирования макромолекул находятся электронно-конформационные взаимодействия.
Специфика макромолекул – большое число однотипных звеньев (мономеров), которые связаны в линейную цепь. Тепловое движение атомов, атомных групп, которые входят в полимерную цепь, их повороты и вращения вокруг единичных звеньев создают большое число внутренних степеней свободы макромолекул.
Конформация – определенное с точностью до амплитуд валентных колебаний расположение атомов в полимере. Каждое макросостояние биополимера осуществляется большим количеством микросостояний или конформаций (рис. 3.9, 3.10).
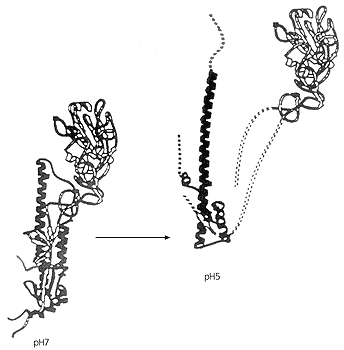
Рис. 3.9. Конформационная перестройка гемагглютинина
Рис. 3.10. Конформац-е перестройки белка приона, вызывающие коровье бешенство (патогенный прион перестраивает стр-ру нормального приона)
Разные конформации макромолекулы получаются путем вращения атомных групп возле отдельных единичных связей, например, С-С связей (рис. 3.11). Атомы, у которых перекрываются электронные оболочки, отталкиваются, вследствие чего возникает тормозящий энергетический потенциал внутреннего вращения.
В разных конформациях молекулы отличаются конформационной энергией. Существуют энергетические барьеры при переходе из одной конформации в другую. Потенциальная энергия внутреннего вращения Е(φ) зависит от угла поворота φ вокруг С-С-связи:
Е(φ) = (Ео/2) (1 – cos3φ)
Потенциальная энергия внутреннего вращения Е(φ) в этане зависит от угла поворота φ вокруг С-С-связи (рис. 3.13).
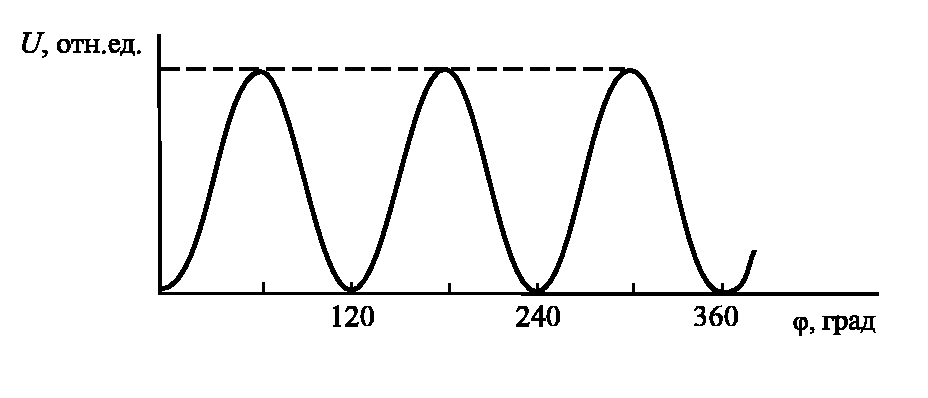
Потенциальная энергия внутреннего вращения в n-бутане зависит от угла поворота: глубокий минимум (0о, 360о) отвечает трансконформации, два других – конформациям, получаемым поворотом из трансположения одной СН3-группы относительно другой на +120о и -120о. Это «свертки» или гошконформации (рис. 3.14).
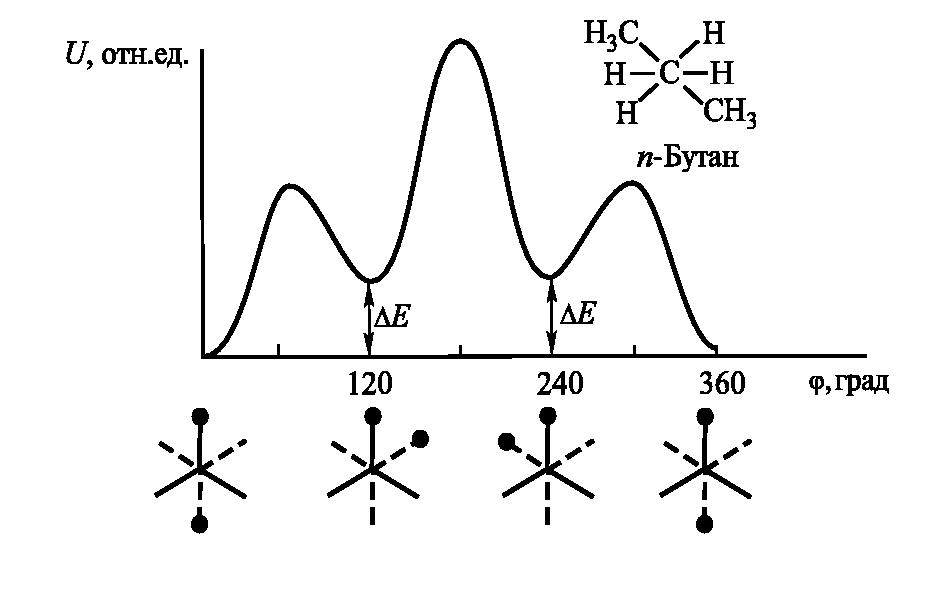
Рис. 3.14. Зависимость потенциальной энергии внутреннего вращения в n-бутане от угла поворота
Cовременные методы позволяют учесть наиболее существенные межатомные невалентные взаимодействия и определить энергетически оптимальные конформации сравнительно небольших участков полипептидной цепи.
Белковая молекула в нормальных условиях характеризуется минимумом конформационной энергии, соответствующий нескольким близким конформационным подсостояниям, между которыми возможны спонтанные флуктуационные переходы.
При сворачивании белка происходит падение энтропии из-за роста упорядоченности. Проигрыш за счет уменьшения энтропии (T∆S < 0) компенсируется выигрышем по энергии (∆U < 0):
∆ F = ∆ U - T∆S < 0 (|∆U | > | T ∆S |)
Активная конформация белка начинается уже на рибосоме в процессе трансляции.
Изменение конформационной структуры белка за счет внешних воздействий (рН, температура, ионный состав) отражается на его функциональной активности.
Характерные времена ферментативных процессов не превышают 10-2 – 10-3 с, также быстро должны происходить конформационные перестройки в макромолекулах.
14. Спин электрона.
Помимо энергии, связанной с движением вокруг ядра атома, электрон обладает еще и дополнительной энергией, связанной с вращением вокруг своей оси наподобие волчка, откуда и происходит слово спин (спин — по-английски верчение). Поскольку же электрон имеет электрический заряд, то при его вращении возникает круговой электрический ток, а следовательно, и магнитное поле, превращающее электрон в маленький электромагнитик, имеющий два магнитных полюса (рис. 3.15). Так как электрон может вращаться в разных направлениях — по часовой стрелке и против нее, то он может пребывать в двух различных энергетических, или, как говорят, спиновых, состояниях. Спин электрона вызывает ряд дополнительных взаимодействий, играющих исключительно важную роль в физических свойствах атома и проявляющихся при электронно-конформационных перестройках.
![]() Рис.
3.15. Спин электрона
Рис.
3.15. Спин электрона
Пример. Конформационные перестройки белка миоглобина (переносчика кислорода в мышцах). Миоглобин содержит один гем и одну полипептидную цепь из 153 аминокислотных остатков, которые распределены по 8 α-спиральным участкам А-Н (рис. 3.16).
Рис. 3.16. Пространственная структура миоглобина (кашалота) в проекции ху
В Fe+2 шесть внешних электронов заполняют 3 d-орбитали таким образом, что на одной из них расположены два электрона с антипаралельными спинами, а четыре оставшиеся орбитали заполняются каждая одним электроном, так что суммарный спин равен 2. В составе гема из-за отрицательно заряженных лигандов d-орбитали различаются по энергии, поэтому ион Fe может находиться в разных спиновых состояниях. В высокоспиновом обладает суммарным спином d-электронов = 2, в низкоспиновом – 0.
Переход из низкоспинового состояния в высокоспиновое увеличивает диаметр иона и приводит к его выходу из плоскости гема, что обусловливает конформационные изменения в «белковом» окружении гема.
В низкоспиноном состоянии Fe+2 обладает координационным числом 5 и расположен вне плоскости гема. Образование связи кислород – железо переводит его в низкоспиновое состояние, увеличивая число лигандов в координационной сфере до шести. Присоединение кислорода индуцирует ряд конформационных изменений молекулы, меняется конформация α-субединиц. Устанавливается новая равновесная оксиформация при другом взаимном расположении атомных групп в белке.
Механизм проникновения полипептидной цепи в мембрану обусловлен центральной неполярной областью бислоя, наиболее энергетически выгодными являются конформации с максимальным числом внутримолекулярных водородных связей: α-спираль и β-бочонки, содержащие по 19-23 и 8-9 аминокислотных остатков, соответственно (рис. 3.17, 3.18).
Рис. 3.17. Белок α-структурный пронизывает липидный бислой
Рис. 3.18. Белок β-структурный образует ионную пору
Мембранный домен бактериородопсина состоит из семи α-спиралей, содержащих по 20-25 остатков.
Порины некоторых бактериальных токсинов, а также транспортер глюкозы представляют собой цилиндры из антипаралельных β-тяжей, пронизывающих бислой и образующих пору диаметром до 10 Ǻ.
В калиевом канале ион-проводящая пора сформирована четырьмя α-субединицами. Воротный механизм – усеченный конус из 4 коротких спиралей. Регуляторный участок канала расположен между α-субединицами, образующими пору (рис. 3.19).

Рис. 3.19. Ион-проводящая пора в мембране
Электронные переходы в биополимерах.
Изменения электронного состояния белка вызывают определенные конформационные переходы, которые происходят в направление достижения нового равновесия и минимума энергии. Полная энергия молекулы представлена суммой электронной Еэл, колебательной Екол и вращательной Евр составляющих:
Е = Еэл + Екол+ Евр, где обычно Еэл>> Екол>> Евр.
Согласно квантовой механике, положение электрона в пространстве описывается волновой функцией ψ (x, y, z), зависящей от пространственных координат x, y, z.
Квадрат абсолютной величины волновой функции |ψi (x, y, z )|2 для данного состояния i в точке (x, y, z) дает вероятность нахождения электрона в элементе объема dx dy dz:
pi (x, y, z) = |ψi (x, y, z )|2 dz dy dz.
Уравнение Шредингера связывает энергию электронной системы с волновой функцией:
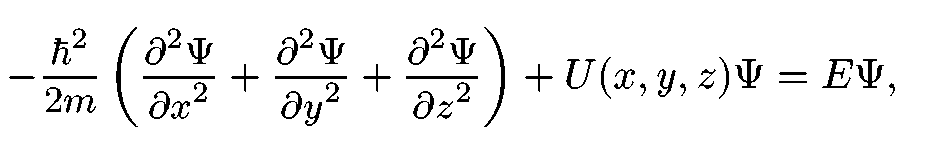
U (x, y, z) – потенциальная энергия электрона; Е – полная энергия системы; m – масса частицы, ħ = h/2π (h – постоянная Планка).
Уравнение позволяет найти электронные волновые функции, или электронные орбитали, например, у атома водорода (рис. 3.20).
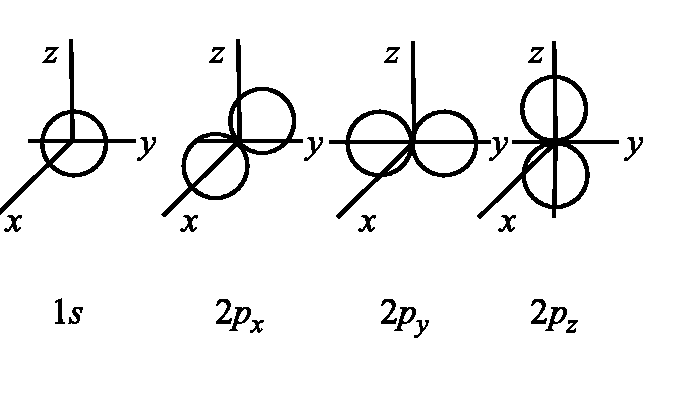
Рис. 3.20. Форма и направление орбиталей 1s, 2px, 2py, 2pz атома водорода
Молекулы образуются при взаимодействии атомных орбиталей электронов. Волновая функция будет описывать движение и распределение общих электронов и зависит от их координат (рис. 3.21).
Рис. 3.21. Форма перекрывания электронных облаков: 1—s-состояние, 2—р-состояние, 3 — s- и р-состояния
Расщепление энергетических уровней.
При образовании молекулы водорода исходный уровень 1 s расщепляется на два уровня:
На первом электронная плотность имеет максимум между ядрами и стягивает их, образуя стабильную молекулу. σ- связи характеризуются симметрией электронного облака по отношению к вращению вокруг оси химической связи.
Второй электронный уровень отличается большими значениями энергии, чем энергия двух свободных атомов, поэтому стабильной системы не образуется.
Электрон имеет собственный магнитный момент или спин. Согласно принципу Паули, полная волновая функция должна быть ассиметрична, т.е. на симметричной орбитали располагаются электроны, отличающиеся ориентацией спинов. Она обусловливает нижнее устойчивое энергетическое состояние системы.
Орбиталь с одинаковыми спинами электронов, проводящими большую часть времени вдали друг от друга, имеет разрыхляющий характер – ядра отталкиваются друг от друга.
При возбуждении светом один из спаренных по спину электронов переходит со связывающей орбитали ψС на разрыхляющую орбиталь ψА. Электроны имеют при этом антипаралельные спины и молекула находится в синглетном состоянии. Если реализуется состояние с паралельными спинами, то молекула оказывается в триплетном состоянии. Триплетный уровень по энергии ниже возбужденного синглетного, т.к. энергия электрон-электронного отталкивания меньше (рис. .

Рис. Синглетное (S1) и триплетное (T1) состояния
При возбуждении светом один из спаренных электронов переходит со связывающей орбитали ψС на разрыхляющую ψА. В этом случае электроны имеют антипараллельные спины и молекула находится в синглетном состоянии. Если реализуется состояние с параллельными спинами, то молекула оказывается в триплетном состоянии. Триплетный уровень по энергии лежит ниже возбужденного синглетного, так как энергия электрон-электронного отталкивания в этом случае меньше
В молекулах белка изменение электронного состояния одного участка (активный центр) дает начало последовательным конформационным превращениям.
Энергия электронного возмущения может мигрировать от молекулы – донора к молекуле – акцептора. Миграция энергии не сопровождается химическими изменениями, это физический процесс.
Электронная энергия в биоструктурах может переноситься и в процессе транспорта электронов независимо от поступательных движений молекул.
