
Кольцевой механизм, открытый Зинером в 1950году:
Этот механизм объяснил явление самодиффузии. Он не связан с наличием дефектов. Зинер предположил, что диффузия происходит путем одновременного поворота нескольких атомов. Этот метод получил название кольцевого.
Коэффициент диффузии и величины его определяющие.
В качестве примера рассмотрим диффузию в ГЦК решетке по вакансионному механизму.
Рассмотрим диффузию
в направлении оси х. Пусть в плоскости
1 находится n1 атомов.
А в плоскости 2 – n2
атомов, но
![]() .
.
Г1 – число переходов в единицу времени атомов с плоскости 1 на плоскость 2.
Г2 – число переходов в единицу времени атомов с плоскости 2 на плоскость 1.
Г1![]() ,
,
где 1 – частота колебаний атомов n1 в направлении оси х; р1 – число мест, на которые может перейти диффундирующий атом.
Для данной решетки р1=4, но р1 нужно умножить на вероятность того, что места являются свободными. Кроме того, частота колебаний должна быть помножена на вероятность того, что это колебание приведет к перескоку:
![]()
где 1 – вероятность того, что частота приведет к перескоку; 1 – вероятность наличия свободных мест.
![]() .
.
Если рассматривать диффузию собственных атомов в свободной решетке, то тогда 1=2, р1=р2, 1=2 и 1=2. Тогда результирующий поток, при условии n1>n2:
![]()
Перейдем от числа атомов к концентрациям. Поскольку кристалл имеет анизотропию, то в качестве концентраций надо брать погонную концентрацию (не на единицу объема, а на единицу длины):
![]()
![]()
Поскольку межатомные расстояния маленькие, то можно считать, что концентрация является квазинепрерывной функцией координаты, поэтому ее можно разложить в ряд Тейлора:
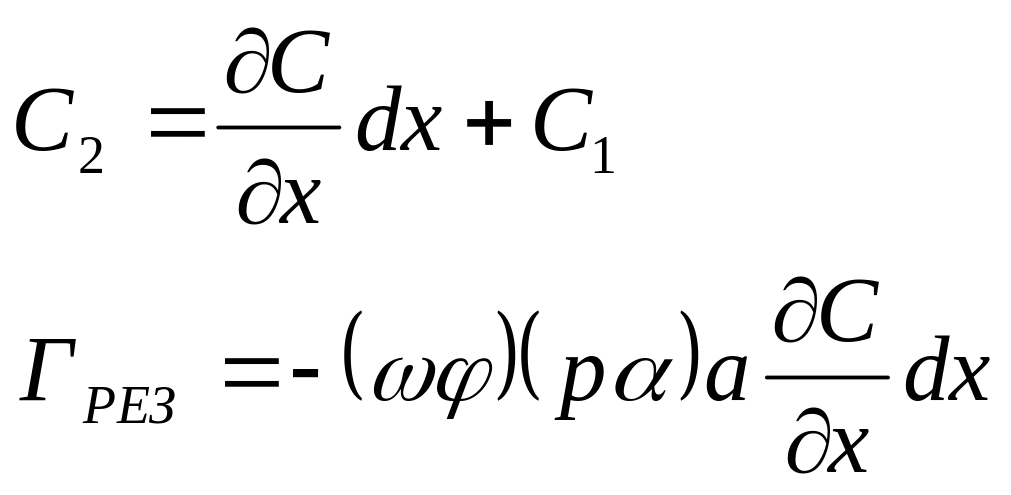
Если dxа, тогда:
![]()
![]() .
.
Коэффициент диффузии зависит от направления, т.к. в его выражение входит постоянная решетки а. Чтобы его посчитать, надо знать величины, входящие в выражение.
Величина р зависит
от вида решетки. Величина
- мольная доля вакансий (константа
Шоттки, или константа Френкеля, т.е.
![]() или
или
![]() ).
Для оценки частотного фактора (),
надо рассматривать как диффундирующий
атом движется. Для перехода на новое
место атому нужно преодолеть потенциальный
барьер. Изменения энергии этого атома
по координате выглядит т.о.:
).
Для оценки частотного фактора (),
надо рассматривать как диффундирующий
атом движется. Для перехода на новое
место атому нужно преодолеть потенциальный
барьер. Изменения энергии этого атома
по координате выглядит т.о.:
т.1 – исходное положение
т.2 – конечное положение
т.3 – перевальная точка.
Процесс перехода можно условно записать как мономолекулярную обратимую реакцию:
![]()
где N – концентрация атомов в т.1; n – концентрация атомов в т.2.
Работа этого процесса:
![]()
![]()
![]()
![]() (на моль пересчет)
(на моль пересчет)
где КР – и есть вероятность преодоления потенциального барьера.
Пусть v – средняя скорость атомов в направлении оси х:
![]()
– эффективная толщина барьера: []=м.
Тогда
![]()
![]() (на частицу пересчет)
(на частицу пересчет)
В направлении оси
х частицы перескакивали бы с такой
частотой (![]() ),
но реально их меньше. Тогда:
),
но реально их меньше. Тогда:
![]()
![]()
Если собственный атом в собственной решетке, то m(кристалла)=1/2m(атома) – приведенная масса.
В справочниках приводят выражение для коэффициента диффузии:
![]()
где Е
– энергия активации диффузии,
![]() ;
D0 – предэкспонента.
;
D0 – предэкспонента.
В справочниках полагают, что D0=const в определенных температурных интервалах. Но на самом деле, она от температуры зависит слабо. Если диффузия не по вакансиям, то энергия образования вакансий =0.
Коэффициенты диффузии при нормальных условиях: 10–8–10–10 см2/с.
