
- •Глава VI. Ректификация
- •VI. Ректификация
- •6.1. Сущность процесса ректификации бинарных смесей
- •6.2. Число теоретических ступеней контакта (теоретических тарелок)
- •6.3. Принципиальное устройство ректификационной колонны
- •6.4. Материальный и тепловой баланСы ректификационной колонны
- •6.5. Флегмовое (паровое) число
- •6.6. Способы создания орошения в колонне
- •6.7. Способы подвода тепла в нижнюю часть колонны
- •6.8. Выбор давления в ректификационной колонне
- •6.9. Основные типы ректификационных колонн
- •6.10. Эксплуатация колонных аппаратов, методы воздействия на эффективность работы колонны.
Глава VI. Ректификация
VI. Ректификация
6.1. Сущность процесса ректификации бинарных смесей
При осуществлении процессов однократного испарения или однократной конденсации можно получить пар более богатый низкокипящим компонентом (НКК), а жидкость более богатую высококипящим компонентом (ВКК), чем исходная смесь. Однако достаточно хорошая степень разделения компонентов не достигается. В случае многократных или постепенных процессов испарения и конденсации можно получить желаемые составы паровой и жидкой фаз, но масса получаемых продуктов незначительна по сравнению с массой исходной смеси.
Для получения продуктов желаемой степени чистоты служит процесс ректификации. Как следует из теории массообменных процессов, при взаимодействии неравновесных паровой и жидкой фаз в результате процессов массо-и теплообмена система придет в состояние равновесия. При этом присутствующие в фазах компоненты будут перераспределяться между ними. В результате вновь образованные паровая и жидкая фазы будут отличаться по составу от вступивших в контакт паров и жидкости. Пары обогатятся НКК, а жидкость ВКК. При данном давлении для осуществления этого процесса температура вступающих в контакт паров должна быть выше, чем жидкости. После контакта температуры обеих фаз выравниваются.
Осуществляя многократно контактирование неравновесных потоков паровой и жидкой фаз, можно изменить их составы в желаемой степени. В этом и состоит сущность процесса ректификации. Процесс ректификации проводят в специальных аппаратах — ректификационных колоннах, заполненных контактными устройствами (тарелками, насадками и т. п.).
При расчетах процесса ректификации обычно пользуются понятием теоретической тарелки.
6.2. Число теоретических ступеней контакта (теоретических тарелок)
Число тарелок, т.е. число ступеней контактирования паровой и жидкой фаз, должно быть таким, чтобы пар на верху колонны и жидкость внизу достигли заданных концентраций низкокипящих и высококипящих компонентов.
Число тарелок, необходимых для разделения данной смеси, определяют графически или аналитически. Для графического определения необходимо иметь кривую равновесия фаз и кривые концентраций для верхней и нижней частей колонны. Под теоретической тарелкой понимаю такую, на которой массообменивающиеся фазы приходят к полному равновесию. Это допущение условно. Практически даже на тарелках самой совершенной конструкции невозможно достигнуть полного равновесия фаз, поэтому число реальных тарелок всегда больше числа теоретических:
![]()
где N — реальное число тарелок в колонне; NТ — теоретическое число тарелок; η— средний к.п.д. тарелок.
Средний к.п.д. тарелок зависит от различных факторов, и в первую очередь от конструкции тарелки и режима ее работы. Значение к.п.д. обычно устанавливают на основе экспериментальных данных, реже – путем приближенных расчетов. Оно колеблется в довольно больших пределах, например для желобчатых тарелок η = 0,3 – 0,7. Схема ступени контакта (теоретической тарелки), при которой обеспечивается получение равновесных потоков фаз, покидающих контактную зону, представлена на рис. 6.2.1.

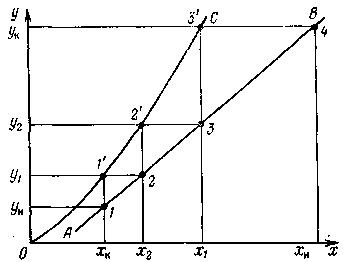
Рис.6.2.1. Схема потоков для теоретической тарелки.
Рис. 6.2.2. Построение числа теоретических тарелок на диаграмме х—у: АВ — рабочая линия; ОС — линия равновесия.
Потоки фаз G и L, имеющие концентрации компонента у1 и х1, поступают в контактную зону, где в результате процесса массообмена концентрации изменяются до у2 и х2. Согласно определению теоретической контактной ступени (теоретической тарелки), эти концентрации находятся в равновесии.
Концентрации потоков у1 и х2, у2 и х1, встречающихся на соответствующих уровнях, удовлетворяют уравнению рабочей линии.
Понятие о теоретической тарелке существенно упрощает расчеты массообменных процессов, так как необходимо располагать только уравнениями равновесия и рабочей линии.
На рис. 6.2.2 представлено построение числа теоретических тарелок (ЧТТ) с использованием диаграммы х—у.
Поступающий в аппарат поток фазы G состава ун и уходящий из аппарата поток фазы L состава хк соответствуют уравнению рабочей линии (точка 1). Поток фазы L состава хк покидает контактную зону и находится в равновесии с потоком фазы G состава y1, покидающей ту же зону (точка 1'). Потоки фаз G состава y1 и L состава х2 отвечают уравнению рабочей линии (точка 2). Составы х2 и y2 находятся в равновесии (точка 2'). Аналогично находим точки 3 и 3' и, наконец, точку 4, определяющую составы хн поступающей в аппарат фазы L и ук уходящей из аппарата фазы G. Таким образом, изменение концентраций фаз ун — ук и хн — хк достигается при построении ступенчатой линии 1, 1', 2, 2', 3, 3', 4 между рабочей и равновесной линиями. Число ступеней (в данном случае три) и будет числом теоретических тарелок NТ, необходимых для данного разделения смеси.
