
- •Глава IV. Физико-химические свойства нефти и её фракций
- •IV. Физико-химические свойства нефти и ее фракций
- •4.1. Средняя температура кипения (фракционный состав)
- •Лабораторный контроль
- •4.2. Объём, удельный объём, масса и плотность нефтепродукта
- •4.3. Давление насыщенных паров
- •Лабораторные методы определения днп
- •4.4. Критические параметры и отклонение реальных газов от идеального
- •4.5. Вязкость нефтепродуктов
- •4.6. Некоторые характерные температуры нефтепродуктов
- •4.6.1. Температура вспышки
- •4.6.2. Температура воспламенения
- •4.6.3. Температура самовоспламенения
- •Лабораторный контроль
- •4.6.4. Температура помутнения
- •Лабораторный контроль
- •4.6.5. Температура застывания
- •Лабораторный контроль
- •4.6.6 Температура полного растворения в анилине ("анилиновая точка")
- •4.6.7. Температура точки росы ("точка росы")
- •4.7. Некоторые тепловые свойства нефтепродуктов
- •4.7.1. Удельная теплоемкость
- •4.7.2. Теплопроводность
- •4.7.3. Теплота сгорания
- •Лабораторный контроль
- •4.8. Моторные свойства
- •4.8.1. Детонационная стойкость
- •4.8.2. Воспламеняемость
- •4.9. Некоторые технологические и эксплуатационные свойства
- •4.9.1. Фильтруемость
- •4.9.2. Коррозионная активность
- •3.9.3. Кислотность
Глава IV. Физико-химические свойства нефти и её фракций
IV. Физико-химические свойства нефти и ее фракций
К физико-химическим свойствам нефти, ее фракций и конечных нефтепродуктов относится комплекс показателей, характеризующих их физические свойства и их связь с химическим составом, а также свойства, определяющие поведение нефтепродукта при использовании его потребителем.
4.1. Средняя температура кипения (фракционный состав)
Кипение – переход жидкости в пар, происходящий с образованием в объеме жидкости пузырьков пара или паровых полостей. Пузырьки растут вследствие испарения в них жидкости, всплывают, и содержащийся в пузырьках насыщенный пар переходит в паровую фазу над жидкостью. Кипение начинается, когда при нагреве жидкости давление насыщенного пара над её поверхностью становится равным внешнему давлению. Температура, при которой происходит кипение жидкости, находящейся под постоянным давлением, называется температурой кипения (Ткип). Строго говоря, Ткип соответствует температуре насыщенного пара (температуре насыщения) над плоской поверхностью кипящей жидкости, так как сама жидкость всегда несколько перегрета относительно Ткип. При стационарном кипении температура кипящей жидкости не меняется. С ростом давления Ткип увеличивается (ур-е Клайперона-Клазиуса). Предельной температурой кипения является критическая температура вещества. Температура кипения при атмосферном давлении приводится обычно как одна из основных физико-химических характеристик химически чистого вещества.
Температура кипения – важная физическая величина, характеризующая большинство веществ. Однако к нефти и ее фракциям она в строгом понятии применена быть не может, поскольку нефть и ее фракции – смесь очень большого количества углеводородов и других химических соединений, разделить которую на эти индивидуальные вещества невозможно.
Дискретный ряд температур выкипания индивидуальных веществ, из которых состоит нефть, заменяется при определении фракционного состава нефти монотонной кривой зависимости "истинных" (усредненных) температур кипения, от выхода фракций нефти при ее кипении (состав нефти по ИТК). Эта монотонная кривая ИТК строится по конечному числу экспериментальных точек, при этом каждая из точек выражает некую усредненную температуру кипения большой группы углеводородов, фиксируемую в момент отбора фракции.
Для технологических расчетов фракционный состав нефти должен быть представлен дискретным рядом компонентов с фиксированными (имитированными) температурами кипения, чтобы можно было по этим температурам определять их другие физические свойства. Для этого пользуются понятием средней температуры кипения.
Обычно величиной средней температуры кипения характеризуют не в целом нефть или полученный из нее нефтепродукт, интервал кипения которых составляет сотни градусов, а узкие их фракции (условные компоненты), на которые делят весь интервал кипения по кривой ИТК.
Это деление может осуществляться тремя способами (рис. 4.1.1.):
по шкале температур, когда задают интервал выкипания каждой узкой фракции (обычно 10 – 20 °С) и по оси абсцисс определяют их выход – Х1, Х2, Х3 и т. д. Такой способ удобен, когда кривая ИТК охватывает интервал температур выкипания более 100 – 150°С;
по шкале выхода фракции, когда задают выход каждой узкой фракции [обычно 5 – 10% (мас.), % (об.) или % (мольн.), в зависимости от того, как выражается выход фракций] и по оси ординат определяют интервалы их выкипания: Δ t1, Δ t2…и т. д. Такой способ удобен, когда кривая ИТК охватывает интервал температур выкипания менее 100 – 150 °С;
по точкам фактического отбора фракций при экспериментальном определении состава по ИТК, когда известны и температурный интервал отбора фракций, и их выход.
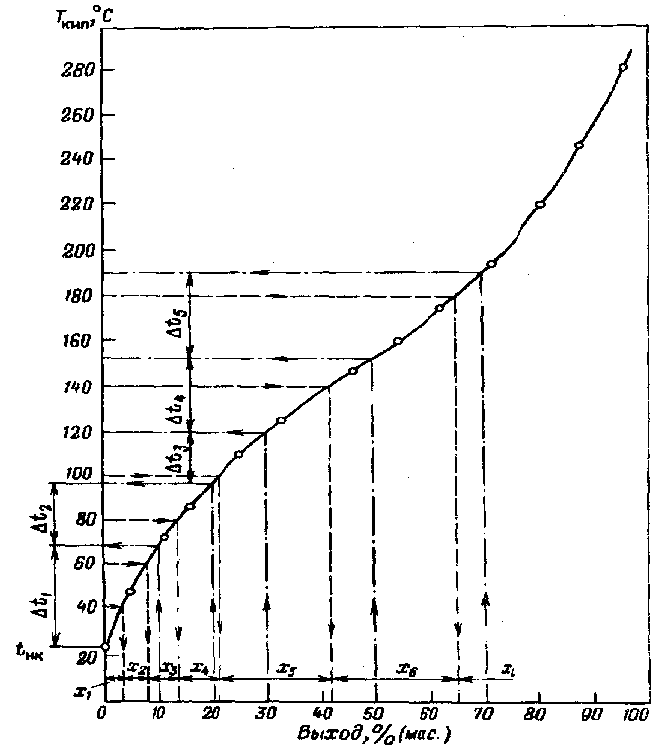
Рис. 4.1.1. Представление кривой ИТК условными компонентами (о – экспериментальные точки; пунктир – деление на узкие фракции по шкале температур кипения; штрих-пунктир – то же по шкале выхода фракций)
Фракция объединяет все соединения, которые кипят между какими-либо двумя температурами, а эти температуры называют границами кипения фракции или пределами выкипания.
Обычно сырая нефть содержит следующие фракции:
Т кипения, оС |
Фракции |
Менее 32 |
Углеводородные газы (метан, этан, пропан, бутан) |
32 – 105 |
Прямогонный бензин (газолин) |
105 – 160 |
Нафта (тяжёлый бензин, бензино-лигроиновая фракция, лигроин) |
160 – 230 |
Керосин |
230 – 430 |
Газойль |
Выше 430 |
Остаток (мазут) |
Как уже отмечалось в Главе I, конечная температура выкипания фракций различных газовых конденсатах находится в пределах 280-360оС. Следовательно, доля углеводородных газов и бензинов (как более низко кипящих фракций) в нём больше, чем в нефти.

Если сделать анализ кривых ИТК данных газовых конденсатов, то можно сделать вывод, что в газовом конденсате 1 больше содержится растворённых газов (пропанов и бутанов) и бензиновых фракций, при этом меньше содержится керосиновых фракций. Конец кипения фракций выше, чем у оппонента, что говорит о том, что в газовом конденсате 1 присутствуют более высококипящие фракции.
В этом и состоит технологическая задача исследования углеводородного сырья – изучить компонентный и фракционный составы смеси, вычислить потенциалы различных фракций, изучить их свойства и сделать вывод – какой вид переработки необходимо запроектировать и какие цели при этом достичь.
