
25. Буферные системы крови - фосфатная
Фосфатная буферная система содержится как в крови, так и в клеточной жидкости других тканей, особенно в почках.
В
клетках она представлена КН2РО4
и К2НРО4.
В плазме крови и межклеточном пространстве
NaH2PO4
и Na2HPO4.
Основную роль в механизме действия этой
системы играет ион
 :
:
⇄ Н+
+

кислота сопр.основание
Увеличение
концентрации Н+
приводит к сдвигу реакции влево, т.е. к
образованию кислоты:
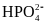 +
Н+
⇄
+
Н+
⇄

основание сопр. кислота
Белковые
буферные системы являются амфолитными,
т.к. в их состав входят
– аминокислоты, содержащие группы с
кислотными свойствами (–СООН и –
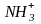 )
и основными свойствами (–СОО–
и –NH2).
Механизм действия такой буферной системы
можно представить следующим образом:
)
и основными свойствами (–СОО–
и –NH2).
Механизм действия такой буферной системы
можно представить следующим образом:
кислотная буферная система
а) H3N+ – R – COOH + OH– ⇄H3N+ – R – COO– + H2O
белок–кислота
б) H3N+ – R – COO– + H+ ⇄H3N+ – R – COOН
соль белка–кислоты
(сопряженное основание)
основная буферная система
а) H2N – R – COO– + Н+ ⇄H3N+ – R – COO–
белок–основание
б) H3N+ – R – COO– + ОН– ⇄H2N – R – COO– + Н2О
соль белка–основания
(сопряженная кислота)
где R – макромолекулярный остаток белка.
Роль белков плазмы крови в гомеостазе ионов водорода весьма мала.
26. Роль буферных систем. Буф емкость.
Действие всех буферных систем организма взаимосвязаны. Поступившие извне или образовавшиеся в процессе обмена веществ Н+ ионы связываются в слабо диссоциирующие соединения, поэтому в жидкостях организма содержится значительно меньше свободных ионов Н+, чем поступает туда.
Буферная емкость
Способность буферного раствора сохранять значение рН при добавлении сильной кислоты или щелочи приблизительно на постоянном уровне характеризует буферная емкость.
Буферная емкость (В) - это число молей эквивалента сильной кислоты или щелочи, которое необходимо добавить к 1 л буферного раствора, чтобы сместить его рН на единицу.
Буферная емкость системы определяется по отношению к добавляемым кислоте (Вкисл.) или основанию (щелочи) (Восн.) и рассчитывается по формулам:
Вкисл.=
 Восн.=
Восн.=

где V(HA), V(B) - объемы добавленных кислоты или щелочи, л.; Сн(НА), Сн(В) - молярные концентрации эквивалента соответственно кислоты и щелочи; V(б.р.) - объем исходного буферного раствора, л.; рНо, рН - значения рН буферного раствора до и после добавления кислоты или щелочи; |рН-рНо| - разность рН по модулю.
Буферная емкость по отношению к кислоте (Вкисл.) определяется концентрацией (количеством эквивалентов) компонента с основными свойствами; буферная емкость по отношению к основанию (Восн.) определяется концентрацией (количеством эквивалентов) компонента с кислотными свойствами в буферном растворе.
Максимальная буферная емкость при добавлении сильных кислот и оснований достигается при соотношении компонентов буферного раствора равном единице, когда рН = рК, при этом Восн. = В кисл.
буферная емкость в основном зависит от соотношения концентраций компонентов и их абсолютных концентраций, а следовательно, от разбавления.
27. Комплексные соединения.
Комплексные соединения — частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения к данному иону (или атому), называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений (координационная теория) была предложена в 1893 г. А. Вернером.
Комплексные соединения мало диссоциируют в растворе (в отличие от двойных солей). Комплексные соединения могут содержать комплексный малодиссоциирующий анион ([Fe(CN)6]3−), комплексный катион ([Ag(NH3)2]+) либо вообще не диссоциировать на ионы (соединения типа неэлектролитов, например карбонилы металлов). Комплексные соединения разнообразны и многочисленны.
Комплексное соединение – химическое вещество, в состав которого входят комплексные частицы. Комплексная частица – сложная частица, способная к самостоятельному существованию в кристалле или растворе, образованная из других, более простых частиц, также способных к самостоятельному существованию. Иногда комплексными частицами называют сложные химические частицы, все или часть связей в которых образованы подонорно-акцепторному механизму.
Комплексообразователь – центральный атом комплексной частицы. Обычно комплексообразователь – атом элемента, образующего металл, но это может быть и атомкислорода, азота, серы, йода и других элементов, образующих неметаллы. Комплексообразователь обычно положительно заряжен и в таком случае именуется в современной научной литературе металлоцентром; заряд комплексообразователя может быть также отрицательным или равным нулю.
Лиганды – атомы или изолированные группы атомов, располагающиеся вокруг комплексообразователя. Лигандами могут быть частицы, до образования комплексного соединения представлявшие собой молекулы (H2O, CO, NH3 и др.), анионы (OH−, Cl−, PO43− и др.), а также катион водорода H+.
Внутренняя сфера комплексного соединения – центральный атом со связанными с ним лигандами, то есть, собственно, комплексная частица.
Внешняя сфера комплексного соединения – остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями, включая водородные.
Координационное число (КЧ) – число - связей, образуемых центральным атомом с лигандами. Для комплексных соединений с монодентантными лигандами КЧ равно числу лигандов, а в случае полидентантных лигандов - числу таких лигандов, умноженному на дентатность.
28.Классификация КС
Классификация
Существует несколько классификации комплексных соединений в основу которых положены различные принципы.
[править]По заряду комплекса
1) Катионные комплексы образованы в результате координации вокруг положительного иона нейтральных молекул (H2O, NH3 и др.).
[(Zn(NH3)4)]Cl2 — хлорид тетраамминцинка(II) [Co(NH3)6]Cl2 — хлорид гексоамминкобальта(II)
2) Анионные комплексы: в роли комплексообразователя выступает атом с положительной степенью окисления, а лигандами являются простые или сложные анионы.
K2[BeF4] — тетрафторобериллат(II) калия Li[AlH4] — тетрагидридоалюминат(III) лития K3[Fe(CN)6] — гексацианоферрат(III) калия
3) Нейтральные комплексы образуются при координации молекул вокруг нейтрального атома, а так же при одновременной координации вокруг положительного иона — комплексообразователя отрицательных ионов и молекул.
[Ni(CO)4] — тетракарбонилникель [Pt(NH3)2Cl2] — дихлородиамминплатина(II)
[править]По числу мест занимаемых лигандами в координационной сфере
1) Монодентатные лиганды. Такие лиганды бывают нейтральными (молекулы Н2О, NH3, CO, NO и др.) и заряженными (ионы CN−, F−, Cl−, OH−, SCN−, S2O32− и др.).
2) Бидентатные лиганды. Примерами служат лиганды: ион аминоуксусной кислоты H2N — CH2 — COO−, оксалатный ион −O — CO — CO — O−, карбонат-ион СО32−, сульфат-ион SO42−.
3) Полидентатные лиганды. Например, комплексоны — органические лиганды, содержащие в своем составе несколько групп −С≡N или−COOH (этилендиаминтетрауксусная кислота — ЭДТА). Циклические комплексы, образуемые некоторыми полидентатными лигандами, относят к хелатным (гемоглобин и др.).
[править]По природе лиганда
1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4 и др.
2) Аквакомплексы — в которых лигандом выступает вода: [Co(H2O)6]Cl2, [Al(H2O)6]Cl3 и др.
3) Карбонилы — комплексные соединения, в которых лигандами являются молекулы оксида углерода(II): [Fe(CO)5], [Ni(CO)4].
4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. К ним относятся комплексные соли: K2[PtCl4], комплексные кислоты: H2[CoCl4], H2[SiF6].
5) Гидроксокомплексы — комплексные соединения, в которых в качестве лигандов выступают гидроксид-ионы: Na2[Zn(OH)4], Na2[Sn(OH)6] и др.
[править]Номенклатура
1) В названии комплексного соединения первым указывают анион|отрицательно заряженную часть — анион, затем положительную часть — катион.
2) Название комплексной части начинают с указания состава внутренней сферы. Во внутренней сфере прежде всего называют лиганды — анионы, прибавляя к их латинскому названию окончание «о». Например: Cl− — хлоро, CN− — циано, SCN− — тиоцианато, NO3− — нитрато, SO32− — сульфито, OH− — гидроксо и т. д. При этом пользуются терминами: для координированного аммиака — аммин, для воды — аква, для оксида углерода(II) — карбонил.
3) Число монодентатных лигандов указывают греческими числительными: 1 — моно (часто не приводится), 2 — ди, 3 — три, 4 — тетра, 5 — пента, 6 — гекса. Дляполидентатных лигандов (например, этилендиамин, оксалат) используют бис-, трис-, тетракис- и т. д.
4) Затем называют комплексообразователь, используя корень его латинского названия и окончание -ат, после чего римскими цифрами указывают (в скобках) степень окисления комплексообразователя.
5) После обозначения состава внутренней сферы называют внешнюю сферу.
6) В названии нейтральных комплексных частиц комплексообразователь указывается в именительном падеже, а степень его не указывается, так как она однозначно определяется, исходя из электронейтральности комплекса.
Примеры:
K3[Fe(CN)6] — гексацианоферрат(III) калия
(NH4)2[PtCl4(OH)2] — дигидроксотетрахлороплатинат(IV) аммония
[Сr(H2O)3F3] — трифторотриаквахром
[Сo(NH3)3Cl(NO2)2] — динитрохлоротриамминкобальт
[Pt(NH3)4Cl2]Cl2 — хлорид дихлоротетраамминплатины(IV)
[Li(H2O)4]NO3 — нитрат тетрааквалития
29. Свойства КС
Комплексные соединения в организмах обычно координируются ионами переходных металлов, например Mn, Co, Fe V(т.н. «биологически активных»). Содержание этих металлов в организмах очень мало, и уже из этого можно сделать предположение, что значение комплексов (доказанное прямым опытом – это почти всегда так) должно быть связано с катализом, т.к. именно активные катализаторы могут способствовать быстрым изменениям состава вещества, действуя в малых концентрациях. Также, комплексы переходных металлов могут играть роль переносчиков групп атомов и целых молекул, закреплять молекулы в определенном положении, поворачивать их, поляризовать и т.п. Металлы-комплексообразователи (таб.1) относятся к группе «жизненно важных», т.е. присутствуют во всех здоровых тканях человека и диапазон их концентраций практически постоянен в каждой ткани, а исключение из организма приводит к тяжелым последствиям.
Комплексные соединения имеют важное значение для живых организмов, так гемоглобин крови образует комплекс с кислородом для доставки его к клеткам, хлорофиллнаходящийся в растениях является комплексом.
Комплексные соединения находят широкое применение в различных отраслях промышленности. Химические методы извлечения металлов из руд связаны с образованием КС. Например, для отделения золота от породы руду обрабатывают раствором цианида натрия в присутствии кислорода. Метод извлечения золота из руд с помощью растворов цианидов был предложен в 1843 г. русским инженером П. Багратионом. Для получения чистых железа, никеля, кобальта используют термическое разложение карбонилов металлов. Эти соединения - летучие жидкости, легко разлагающиеся с выделением соответствующих металлов.
Широкое применение комплексные соединения получили в аналитической химии в качестве индикаторов.
Многие КС обладают каталитической активностью, поэтому их широко используют в неорганическом и органическом синтезах. Таким образом, с использованием комплексных соединений связана возможность получения многообразных химических продуктов: лаков, красок, металлов, фотоматериалов, катализаторов, надежных средств для переработки и консервирования пищи и т.д.
Комплесные соединения цианидов имеют важное значение в гальванопластике, так как из обычной соли бывает невозможно получить настолько прочное покрытие как при использовании комплексов.
30. Титриметрический анализ
Виды титриметрического анализа
Титриметрический анализ использует различные типы химических реакций:
нейтрализации (кислотно-основное титрование) — нейтрализация — это реакции с изменением pH растворов.
окисления-восстановления (перманганатометрия, иодометрия, хроматометрия) — реакции, которые происходят с изменением окислительно-восстановительных потенциалов в системе титрования.
осаждения (аргентометрия) — реакции, протекающие с образованием малорастворимого соединения, при этом изменяются концентрации осаждаемых ионов в растворе.
комплексообразования (комплексонометрия) — реакции, основанные на образовании прочных комплексных соединений ионов металлов (всех, кроме одновалентных) с комплексоном III (двунатриевой солью этилендиаминтетрауксусной кислоты), при этом изменяются концентрации ионов металлов в титруемом растворе.
[править]Титрование
Титрование — процесс определения титра исследуемого вещества. Титрование производят с помощью бюретки, заполненной титрантом до нулевой отметки. Титровать, начиная от других отметок, не рекомендуется, так как шкала бюретки может быть неравномерной. Заполнение бюреток рабочим раствором производят через воронку или с помощью специальных приспособлений, если бюретка полуавтоматическая. Конечную точку титрования (точку эквивалентности) определяют индикаторами или физико-химическими методами (по электропроводности, светопропусканию, потенциалу индикаторного электрода и т. д.). По количеству пошедшего на титрование рабочего раствора рассчитывают результаты анализа.
[править]Типы титрования
Различают прямое, обратное титрование и титрование заместителя.
При прямом титровании к раствору определяемого вещества (аликвоте или навеске, титруемому веществу) добавляют небольшими порциям раствор титрант (рабочий раствор).
При обратном титровании к раствору определяемого вещества добавляют сначала заведомый избыток специального реагента и затем титруют его остаток, не вступивший в реакцию.
При заместительном титровании к раствору определяемого вещества добавляют сначала заведомый избыток специального реагента и затем титруют один из продуктов реакции между анализируемым веществом и добавленным реагентом.
31. оксидиметрия
Оксидиметрия ( от нем. oxydiren — окислять и ...метрия) — титриметрические методы в аналитической химии, основанные на реакциях окисления-восстановления. В процессе титрования изменяется окислительно-восстановительный потенциал системы, вблизи точки эквивалентности наблюдается резкое изменение потенциала. Оксидиметрию классифицируют в зависимости от применяемого в данной реакции раствора вещества — окислителя или восстановителя. К оксидиметрии относятся перманганатометрия, периметрия, хроматометрия, иодометрия
Иодометрия — титриметрический (объёмный) метод определения веществ, основанных на реакциях окисления-восстановления с участием иода или иодида:
![]()
Преимуществом метода является возможность применения селективного индикатора для определения йода — крахмала.
Иодометрически определяют кислоты:
IO3− + 5I− + 6Н+ = 3I2 + ЗН2О
Перманганатометрия – один из наиболее часто применяемых методов окислительно-восстановительного титрования. В качестве титранта используют раствор перманганата калия, окислительные свойства которого можно регулировать в зависимости от кислотности раствора.
Особенности и возможности метода
Наибольшее распространение в аналитической практике получил перманганатометрический метод определения в кислых средах: восстановление МnО4- до Мn2+ проходит быстро и стехиометрично:
МnО4- + 8Н+ + 5 е- → Мn2+ + 4Н2О.
Особенностью метода является сильное влияние pH на Ео системы (МnО4- + 8Н+ )/Мn2+. При титровании в сильно кислых средах чаще всего используют серную кислоту. Хлороводородную и азотную кислоты применять не следует, так как в их присутствии могут идти конкурирующие окислительно-восстановительные реакции. Восстановление перманганат-иона в щелочной среде протекает последовательно: сначала до мангант-иона МnO42-, а затем до диоксида марганца МnО2:
МnО4- + е- → МnО42-,
МnО42- + 2Н2О + 2е- → МnО2 + 4ОН-.
