
- •Билет №1
- •1. Периодический закон и периодическая система химических элементов д.И.Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
- •2. Предельные углеводороды, общая формула и химическое строение гомологов данного ряда. Свойства и применение метана.
- •Гомологический ряд алканов:
- •Билет №2
- •2. Непредельные углеводороды, общая формула и химическое строение гомологов данного ряда. Свойства и применение этилена.
- •Гомологический ряд алкенов:
- •Билет№ 3
- •Циклопарафины, их химическое строение, свойства, нахождение в природе, практическое значение.
- •Гомологический ряд алканов:
- •Гидрирование.
- •Галогенирование.
- •Дегидрирование.
- •Задача.
- •Билет №4
- •Классификация химических реакций в неорганической и органической химии.
- •Диеновые углеводороды, их химическое строение, свойства, получение и практическое значение. Натуральный и синтетический каучуки.
- •Полимеризация.
- •Каучук и его свойства. Вулканизация каучука
- •Билет №5
- •Обратимость реакций. Химическое равновесие и способы его смещения: изменение концентрации реагирующих веществ, температуры, давления.
- •Получение.
- •Применение.
- •Билет №6
- •Условия, влияющие на скорость реакций.
- •Ароматические углеводороды. Бензол, структурная формула, свойства и получение. Применение бензола и его гомологов.
- •Бромирование.
- •Нитрование.
- •Гидрирование.
- •Билет №7
- •Основные положения теории химического строения органических веществ а.М.Бутлерова. Химическое строение как порядок соединения и взаимного влияния атомов в молекулах.
- •Реакции ионного обмена в водных растворах. Условия их необратимости.
- •Задача.
- •Билет №8
- •Изомерия органических соединений и ее виды.
- •Существует несколько видов изомерии:
- •Классификация неорганических соединений.
- •Опыт и задача.
- •Билет №9
- •Металлы, их положение в периодической системе химических элементов д.И.Менделеева, строение их атомов, металлическая связь. Общие химические свойства металлов.
- •Природные источники углеводородов: нефть, природный газ и их практическое значение.
- •Задача.
- •Билет №10
- •Строение и особенности химической связи в спиртах
- •3.Опыт. Проведение реакций, подтверждающих важнейшие химические свойства глицерина.
- •Билет №11
- •Фенол, его строение, свойства, получение и применение.
- •Задача.
- •Билет №12
- •Электрохимический ряд напряжений металлов. Вытеснение металлов из растворов солей другими металлами.
- •А льдегиды, их химическое строение и свойства. Получение, применение муравьиного и уксусного альдегида.
- •3. Задача.
Бромирование.
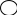
+ Br2 → - Br + HBr
бензол бромбензол
Нитрование.
+ HNO3 → - NO2 + H2O
бензол нитробензол
Бензол вступает в реакции присоединения:
Гидрирование.
+ 3H2 →
бензол циклогексан
Х лорирование. Cl Cl

+ 3Cl2 → Cl Cl
Cl Cl
бензол гексахлорциклогексан
Бензол применяется как растворитель и сырье для получения многих ароматических соединений, которые используются для производства красителей (анилин), полимеров (стирол, фенол, анилин), лекарственных препаратов. Нитрованием толуола получают тротил или тол – мощное взрывчатое вещество.
Опыт.
Проведение реакций, подтверждающих характерные свойства кислот.
Лакмус окрашивается в красный цвет.
Взаимодействие с активными металлами.
Zn + 2HCl = ZnCl2 + H2↑
Выделяются пузырьки газа.
Взаимодействие с оксидами металлов.
CuO + H2SO4 = CuSO4 + H2O
Порошок черного цвета растворяется при нагревании. Раствор становится голубого цвета.
Взаимодействие с солями.
AgNO3 + HCl = AgCl↓ + HNO3
Выподает осадок белого цвета.
Взаимодействие с основаниями.
HCl + NaOH = NaCl + H2O
Билет №7
Основные положения теории химического строения органических веществ а.М.Бутлерова. Химическое строение как порядок соединения и взаимного влияния атомов в молекулах.
В 1861 году была разработана теория химического строения органических веществ. Эта теория была охарактеризована Бутлеровым следующим образом: он определил, что свойства веществ зависят от их строения и показал, что его теория имеет большое практическое значение в предсказании новых веществ.
Основные положения теории Бутлерова:
Атомы в молекулах веществ соединены согласно их валентности. Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом образуя различные цепи.
Свойства веществ определяются ни только их качественным и количественным составом, но и порядком соединения атомов в молекуле, то есть химическим строением вещества.
Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
Разработанная теория объяснила строение молекул всех известных органических веществ и их свойств, а также дала возможность теоретически предвидеть существование новых веществ и найти пути их синтеза.
Реакции ионного обмена в водных растворах. Условия их необратимости.
Реакции, протекающие между ионами называются ионными реакциями.
Реакции ионного обмена могут протекать:
а) обратимо, то есть в двух противоположных направлениях;
б) необратимо, то есть до конца.
Условия протекания необратимых реакций.
Образуется осадок.
AgNO3 + HCl = AgCl↓ + HNO3
Образуется малодиссоциируемое вещество (вода).
NaOH + HCl = NaCl + H2O
Образуется газообразное вещество.
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
