
- •1.Основные теоретические модели процесса массоотдачи (пленочная, проникновения, диффузионного пограничного слоя).
- •2.Дифференциальное уравнение ковнективно-диффузионного переноса массы.
- •3.Движущая сила и направление масообменного процесса.
- •4.Уравнения массоотдачи и массопередачи. Связь коэффициентов массоотдачи и массопередачи.
- •5.Подобие массообменных(диффузионных) процессов.Общий вид критериального уравнения для расчета коэффициентов массоотдачи.
- •6.Методы определения общего числа единиц переноса.
- •12. Непрерывно действующая абсорбционно-десорбционная установка.
- •13.Как определить экспериментально коэффициент массопередачи в насадочной абсорбционной колонне?
- •14. Материальный баланс ректификационной колонны непрерывного действия.Уравнения рабочих линий.
- •15.Тепловой баланс ректификационной колонны. Определение расходов греющего пара и охлаждающей воды.
- •16.Теоретически минимальное и оптимальное флегмовое число.
- •17.Влияние расхода флегмы на движущуюся силу процесса, на диаметр и высоту ректификационной колонны, на расходы греющего пара и охлаждающей воды.
- •18.Схема ректификационной установки непрерывного действия.
- •19.Конструкции тарелок ректификационной колонны. Коэффициент обогащения.
- •20.Экстрактивная и азеотропная ректификация.
- •21.Простая перегонка. Перегонка с водяным паром.
- •22.Материальный баланс однократной экстракции. Конструкции экстракторов.
- •23.Расчет противоточной экстракции на основе уравнения массопередачи.
- •24.Адсорбция.Статика и кинетика. Адсорбция в неподвижном слое.
- •25.Как определить экспериментально коэффициент массопередачи в противоточном адсорбере со взвешенным слоем адсорбента.
- •26. Сушильные агенты, их основные параметры и связь между ними.
- •27.Материальный баланс конвективной сушки. Удельный расход сушильного агента.
- •28.Тепловой баланс конвективной сушки. Удельный расход теплоты. Тепловой кпд.
- •29.Изображение основных вариантов сушильных процессов на диаграмме I-X.
- •30.Конструкции конвективных сушилок.
- •31.Контактная, радиационная, высокочастотная и сублимационная сушка.
- •32.Расчет времени процесса конвективной сушки.Вывод уравнений.
- •33.Кинетика процесса конвективной сушки.
- •34.Схема сушильной установки со взвешенным слоем дисперсного материала.
- •1.Основные теоретические модели процесса массоотдачи (пленочная, проникновения, диффузионного пограничного слоя).
- •2.Дифференциальное уравнение ковнективно-диффузионного переноса массы.
21.Простая перегонка. Перегонка с водяным паром.
Простая
перегонка или однократный акт разделения
жидкой смеси, состоит в том, что исходную
смесь нагревают до
 ,после чего продолжают подводить к
кипящей смеси теплоту, которая требуется
на процесс парообразования.В равновесном
составе образующихся паров более
летучего компонента относительно
больше.Эти пары непрерывно отводятся
в конденсатор, где они полностью
конденсируются, образуя новую жидкую
смесь, обогащенную летучим компонентом
по сравнению с исходной жидкой смесью.
При конденсации выделяется теплота
фазового перехода, поэтому для её отвода
в конденсатор необходимо подавать воду
или другой тепловоспринимающий агент.
Идет процесс для тех систем, которые
нерастворимы в воде и вода в них не
растворима.Используется для очистки
органических веществ от примесей
(бензол, толуол).1.Бензол
,после чего продолжают подводить к
кипящей смеси теплоту, которая требуется
на процесс парообразования.В равновесном
составе образующихся паров более
летучего компонента относительно
больше.Эти пары непрерывно отводятся
в конденсатор, где они полностью
конденсируются, образуя новую жидкую
смесь, обогащенную летучим компонентом
по сравнению с исходной жидкой смесью.
При конденсации выделяется теплота
фазового перехода, поэтому для её отвода
в конденсатор необходимо подавать воду
или другой тепловоспринимающий агент.
Идет процесс для тех систем, которые
нерастворимы в воде и вода в них не
растворима.Используется для очистки
органических веществ от примесей
(бензол, толуол).1.Бензол
 ;
2.Толуол
;
2.Толуол
 ;
3.Финол
;
4.
;
3.Финол
;
4.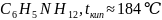 ;
5.
;
5. ;
;
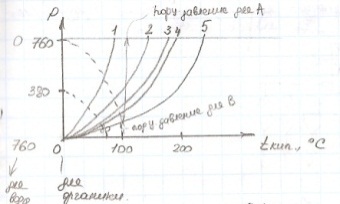
----вода;
все точки М сместятся при Р=380 мм.рт.ст.
и
 Перегонка
с водяным паром:равновесные
диаграммы для систем, компоненты которой
не растворяются друг в друге.Если
жидкости не растворяются друг в друге,
то по уравнению Гиббса(2 жидкости+паровая
фаза)=> 1 степень свободы, а система
описывается 3-мя параметрами (Т,Р и
составом).Если
Т=const,
A
–легколетучий компонент.Парциальные
давления=насыщенным давлениям. А и В
не зависят друг от друга, П-общее
давление.
Перегонка
с водяным паром:равновесные
диаграммы для систем, компоненты которой
не растворяются друг в друге.Если
жидкости не растворяются друг в друге,
то по уравнению Гиббса(2 жидкости+паровая
фаза)=> 1 степень свободы, а система
описывается 3-мя параметрами (Т,Р и
составом).Если
Т=const,
A
–легколетучий компонент.Парциальные
давления=насыщенным давлениям. А и В
не зависят друг от друга, П-общее
давление. смеси будет ниже
любого из компонентов.
смеси будет ниже
любого из компонентов.

Если Р=const, 1-линия кипения, 2-линия конденсации.Смесь будет кипеть при меньшей, чем компонентов.


Если желаем получить ха, то нужно изменить давление=> точка М сдвигается.
22.Материальный баланс однократной экстракции. Конструкции экстракторов.
1.Смесительно-отстойный экстрактор. Может работать непрерывно и периодически.

 – первичный
растворитель (х-концентрация компонента
в первичном растворителе);
– первичный
растворитель (х-концентрация компонента
в первичном растворителе);
 – вторичный растворитель,
2-отстойник,1-смеситель,
– вторичный растворитель,
2-отстойник,1-смеситель,
 – рафинад,
– рафинад,
 – экстракт.
– экстракт.
 ;
;
 ;
;
2.Экстрактор ячеичного типа (противоточный). Окна для перелива жидкости сделаны на разном уровне.

3.Роторно-дисковый экстрактор.
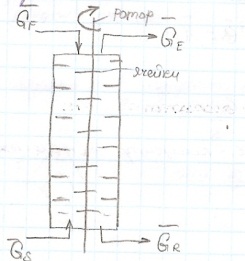
Экстракция состоит из: 1) смешение; 2)отстаивание.

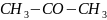 – ацетон,
из него вытекают
– ацетон,
из него вытекают
 водой;
водой; – четыреххлористый углерод подается
сверху, вода-
– четыреххлористый углерод подается
сверху, вода- .
.
 .
Поверхность контакта фаз для пузырей
не определить, поэтому поверхность
берём через объем.
.
Поверхность контакта фаз для пузырей
не определить, поэтому поверхность
берём через объем.
4.Пульсационные колонны.Это тарельчатые колонны большого диаметра.

23.Расчет противоточной экстракции на основе уравнения массопередачи.
 концентрация
компонента в первичном растворителе.
По Y
находим среднюю движущую силу процесса:
концентрация
компонента в первичном растворителе.
По Y
находим среднюю движущую силу процесса:

 находим
в относительных массовых концентрациях.
находим
в относительных массовых концентрациях.
 Вторичный растворитель не содержит Y.
Вторичный растворитель не содержит Y.

24.Адсорбция.Статика и кинетика. Адсорбция в неподвижном слое.
Адсорбция – избирательное поглащение компонента (компонентов) твердой поверхностью из газовой (паровой) и жидкой сред.Используется адсорбция тогда, когда концентрация компонента меньше 50 г/м3. –процесс экзотермический=> возможно снизить температуру и повысить давление. – процесс похож на гетерогенный катализ. – чем более развита поверхность твердого вещества, тем процесс идет лучше. – адсорбент-сорбент. – компонент который поглащается – сорбтив. – чем лучше сжижаемость компонента, тем процесс адсорбции идет лучше. – активация – удаление смолистых веществ из твердого. Сорбенты: - активированный уголь (получают обработкой древесины перегретым паром); -селикогель, ферогель, алюмогель. –солиты-алюмосиликаты. – цеолиты с Ме I , II Менделеева. Диаметр пор: 1.Микропоры D<1,4 нм(нано 10-9м).2.Субмикропоры D=1,4÷3,0 нм. 3.Мезопоры D=3,0÷200 нм. 4.Макропоры D>200 нм. Поверхность твердого тела, с позиции адсорбции, имеют микротрещины, микровпадины, выступы. На поверхности твердого тела есть активные участки, которые притягивают молекулы сорбтива. Теория Ленгмюра (химическая теория нач 19 в.): атом углерода на поверхности с ненасыщенной связью, которые притягивают молекулы сорбтивов.
![]()
Теория Поляни(физическая теория)- силы очень слабые, на подобие Вандервальсовых.Процесс динамический. Сорбтивы притягиваются слоями.Часть сорбентов относится к химической теории, часть к физической.
![]()
Парциальное давление не большое.

Изотерма
работает для одного адсорбента и для
одного сорбтива. Изотерма Френдлиха:
 – уравнение Генри;
– уравнение Генри;
 -
концентрация компонента в газовой
фазе;
-
концентрация компонента в газовой
фазе;
 -
концентрация компонента в твердой
фазе.
-
концентрация компонента в твердой
фазе.



Если
n=0,
т.е. это химическая реакция нулевого
порядка – отражает теорию Ленгмюра.
Существует динамическая равновесная
составляющая и статическая:
 соотношение
соотношение
 т.е.
на 10%. Кинетика процесса:
т.е.
на 10%. Кинетика процесса:
 .
Т.к. поверхность пор не известна, то все
рассчеты ведут через объемный коэффициент.
.
Т.к. поверхность пор не известна, то все
рассчеты ведут через объемный коэффициент.
 .
.
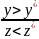 Текущий компонент больше, чем равновесный.
Текущий компонент больше, чем равновесный.
 .
.

Уравнение Шилова:

 -
время действия защитного слоя (с),
-
время действия защитного слоя (с),
 – длина (высота) слоя (м);
– длина (высота) слоя (м);
 – время потери защитного действия
слоя.
– время потери защитного действия
слоя.

-Если изотерма будет вогнутой, то при увеличении слоя сорбента эти кривые будут падать; -Если изотерма – выгнутая, то при каком – то времени будут получаться S- образные II кривые.
