
- •Глава 1. Номенклатура и изомерия органических соединений.
- •Теория строения органических соединений а.М. Бутлерова.
- •Свойства вещества определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т.Е. Химическим строением вещества.
- •Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
- •Основы строения и реакционной способности органических соединений Общая характеристика и классификация органических соединений
- •1.2.1. Заместительная номенклатура
- •Некоторые характеристические группы, обозначаемые только префиксами
- •Порядок старшинства характеристических групп, обозначаемых префиксами и суффиксами
- •Номенклатуре
- •Радикально-функциональная номенклатура
- •Глава 2. Электронное строение органических молекул.
- •Понятие о взаимном влиянии атомов в молекуле и электронные эффекты
- •Системы с замкнутой цепью сопряжения.
- •Кислотно-основные свойства органических соединений. Типы кислот и оснований.
- •Льюисовская кислотность и основность органических соединений.
- •Концепция жестких и мягких кислот и оснований (принцип жмко)
- •Глава 3. Механизмы реакций органических соединений.
- •Классификация органических реакций и их компонентов.
- •Реакции электрофильного присоединения, электрофильного замещения.
- •Реакции нуклеофильного замещения, нуклеофильного присоединения (присоединения-отщепления).
- •Глава 4. Оксосоединения (альдегиды и кетоны).
- •Общая характеристика реакционной способности
- •Альдегиды и кетоны
- •Альдегиды и их производные
- •Лабораторный практикум
- •Ход работы.
- •Глава 5. Карбоновые кислоты. Вопросы к занятию.
- •Строение, номенклатура и физико-химические свойства карбоновых кислот
- •Химические свойства предельных кислот и их производных
- •Декарбоксилирование
- •Кислотно-основные свойства
- •Карбоновые кислоты как ацилирующие реагенты
- •Производные карбоновых кислот, их свойства и взаимные превращения.
- •Функциональные производные карбоновых кислоты
- •Сложные эфиры, имеющие приятный аромат
- •Дикарбоновые кислоты
- •Некоторые дикарбоновые кислоты, их названия и кислотные свойства
- •Ненасыщенные карбоновые кислоты
- •Содержание высших ненасыщенных кислот в растительных маслах, % по массе
- •Лабораторный практикум.
- •Инструкция по технике безопасности.
- •Ход работы.
- •Глава 6. Гетерофункциональные соединения.
- •Поли- и гетерофункциональные соединения, участвующие в процессах жизнедеятельности.
- •Классификация
- •Общая характеристика реакционной способности.
- •Специфические реакции.
- •Аминоспирты.
- •Гидроксикарбоновые кислоты
- •Оксокарбоновые кислоты
- •Отдельные представители фенолокислот
- •Лабораторный практикум.
- •Ход работы.
- •Глава 7. Биологически-активные гетероциклические соединения.
- •Азотосодержащие ароматические гетероциклические соединения
- •Лабораторный практикум.
- •Ход работы.
- •Глава 8. Амиокислоты, пептиды, белки.
- •Строение и свойства аминокислот и пептидов
- •Физиологическая роль и применение в медицине некоторых аминокислот
- •Контрольные вопросы
- •1. Каталитическая функция
- •7. Защитная функция
- •Лабораторный практикум.
- •Ход работы:
- •Глава 9. Углеводы.
- •Строение и свойства углеводов
- •Гетерополисахариды
- •Функции углеводов и их обмен
- •Контрольные вопросы
- •Глава 10. Нуклеиновые кислоты, их структура и свойства. Вопросы к занятию:
- •Нуклеотидный состав и структура днк и рнк.
- •Биологические функции нуклеиновых кислот.
- •Контрольные вопросы
- •Глава 11. Омыляемые и неомыляемые липиды. Стероиды и стероидные гормоны.
- •Липиды. Строение и классификация липидов
- •Простые липиды
- •Константы некоторых жиров животного и растительного происхождения
- •Температура плавления (застывания) некоторых жиров
- •Терпены
- •Стериды. Стероиды и стероидные гормоны.
- •Стероидные гормоны
- •Сложные липиды
- •Лабораторная работа
- •II. Некоторые свойства скипидара.
- •III. Качественные реакции на холестерин и жёлчные кислоты.
- •IV. Качественная реакция на витамин d2 (кальциферол).
- •Глава 12. Адсорбция на подвижной границе раздела фаз.
- •12.1. Поверхностная энергия и поверхностное натяжение.
- •Поверхностное натяжение жидкостей на границе с воздухом (298 к)
- •2. Изотерма Ленгмюра:
- •§7.Лабораторный практикум
- •Ход работы.
- •Глава 13. Адсорбция на неподвижной границе раздела фаз. Изотерма адсорбции уксусной кислоты на угле.
- •Адсорбционные равновесия и процессы на подвижной и неподвижной границах раздела фаз. Влияние различных факторов на величину адсорбции.
- •Контрольные вопросы
- •§7. Лабораторный практикум.
- •Ход работы.
- •Глава 14. Физикохимия дисперсных систем
- •По размерам частиц дисперсной фазы
- •По агрегатному состоянию дисперсной фазы и дисперсионной среды:
- •По характеру взаимодействия дисперсной фазы с дисперсионной средой:
- •Получение и устойчивость дисперсных систем
- •Лабораторный практикум.
- •Ход работы.
- •Литература основная литература
- •Дополнительная литература
Лабораторный практикум
”Альдегиды и кетоны”.
Инструкция по технике безопасности.
Низшие альдегиды обладают резким раздражающим и удушающим действием. Поэтому, работать с ними необходимо под вытяжной системой.
Ход работы.
Опыт №1. Окисление альдегидов гидратом окиси меди (реакция Троммера).
Налейте в пробирку 5-10 капель раствора формалина и 2-3 мл 10%-ного раствора щёлочи. Перемешивая смесь, прилейте к ней по каплям слабый раствор медного купороса до появления очень слабой мути. Нагрейте содержимое. Что наблюдается? Напишите уравнение реакции.
Опыт №2. Окисление альдегидов аммиачным раствором оксида серебра (реакция «серебряного зеркала», реакция Толленса).
В чистую пробирку поместите 3 капли 0,2 Н AgNO3, прибавьте 8-10 капель 2Н NH4OH до растворения образующегося осадка гидроксида серебра. К прозрачному раствору добавьте 3 капли 2%-ного раствора формалина или уксусного альдегида. Слабо нагрейте смесь. Что наблюдаете? Напишите уравнение реакции.
Опыт №3. Йодоформная проба на ацетон.
К раствору ацетона прибавьте около 1 мл раствора йода. Сюда же, перемешивая, прилейте по каплям раствор едкого натра – столько. Чтобы жидкость обесцветилась. Что наблюдается? Какой ощущаете запах? Запишите результаты и схему образования йодоформа из ацетона.
Опыт№4. Получение оксима ацетона.
В пробирку поместите по одной лопаточке солянокислого гидроксил амина, безводной соды и 10-15 капель воды. Подождите пока выделится основная масса СО2, затем охладите и добавьте при хорошем перемешивании 15 капель ацетона. Смесь разогревается и выпадают кристаллы оксима ацетона. Напишите уравнение реакции.
Опыт №5. получение динитрофенилгидразона.
В пробирку поместите одну лопаточку 2,4-динитрофенилгидразина и такое же количество CH3COONa (кристаллы), добавьте 1 мл 2 Н раствор HCl. Хорошо перемешайте и прибавьте 2-3 капли чистого ацетона. При сильном встряхивании образуется жёлтый кристаллический осадок гидразона ацетона. Напишите схему реакции образования 2,4-динитрофенилгидразона ацетона.
Глава 5. Карбоновые кислоты. Вопросы к занятию.
Электронное строение карбоксильной группы.
Кислотность и основность карбоновых кислот с точки зрения протолитической теории.
Влияние на кислотность карбоновых кислот структуры органического заместителя в молекуле кислоты.
Классификация, изомерия и номенклатура карбоновых кислот.
Химические свойства карбоновых кислот.
Механизм реакции этерефикации.
Хлорангидриды, ангидриды, амины и нитрилы производные карбоновых кислот.
Ди- и трикарбоновые кислоты и особенности их поведения.
Медико-биологическое значение карбоновых кислот.
Строение, номенклатура и физико-химические свойства карбоновых кислот
Органические
соединения, содержащие карбоксильную
группу![]() называются
одноосновными
карбоновыми кислотами, две - двухосновными
и т. д. В
зависимости от природы углеводородного
остатка различают карбоновые
кислоты: предельные, непредельные,
ароматические,
гетероароматические, гидрокси- и
оксокислоты, аминокислоты
и др. Одноосновные карбоновые кислоты
общей формулы
CnH2n+1COOH
называются предельными
кислотами.
называются
одноосновными
карбоновыми кислотами, две - двухосновными
и т. д. В
зависимости от природы углеводородного
остатка различают карбоновые
кислоты: предельные, непредельные,
ароматические,
гетероароматические, гидрокси- и
оксокислоты, аминокислоты
и др. Одноосновные карбоновые кислоты
общей формулы
CnH2n+1COOH
называются предельными
кислотами.
По систематической номенклатуре ИЮПАК названия карбоновых кислот образуют от названий родоначальных углеводородов с тем же числом атомов углерода с добавлением окончания -овая кислота. Названия циклических и ароматических карбоновых кислот образуют добавлением к названию родоначального углеводорода слов карбоновая кислота. Нумерацию цепи начинают с атома углерода карбоксильной группы. Для кислот использу-
ются и тривиальные названия, которые применяют также для замещенных кислот, обозначая положение заместителей греческими буквами. В этом случае углеродный атом, соседний с карбоксильной группой, обозначается как α-углерод, затем β-углерод, γ-углерод:
γ β α
R—СН2—СН3—СН2СООН и т. д.
Для
названия аниона карбоновой кислоты
RCOOӨ
используется
ее латинское тривиальное название с
суффиксом -am,
a
для
названия ее молекулярного остатка без
гидроксильной группы,
т. е. ацила
![]() - то же название, но с суффиксом -ил.
Примеры
тривиальных и систематических названий
некоторых карбоновых кислот, их
анионов и ацильных групп приведены
в табл. 9.
- то же название, но с суффиксом -ил.
Примеры
тривиальных и систематических названий
некоторых карбоновых кислот, их
анионов и ацильных групп приведены
в табл. 9.
Название функциональных производных карбоновых кислот (эфиров, амидов и т. д.) формируется на основе названий их ацильного остатка.
Низшие предельные монокарбоновые кислоты (C1—C9) представляют собой жидкости, а высшие предельные и ароматические кислоты - твердые вещества. Для карбоновых кислот характерна значительная межмолекулярная ассоциация вследствие образования циклических димеров или линейных ассоциатов за счет водородных связей:
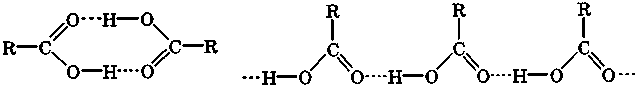
ассоциативный линейные ассоциаты
циклический димер
Таблица 9
Тривиальные и систематические названия некоторых монокарбоновых кислот
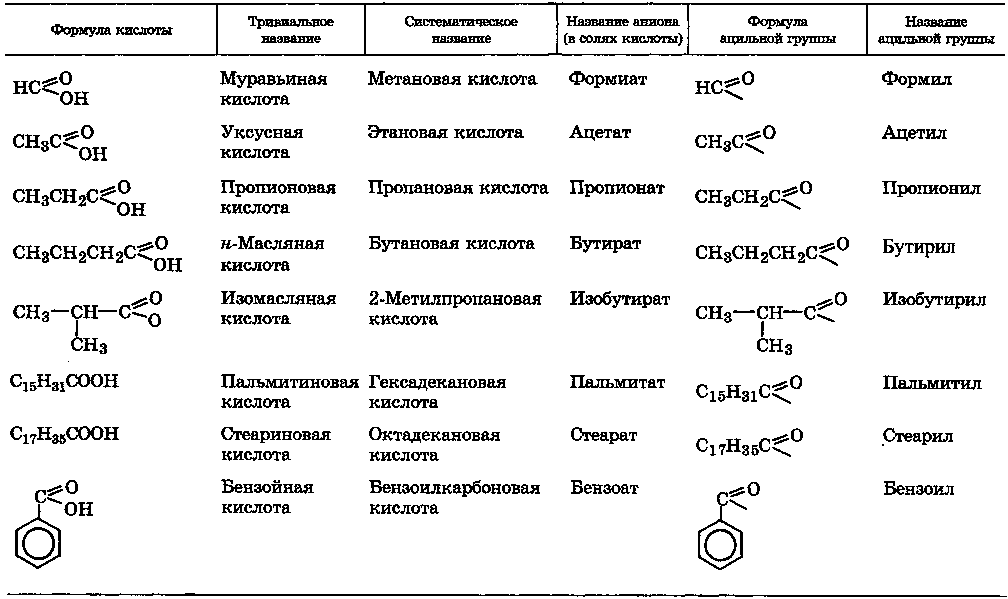
Плавление высших карбоновых кислот, молекулы которых имеют явно анизометрическую форму, происходит постепенно. В интервале от температуры начала плавления до температуры просветления они могут находиться в жидкокристаллическом состоянии (разд. 3.2.3).
Молекулы карбоновых кислот дифильны, так как содержат гидрофильный фрагмент — карбоксильную группу —СООН и гидрофобный фрагмент — углеводородную цепь —R. С увеличением длины последней дифильность молекул увеличивается, а растворимость кислот в воде уменьшается. Высшие карбоновые кислоты алифатического ряда, начиная с С10, в воде практически нерастворимы, а растворимость их солей сильно ограничена. Поэтому соли высших кислот образуют истинные растворы только при низких концентрациях, а при более высоких концентрациях - коллоидные растворы. Вследствие анизометричности молекул высших карбоновых кислот, их солей, а также их ассоциатов (мицелл) коллоидные растворы этих веществ могут находиться в лиотропном жидкокристаллическом состоянии (разд. 3.2.3 и 27.3.2).
Первые гомологи предельных кислот — муравьиная, уксусная и пропионовая кислоты - имеют резкий раздражающий запах, а при попадании на слизистые ткани вызывают их ожог.
