
- •Кафедра «Общая химия, физика и химия композиционных материалов» Курсовая работа по неорганической и аналитической химии «Свойства металла и его соединений».
- •2.Свойства соединений данного химического элемента
- •3 Состояние электролита в растворе.
- •4.Окислительно-восстановительные процессы
- •5. Электрохимические свойства металлов
Министерство образования и науки Российской Федерации
«МАТИ»-РГТУ им. К.Э.Циолковского
Кафедра «Общая химия, физика и химия композиционных материалов» Курсовая работа по неорганической и аналитической химии «Свойства металла и его соединений».
Студент: Саиткулов И.М.
Факультет № 4
Группа:4МТМ-1ДБ-058
Преподаватель: Белая А.В.
Отметка о сдаче
1.1Электронная формула висмута имеет вид: 1s2|2s22p6|3s23p63d10|4s24p64d104f14|5s25p65d10|6s26p3
1.2Порядковый номер висмута в периодической системе химических элементов Д.И. Менделеева – 83. Номер элемента обозначает заряд ярда, следовательно у висмута заряд ядра - +83, масса ядра – 208,98. Висмут находится в пятой группе, в главной подгруппе. Номер периода указывает на количество электронных слоев. Номер группы обозначает количество валентных электронов. Главная подгруппа указывает на то, что висмут относится к s или p - элементам. Так как последний валентный подуровень 6p, следовательно висмут относится к p-элементам. Эффект провала электрона невозможен так как электрон может «провалиться только» на f-орбиталь 5 уровня, что невозможно, потому что f-орбиталь заполняется только у f-элементов, а эти элементы являются лантаноидами и актиноидами.
1.3Висмут имеет два валентных электрона на s-орбитали и три валентных электрона на p-орбитали внешнего слоя.
1.4Квантовые числа для каждого валентного электрона:
|
6s1 |
6s2 |
6p1 |
6p2 |
6p3 |
N |
6 |
6 |
6 |
6 |
6 |
L |
0 |
0 |
1 |
1 |
1 |
ml |
0 |
0 |
-1 |
0 |
+1 |
ms |
+1/2 |
-1/2 |
+1/2 |
+1/2 |
+1/2 |
1.5 Висмут – металл, т.к. его атомы отдают электроны, превращаясь в положительные ионы. Также можно определить принадлежность его к металлам по ряду физических свойств.
1.6Распределение валентных электронов по энергетическим уровням:
↑ |
↑ |
↑ |
↑↓ |
В возбужденном состоянии один электрон с 6s-орбитали перескакивает на 6d, образуя ковалентность равную пяти:
↑ |
|
|
|
|
↑ |
↑ |
↑ |
↑ |
Характерная степень окисления равна +3. Так же висмут может проявлять степень окисления равную +5.
2.Свойства соединений данного химического элемента
2.1 +83 Bi …..6s26p3
↑ |
↑ |
↑ |
↑↓ |
Характерная степень окисления равна +3. Так же висмут может проявлять степень окисления равную +5.
Висмут с характерным степенем окисления образует следующий оксид:
Bi+32O-23 – окись висмута 6s26p0, К=3, амфотерный оксид т.к. сепень окисления висмута равна +3.
2.2 Оксиду висмута(III) Bi+32O-23 соответствует основание Bi+3(OH)3-
а) Взаимодействуя с сильными кислотами, амфотерные оксиды и гидроксиды проявляют основные свойства:
Bi2O3+6HCl=2BiCl3+3H2O
2Bi(OH)3+3H2SO4=Bi2(SO4)3+6H2O
б) Взаимодействуя с щелочами амфотерные гидроксиды и оксиды проявляют кислотные свойства :
Bi2O3+2KOH=2KBiO2+H2O
Bi(OH)3+NaOH=Na[Bi(OH)4]
Уравнение реакции электролитической диссоциации гидроксида:
B i2O3*aq 2Bi+3*aq+3O-2*aq
i2O3*aq 2Bi+3*aq+3O-2*aq
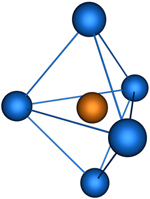
2.3 BiF5-фторид висмута SP3d-q5 гибридизация
тригональная-бипирамида
2.4 BiI3+KIK+[BiI4]-- соль анионного типа(тетра йода висмутат калия)
Внутренняя сфера анион.
Центральным ионом комплексообразователя является Bi+3
Лигандом является I-
Координационное число=4
Определяем донор и акцептор во внутренней сфере. Для этого необходимо написать электронную формулу:
Bi0….6s26p3
Bi0-3eBi+3…6s26p0
|
|
|
- предоставляет свободные ячейки
↑↓ |
I0…5s25p5
I0+eI-…5s25p6
↑↓ |
↑↓ |
↑↓ |
↑↓ |
Вывод:Bi+3-акцептор, I—донор
Уравнение электролитической диссоциации комплексного соединения. Данный процесс протекает в 2-е стадии:
В первой стадии реакция необратима . В процессе реакции образуется гидротированный ион внутренней и внешней сферы
K+[BiI4]-+aqK+*aq+[BiI4]-*aq
Обратимый процесс,const равновесия данной реакции является const нестойкости комплексного соединения
[ Bi+3I-4]-+aq Bi+3*aq+4I-*aq
Kн=CBi+3*C4I-/C[BiI4]-
