
- •Загальні правила виконання лабораторних робіт
- •Правила техніки безпеки
- •Перша допомога при нещасних випадках
- •Тема: аналитичні терези та лабораторний посуд.
- •Контрольні питання
- •Тема: гравіметричний аналіз (ваговий аналіз)
- •Основні операції вагового аналізу
- •Лабораторна робота № 2 Визначення вологості мінеральних добрив.
- •Ход роботи.
- •Зважування при висушуванні солі:
- •Лабораторна робота № 3 Визначення барію в хлориді барію гравіметричним методом.
- •Ход роботи.
- •5.Обчислення.
- •Контрольні питання
- •Тема: титриметричний аналіз (об’ємний аналіз)
- •Лабораторна робота № 4 Приготування робочого розчину соляної кислоти.
- •Хід роботи.
- •4.Обчислення.
- •Контрольні питання
- •Тема: метод нейтралізації
- •Лабораторна робота № 5 Визначення вмісту лугу у розчині.
- •Ход роботи.
- •Лабораторна робота № 6 Визначення вмісту гідрокарбонату натрію в питній соді.
- •Ход роботи.
- •Контрольні питання
- •Тема: комплексонометрія
- •Лабораторна робота № 7 Визначення загальної жорсткості води методом комплексонометрії.
- •Ход роботи.
- •Контрольні питання
- •Тема: редоксиметрія
- •Лабораторна робота № 8 Визначення пероксиду водню методом перманганатометрії
- •Ход роботи
- •Контрольні питання
- •Тема: фотометричний аналіз
- •Лабораторна робота № 9 Визначення міді в розчинах фотометричним методом.
- •Ход роботи.
- •Контрольні питання
- •Тема: хроматографічний аналіз
- •Лабораторна робота № 10 Розділення іонів заліза і міді за допомогою хроматографії на папері.
- •Ход роботи.
- •Контрольні питання
- •Тема: потенціометрія
- •Лабораторна робота № 11 Визначення рН розчинів за допомогою рН-метру.
- •Ход роботи
- •Контрольні питання
- •Рекомендована література.
Тема: фотометричний аналіз
Фотометричний метод базується на вибірковому поглинанні електромагнітного випромінення речовиною. Електромагнітне випромінення характеризується довжиною хвилі. В спектрофотометрії використовують ультрафіолетовий (УФ) спектр – довжина хвилі до 400 нм, видимий спектр – 400-700 нм, інфрачервоний (ІЧ) спектр – більше 700 нм. УФ та видимий спектри викликають зміну енергії валентних електронів, ІЧ спектр призводить до зміни енергії коливання молекул. Вибірковість поглинання легко спостерігається, якщо система поглинає випромінення видимої частини спектру.
Колориметрія є частиною спектрофотометричного аналізу, яка базується на утворенні або руйнуванні забарвлених сполук, де кількість продукту пропорційна інтенсивності забарвлення. В колориметричному аналізі використовуються реакції різних типів. Головним є те, що визначає мий компонент Х за допомогою реактиву R переводять в забарвлену сполуку, а інтенсивність її забарвлення порівнюють з забарвленням стандартного розчину з відомою концентрацією речовини. Коли монохроматичний пучок світла проходить крізь забарвлений розчин, частина світла поглинається, а частина проходить крізь розчин, причому інтенсивність світла зменшується. Оптична густина розчину А дорівнює логарифму відношення початкової та кінцевої інтенсивності світла.
Закон Бугера-Ламберта-Бера встановлює залежність оптичної густини забарвленого розчину від концентрації, товщини шару і молярного коефіцієнта поглинання і має такий математичний вираз:
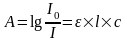
де, - коефіцієнт молярного коефіцієнта поглинання,
l - товщина шару забарвленого розчину,
c- концентрація забарвленого розчину.
Методи реєстрації даних можуть бути візуальними або інструментальними. Серед перших виділяють метод стандартних серій, метод колориметричного титрування, метод розведення. Але використання приладів здатних реєструвати інтенсивність світла за допомогою фотоелементів прискорює та підвищує чутливість цього методу. В фотоколориметрах використовуються світлофільтри, які здатні вибрати ту частину спектру, яка найбільш сильно поглинається забарвленим розчином.
Техніка роботи на фотоколориметрах залежно від його марки наводиться у інструкції до нього.
Лабораторна робота № 9 Визначення міді в розчинах фотометричним методом.
Мета роботи: ознайомитись з методикою фотометричного аналізу, визначити вміст Cu2+ в розчині за допомогою фотоколориметру.
Прилади та реактиви: колби мірні (50,1000мл), годинникове скло, аналітичні терези, піпетки (1-10мл), фотоколориметр (КФК-2), кювети (h=1см), фільтровальний папір, пробірки. Розчини: гідроксиду амонію (1:3), концентрованої сірчаної кислоти. Мідний купорос перекристалізований. Дистильована вода.
Принцип методу: метод ґрунтується на утворенні іонами міді і гідроксидом амонію аміачного комплексу міді Cu(NH3)42+ , що має сине забарвлення.
