
Лабораторная работа №22(1)
.docСАНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ ЭЛЕКТРОТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
КАФЕДРА ФИЗИКИ
Отчет по лабораторной работе №2 по термодинамике
«Изучение термодинамического цикла при сжатие и расширение воздуха»
Выполнил: Лебедев. А.А.
гр. 2362
ФКТИ
Преподаватель: Альтмарк А.М.
г. Санкт-Петербург 2002 г.
Цель работы: исследование политропно-изохорно-изотермического цикла, измерение показателя поли фоны; построение цикла.
Приборы и принадлежности; баллон с воздухом, манометр, микрокомпрессор, лабораторные термометр и барометр.
Исследуемые закономерности
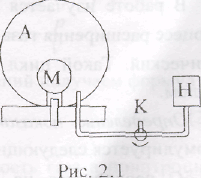
Метод измерений. Используемая в работе установка изображена на рис. 2.1. Баллон А объёмом V1 может сообщаться либо с насосом Н. либо с атмосферой. Внутрь баллона помещён манометр М, измеряющий избыточное давление. Одно деление шкалы равно 4 мм вод. ст., что составляет 40 Па. Рабочим газом является воздух. В исходном состоянии параметры состояния воздуха следующие: давление р2 и температура T1. Диаграмма исследуемого цикла в координатах давления р и объёма V показана на рис. 2.2.
В
исходном состоянии воздух имеет
давление![]() и
температуру
и
температуру![]() Насосом
в баллон накачивают воздух до
давления
Насосом
в баллон накачивают воздух до
давления![]() (состояние
/
(состояние
/
![]() При сжатии воздух нагревается, поэтому
после закрытия крана необходимо выждать
некоторое время, пока температура
воздуха в баллоне не сравняется с
температурой окружающей среды.
При сжатии воздух нагревается, поэтому
после закрытия крана необходимо выждать
некоторое время, пока температура
воздуха в баллоне не сравняется с
температурой окружающей среды.
Затем
воздух выпускают через кран К в атмосферу
в течение нескольких секунд. Когда
стрелка манометра приблизится к нулю,
кран закрывают. В этот момент давление
воздуха баллоне становится![]() (состояние
(состояние![]() Изменение параметров состояния воздуха
в процессе расширения отражает линия
/-2, которая является политропой.
Изменение параметров состояния воздуха
в процессе расширения отражает линия
/-2, которая является политропой.
После
закрытия крана охлаждённый при расширении
воздух и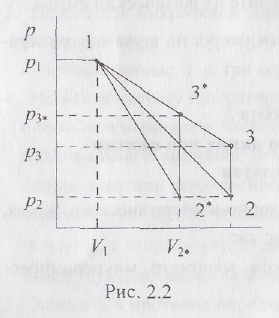 зохорически
нагревается до температуры окружающей
среды в результате теплообмена.
Изменение параметров состояния воздуха
отражает линия 2—3,
которая
является изохорой. Температура воздуха
в баллоне становится равной температуре
в точке /
зохорически
нагревается до температуры окружающей
среды в результате теплообмена.
Изменение параметров состояния воздуха
отражает линия 2—3,
которая
является изохорой. Температура воздуха
в баллоне становится равной температуре
в точке /
![]() следовательно, точки / и 3
лежат
на одной изотерме.
следовательно, точки / и 3
лежат
на одной изотерме.
После
выравнивания температур давление в
баллоне изменится на![]() и
станет Уг
V
и
станет Уг
V
![]() состояние
3
состояние
3![]() Таким
образом,
Таким
образом,![]() -
это изменения давления на участках 1-2
и
2-3.
Участки
1-2
и
1-3
на
диаграмме можно аппроксимировать
прямыми, так как изменения параметров
р, У,
Т в данной
работе малы и много меньше абсолютных
значений соответствующих величин.
-
это изменения давления на участках 1-2
и
2-3.
Участки
1-2
и
1-3
на
диаграмме можно аппроксимировать
прямыми, так как изменения параметров
р, У,
Т в данной
работе малы и много меньше абсолютных
значений соответствующих величин.
В
работе изучается
политропно-изохорно-изотермический![]() цикл.
цикл.
Процесс расширения газа на участке 1-2 можно также рассмотреть как адиабатический. Такой цикл назван адиабатно-изохорно-изотермическим (SVT) циклом.
Определение
показателя политропы. Первое
начало термодинамики формулируется
следующим образом: сообщённое системе
количество теплоты
![]() расходуется на увеличение внутренней
энергии
расходуется на увеличение внутренней
энергии
![]() системы и совершение системой работы
системы и совершение системой работы![]()
![]()
где![]() -теплоёмкость
газа при изохорном процессе.
-теплоёмкость
газа при изохорном процессе.
к Процесс расширения воздуха на участке 1-2 (рис. 2.1) рассматривается как политропный, при котором теплоёмкость газа С остаётся постоянной. Тогда первое начало термодинамики имеет вид
где![]() .
Из этого соотношенияс
.
Из этого соотношенияс![]() помощью уравнения состояния идеального
газа можно получить уравнение политропного
процесса
помощью уравнения состояния идеального
газа можно получить уравнение политропного
процесса![]() или
или![]() ,
где п
- показатель
политропы,
,
где п
- показатель
политропы,
![]()
SVT-цикл.
Полагаем, что процесс адиабатного
расширения воздуха на участке 7-2* (рис.
2.1) обратимый. Адиабатный процесс
происходит без теплообмена с окружающей
средой,![]() ,
поэтому
,
поэтому
![]()
Из
этого соотношения с помощью уравнения
состояния идеального газа можно
получить уравнение адиабатного
процесса
![]() или
или
![]() , где
, где![]() -
показатель адиабаты. Его значение равно
отношению теплоёмкостей газа при
изобарном и изохорном процессах,
-
показатель адиабаты. Его значение равно
отношению теплоёмкостей газа при
изобарном и изохорном процессах,![]() Для
воздуха
Для
воздуха![]() Показатель
политроны п
может
быть определён экспериментально. Выразим
п
через
экспериментально измеренные величины,
для чего продифференцируем уравнения
политропы
Показатель
политроны п
может
быть определён экспериментально. Выразим
п
через
экспериментально измеренные величины,
для чего продифференцируем уравнения
политропы![]() и
изотермы
и
изотермы![]() :
:
![]() - для политропы и
- для политропы и![]() -
для изотермы. Преобразуем соотношения
к виду
-
для изотермы. Преобразуем соотношения
к виду
![]()
При
относительно малых изменениях![]() и
и
![]() тангенс
угла наклона политропы 1-2
и
изотермы 1-3
(см.
рис. 2.1) рассчитывается по формулам
тангенс
угла наклона политропы 1-2
и
изотермы 1-3
(см.
рис. 2.1) рассчитывается по формулам
![]()
где![]() Из
отношения приведенных уравнений получаем
формулу
Из
отношения приведенных уравнений получаем
формулу
![]() (2.1)
(2.1)
Зная n, можно определить мольную теплоемкость газа в политроином процессе (мольные величины обозначаем соответствующими строчными буквами)
![]()
где R
- универсальная
газовая постоянная, равная 8,31 Дж/(К-моль);![]() мольная теплоемкость воздуха при
постоянном объеме. При нормальных
условиях
мольная теплоемкость воздуха при
постоянном объеме. При нормальных
условиях![]() определяется
числом степеней свободы (i)
молекул (считать воздух двухатомным
газом):
определяется
числом степеней свободы (i)
молекул (считать воздух двухатомным
газом):
![]() (2.3)
(2.3)
На участке 1-2 воздух охлаждается, поэтому величина с имеет знак «минус».
Расчёт
холодильного коэффициента.
Холодильный
коэффициент е
определяется
как отношение теплоты, отнятой от
охлаждаемого газа, к затраченной в цикле
работе. Для SVT-цикла
![]() равен
равен
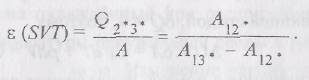
![]()
![]()
Перепишем
выражения для s,
используя экспериментально измеренные
величины давлений, для чего значения
работы![]() определим
i-
графическим
способом. В pV-координатах
(рис. 2.2) они равны площадям трапеций,
основания которых
определим
i-
графическим
способом. В pV-координатах
(рис. 2.2) они равны площадям трапеций,
основания которых![]() ,
а высоты -
,
а высоты -![]()
соответственно. После преобразований получаем:
![]()
В нашем
опыте![]()
![]() больше^
чем
больше^
чем![]() поэтому
отношение холодильных коэффициентов
поэтому
отношение холодильных коэффициентов![]() больше
единицы.
больше
единицы.
Расчет
изменения энтропии. Функция
состояния, дифференциалом которой
является![]() ,
называется энтропией,
,
называется энтропией,
![]()
Отметим, что данное выражение справедливо лишь для обратимых процессов и дает определение разности энтропии, но не ее абсолютное значение.
Выразим
изменение энтропии![]() через
экспериментально измеренные величины
давлений сначала для я^Т-цикла. При
политропном процессе (на участке 1-2)
через
экспериментально измеренные величины
давлений сначала для я^Т-цикла. При
политропном процессе (на участке 1-2)
![]()
Логарифм
отношения заменяем приращениями
соответствующих величин и учитываем,
что для воздуха![]() тогда
тогда
![]()
При изохорном процессе (на участке 2-3) изменение энтропии равно:
![]()
При изотермическом процессе (на участке 3-1)
![]()
Для SVT-цикла изменение энтропии при адиабатном процессе (на участке 1-2 ) равно нулю.
Изменения энтропии при изохорном и изотермическом процессах равны по величине, но различаются знаком:
![]()
При расчетах учесть, что сумма изменений энтропии за цикл равна нулю.
Протокол наблюдений
|
P1 |
P3 |
P2 |
T1 |
V1 |
|
Па |
Па |
Па |
К |
См |
|
|
|
|
|
|
Выполнил: Лебедев А.А.
Проверил: Альтмарк А.М.
Подпись:
