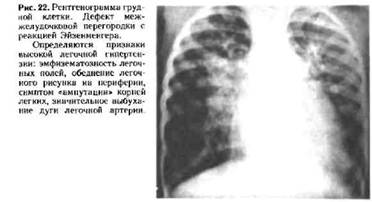
Открытый артериальный проток
Открытый артериальный проток ( dustus arteriosus , боталлов проток ) — сосуд , соединяющий аорту и легочную артерию , сохранивший нормальную для плода структуру после истечения срока его закрытия [ Bankl G ., 1980]. Порок описан Галеном во II веке , но первое сообщение принадлежит G . Aranzio (1564). Название дано в честь итальянского врача Л . Боталло , описавшего порок немного позже .
Анатомия . ОАП располагается в верхнем отделе переднего средостения и прикрыт листком париетальной плевры . Проток отходит от аорты на уровне левой подключичной артерии и в большинстве случаев впадает в ствол легочной артерии в месте его деления на две ветви или в начальную часть левой ветви ; реже встречается право - или двусторонний проток . Он может быть изолированным или в 5 — 10% сочетаться с другими ВПС ( ДМЖП , коарктация аорты , ДМПП , недостаточность митрального клапана ), нередко проток выполняет функцию компенсирующего сообщения при так называемых дуктусзавнсимых пороках ( атрезия легочной артерии , крайняя форма тетрады Фалло , атрезия аорты и др .), при которых если ОАП закрывается , жизнь во внеутробном периоде становится невозможной . ОАП имеют в течение нескольких месяцев жизни 50 % детей , рожденных с массой менее 1700 г ; у 20 % он остается незакрытым

в течение 1 — 2 лет . Проток может быть длинным , узким и извилистым или коротким и широким , диаметр его составляет от 2 — 3 до 30 мм , чаще 3 — 15 мм , длина 3-^25 мм , Систолодиастолический шум слышен , если диаметр протока превышает 4 мм . В зависимости от формы протока существуют различные анатомические типы порока : цилиндрический , воронкообразный , ококчатый , аневризматический . При длительном существовании протока может возникать его кальциноз с переходом на аорту . На аутопсии в 15 % случаев обнаруживают сопутствующие пороки развития внутренних органов ( желудочно - кишечного тракта , мочеполовой системы и др .).
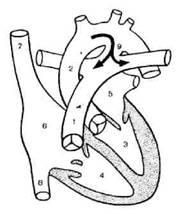
Гемодинамика ( рис . 4). В период внутриутробного развития основное количество крови у плода из правого желудочка (4) и легочного ствола поступает через артериальный проток в аорту После рождения , с первым вдохом легочное сопротивление падает и поднимается давление в аорте , что способствует возникновению обратного сброса ( из аорты в легочную артерию ). Высокое насыщение крови кислородом после включения легочного дыхания вызывает спазм протока ; шум исчезает в течение 15 — 20 ч ( функциональное закрытие ); у недоношенных детей боталлов проток остается открытым более длительно из - за снижения чувствительности к кислороду констрикторного рефлекса . Окончательная облитерация и превращение протока в ligamentutn arteriosum происходит в период от 2- й до 10- й недели внеутробной жизни . Артериальный проток считается аномалией , если по клиническим данным он функционирует спустя 1 — 2 нед после рождения . Закрытие протока начинается в месте его отхождения от легочной артерии , где имеется большое количество гладкомышечных клеток . Возможно , что незакрытие артериального протока связано ^ с дефицитом или недоразвитием гладкомышечных клеток или эластических волокон в его стенке . Увеличенное насыщение крови кислородом является главным стимулом для сокращения гладкомышечных клеток . Выделяющиеся при этом браднкиннн и аиетилхолин способствуют сокращению протока , тогда как простагландин Е поддерживает его в состоянии дилатации . В тех случаях , когда проток не закрывается , эластическая ткань стенки замещается мышечной . При ОАП (9) происходит сброс окснгенированной крови из аорты (2) в легочную артерию ( I ), поэтому это порок бледного типа . Сброс из аорты происходит и во время систолы , и в период диастолы , так как в обе эти фазы давление в аорте превышает таковое в легочной артерии . У детей первых месяцев жизни часто отсутствует диастолический градиент давления между аортой и легочной артерией , поэтому сброс происходит только в систолу . Отсутствие в первые недели жизни большой разницы в давленин между малым и иильшим кругами кровообращения приводит к тому , что при крике , ОРВИ или пневмонии возникает обратный ( веноартериальный ) сброс крови через ОАП , появляется цианоз [ Бураков - ский В . И ., Константинов Б . А ., 1970]. Клинически тяжесть течения порока определяется следующими факторами : I ) размерами протока ; 2) углом отхождения его ( более благоприятно , если он отходит от аорты под острым углом , хуже — если под тупым , поскольку это способствует большему сбросу ); 3) величиной общелегочного сопротивления . При большом протоке значительное количество крови поступает в легочную артерию , затем в левые отделы (3, 5), вызывая их объемную перегрузку . Кроме того , давление в аорте передается непосредственно через проток в легочную артерию , что способствует раннему развитию легочной гипертензии . В таких случаях , если сопротивление в малом круге кровообращения будет превышать таковое в большом , возникает обратный веноартериальный сброс и появляется цианоз . Гемодинамические нарушения при артериаль - jU . ном протоке обусловливают расширение преимущественно левых отделов сердца , но при развитии легочной гипертензии , особенно в ее склеротической стадии , преобладает дилатация и гипертрофия правого желудочка
ДЕФЕКТ МЕЖПРЕДСЕРДНОЙ ПЕРЕГОРОДКИ
Дефект межпредсердной перегородки ( ДМПП ) —сообщение между двумя предсердиями - является результатом ненормального развития первичной и вторичной межпредсердных перегородок и эндокардиальных валиков . У детей старшего возраста и взрослых порок встречается чаще , чем у детей первых месяцев и лет жизни , у которых более распространены тяжелые редкие прроки , приводящие к раннему летальному исходу .
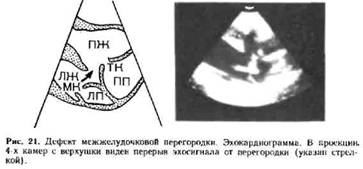
Гемодинамика при ДМПП определяется размерами дефекта , величиной н направлением сброса , состоянием сосудов малого круга кровообращения и миокарда правого желудочка , возрастом больных и др . Суть гемодинамических нарушений — это артерио - венозный сброс из левого в правое предсердие , что приводит к гнперволемни малого круга кровообращения , диастилической перегрузке и дилатации полости правого желудочка ( рис . 9). При интактной межпредсердной перегородке в норме давление в левом предсердии (5) больше , чем в правом (6), на 5 — 6 мм рт . ст . Градиент давления сохраняется и оказывает влияние на величину сброса лишь при небольших размерах дефекта . При больших де -
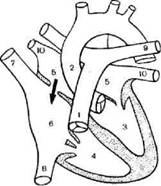
Рис . 9. Схема вторичного дефекта межпредсердной перегородки { указан стрелкой ).
фектах объем сброса крови и его направление определяются не столько разностью давления в предсердиях ( она практически исчезает ), сколько относительной растяжимостью ( комплайнс ) обоих желудочков (3,4) во время диастолы , соотношением конечно - диа - столического давления в их полостях . У детей первых месяцев жизни способность обоих желудочков к растяжению определяется толщиной их стенок , которая однакова или почти одинакова , в результате сброс небольшой и порок остается бессимптомным . После рождения ребенка легочное сопротивление падает , соответственно уменьшается гипертрофия миокарда правого желудочка , он делается более податливым ; одновременно с возрастом увеличивается системное сопротивление , стенка левого желудочка (3) утолщается , способность к диастолическому расслаблению уменьшается . Эти изменения приводят к увеличению левоправого сброса на уровне предсердий . Из - за особенностей сброса основная нагрузка при этом пороке приходится на правые отделы . Левое предсердие увеличивается редко , так как дефект обычно расположен близко к правым легочным венам (10) и кровь из них шунтируется непосредственно в правое предсердие .
ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
Дефект межжелудочковой перегородки ( ДМЖП ) является одним из самых распространенных ВПС .
Размер ДМЖП составляют от 1 до 30 мм и более . Дефект имеет различную форму ( круглый , эллипсовидный ), края его мягкие или фиброзно изменены , иа них можно встретить вегетации при осложнении бактериальным эндокардитом . Выделяют большой ДМЖП его величина сходна с диаметром аорты или превышает его , и небольшой или средних размеров — меньше диаметра аорты , обычно 0,5 — 1,5 см .
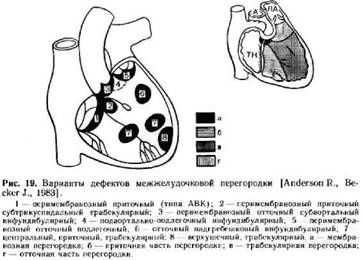
Гемодинамика. Во внутриутробном периоде ДМЖП не оказывает влияния на кровообращение . После рождения ребенка направление сброса определяется размером дефекта , разницей давления в левом и правом желудочках , соотношением общелегочного и общепериферического сопротивлений . В первые дни жизни сброс может быть перекрестным , но вскоре изменяется структура легочных сосудов , падает легочное сопротивление , в результате чего давление в большом круге кровообращения намного превышает таковое в малом . Артериальная кровь сбрасывается из левого в правый желудочек и легочную артерию , откуда возвращается в левые отделы сердца . Давление в правых отделах и легочной артерии определяется величиной сброса и общелегочным сопротивлением . Развитию легочной гипертензии могут препятствовать провисающие створки аортального или трикуспидального клапанов , аномально прикрепляющиеся , или дополнительные хорды , инфундибулярный стеноз легочной артерии .