
- •Сжижение газов
- •Физические основы сжижения газов
- •Жидкое состояние и его характеристики с точки зрения молекулярно - кинетической теории
- •Вязкость жидкостей Динамический коэффициент вязкости
- •Кинематическая вязкость
- •Ньютоновские и неньютоновские жидкости
- •Описание опытов: Максвелловское распределение молекул по скоростям – опыт Штерна. Экспериментальный метод определения числа Авогадро – опыт Перрена Опыт Штерна.
- •Опыт Перрена
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
БРЯНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра: «Общей физики»
Реферат
Темы:
1. «Эффект Джоуля-Томсона. Сжижение газов. Жидкое состояние и его характеристики с точки зрения молекулярно - кинетической теории. Вязкость жидкостей и сверхтекучесть газов.»
2. «Описание опытов: Максвелловское распределение молекул по скоростям – опыт Штерна. Экспериментальный метод определения числа Авогадро – опыт Перрена.»
Студент гр. 11-ПСЖД-1
Поцепай Д. В.
Преподаватель
Некрасова М. Ю.
Брянск 2012
Эффект Джоуля-Томсона
Эффе́ктом Джо́уля — То́мсона называется изменение температуры газа при адиабатическом дросселировании — медленном протекании газа под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). Данный эффект является одним из методов получения низких температур.
Изменение энергии
Изменение энергии газа в ходе этого
процесса будет равно работе:
![]() .
Следовательно, из определения энтальпии
(
.
Следовательно, из определения энтальпии
(![]() )
следует, что процесс
изоэнтальпиен.
)
следует, что процесс
изоэнтальпиен.
Изменение температуры
Изменение температуры при малом
изменении давления (дифференциальный
эффект) в результате процесса
Джоуля — Томсона определяется
производной
![]() ,
называемой коэффициентом Джоуля —
Томсона. С помощью элементарных
преобразований можно получить выражение
для этого коэффициента:
,
называемой коэффициентом Джоуля —
Томсона. С помощью элементарных
преобразований можно получить выражение
для этого коэффициента:
![]()
где
![]() —
теплоёмкость
при постоянном давлении. Для идеального
газа
—
теплоёмкость
при постоянном давлении. Для идеального
газа
![]() ,
а для реального газа он определяется
уравнением
состояния. Если при протекании газа
через пористую перегородку температура
возрастает (
,
а для реального газа он определяется
уравнением
состояния. Если при протекании газа
через пористую перегородку температура
возрастает (![]() ),
то эффект называют отрицательным,
и наоборот, если температура убывает
(
),
то эффект называют отрицательным,
и наоборот, если температура убывает
(![]() ,
то процесс называют положительным.
Температуру, при которой
,
то процесс называют положительным.
Температуру, при которой
![]() меняет
знак, называют температурой инверсии.
меняет
знак, называют температурой инверсии.
Сжижение газов
Сжижение газов включает в себя несколько стадий, необходимых для перевода газа в жидкое состояние. Эти процессы используются для научных, промышленных и коммерческих целей. Многие газы могут быть приведены в жидкое состояние путём простого охлаждения при нормальном атмосферном давлении, другие, как, например, диоксид углерода, требуют для этого также и повышения давления. Сжижение используется для изучения фундаментальных свойств молекул газа (например, межмолекулярных сил взаимодействия), для хранения газов. Газы сжижаются в специальных конденсаторах, которые поглощают теплоту парообразования, и переводятся в газообразное состояние в испарителях, где теплота парообразования выделяется.
Физические основы сжижения газов
Все вещества, в том числе и те, которые в «обычных земных условиях» находятся в газообразном состоянии, могут находиться в трёх основных состояниях — жидком, твёрдом и газообразном. каждое из веществ ведёт себя согласно своей фазовой диаграмме, общий вид которой для всех веществ похож. Согласно этой диаграмме, для сжижения газа необходимо либо понижение температуры, либо увеличение давления, или изменение обоих этих параметров.
Сжижение газов — сложный процесс, который включает в себя множество сжатий и расширений газа для достижения высокого давления и низких температур, используя, например, детандеры.
Жидкое состояние и его характеристики с точки зрения молекулярно - кинетической теории
Кинетическая теория жидкого состояния
Жидкости имеют промежуточную природу между твердыми веществами и газами (рис. 3.12). Например, силы притяжения между частицами (атомами, ионами или молекулами) в жидкости имеют промежуточные значения между этими силами в твердых веществах и в газах. Поэтому частицы жидкости могут удерживаться вместе в определенном объеме. Однако в отличие от твердых веществ силы притяжения недостаточны, чтобы соединять частицы в упорядоченную структуру. Поэтому жидкости не имеют определенной формы. Однако существуют экспериментальные данные, которые свидетельствуют о том, что небольшие группы частиц в жидкостях все же упорядочиваются в небольшие и малоустойчивые кластеры. Это гораздо больше заметно в полярных жидкостях, чем в неполярных. Частицы жидкости, подобно частицам газа, находятся в состоянии непрерывного движения. Впервые это экспериментально обнаружил английский ботаник Роберт Броун в 1827 г. Он наблюдал в микроскоп за крохотными зернышками, плавающими на поверхности воды, и заметил, что они непрерывно совершают хаотические зигзагообразные движения. Это так называемое броуновское движение объясняется столкновениями частиц жидкости с зернышками.
Испарение. С открытой поверхности жидкости некоторые ее частицы постепенно улетают в газовую фазу. Этот процесс называется испарением. Скорость испарения возрастает при следующих условиях: увеличении площади поверхности жидкости, повышении температуры, уменьшении внешнего давления.
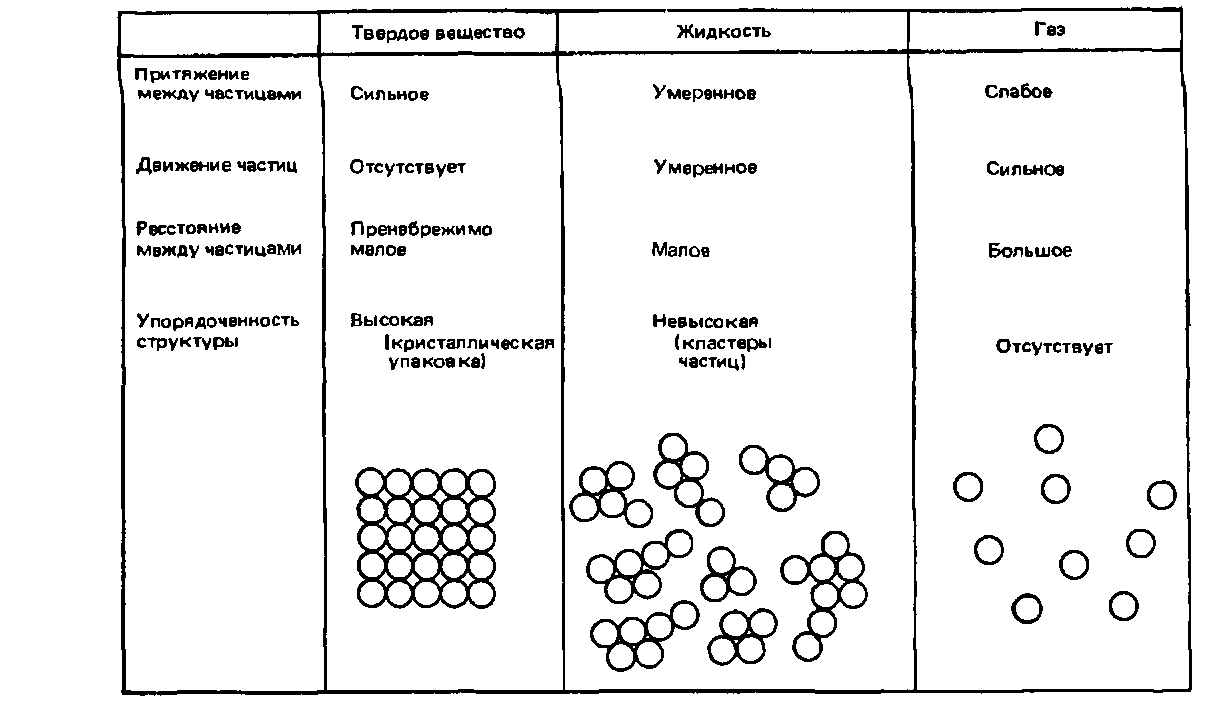 Рис.
3.12. Кинетические представления о
различных физических состояниях
вещества.
Рис.
3.12. Кинетические представления о
различных физических состояниях
вещества.
Вязкость жидкостей и сверхтекучесть газов
Сверхтеку́честь — способность вещества в особом состоянии (квантовой жидкости), возникающем при понижении температуры к абсолютному нулю (термодинамическая фаза), протекать через узкие щели и капилляры без трения. До недавнего времени сверхтекучесть была известна только у жидкого гелия, однако в последние годы сверхтекучесть была обнаружена и в других системах: в разреженных атомных бозе-конденсатах, твёрдом гелии. Сверхтекучесть объясняется следующим образом. Поскольку атомы гелия являются бозонами, квантовая механика допускает нахождение в одном состоянии произвольного числа частиц. Вблизи абсолютного нуля температур все атомы гелия оказываются в основном энергетическом состоянии. Поскольку энергия состояний дискретна, атом может получить не любую энергию, а только такую, которая равна энергетическому зазору между соседними уровнями энергии. Но при низкой температуре энергия столкновений может оказаться меньше этой величины, в результате чего рассеяния энергии попросту не будет происходить. Жидкость будет течь без трения.
Вя́зкость (вну́треннее тре́ние) — одно из явлений переноса, свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. Механизм внутреннего трения в жидкостях и газах заключается в том, что хаотически движущиеся молекулы переносят импульс из одного слоя в другой, что приводит к выравниванию скоростей — это описывается введением силы трения. Вязкость твёрдых тел обладает рядом специфических особенностей и рассматривается обычно отдельно.
